酪氨酸激酶抑制剂的不良反应*
黄烽如,刘连科,钱 依,刘 晋,吴德芹,谢健翔,孙鲁宁**,王永庆**
南京医科大学第一附属医院 1临床药理研究室;2肿瘤科,南京 210029
根据国家癌症中心2018年全国癌症报告,我国癌症发病率与世界水平基本持平,而死亡率明显高于世界水平,肺癌、肝癌、胃癌、食管癌、结直肠癌在各地区均为主要恶性肿瘤的死因[1]。与传统治疗手段如化疗、放疗与手术相比,分子靶向药物以肿瘤组织中特异性高表达蛋白分子或基因片段为靶点,药物与其结合后造成肿瘤细胞特异性凋亡,而对正常细胞影响较小,从而发挥高效、低毒的抗肿瘤作用[2]。蛋白酪氨酸激酶(PTK)在肿瘤的发生、发展过程中起着非常重要的作用,以PTK为靶点进行研发的酪氨酸激酶抑制剂(Tyrosine kinase inhibitor,TKI)成为分子靶向抗肿瘤领域的研究热点,极具发展前景。
1 酪氨酸激酶抑制剂的作用机制
酪氨酸激酶对正常细胞的调节、信号传递、发育发挥着重要的作用,同时也与肿瘤细胞的增殖、分化、迁移、凋亡密切相关[3]。它们能够催化三磷酸腺苷(ATP)的磷酸基团转移到许多重要蛋白质的酪氨酸残基上,使其磷酸化,从而激活各种底物,通过下游信号传导通路使得酪氨酸激酶异常表达,引起细胞增殖调节的紊乱,导致肿瘤的形成[4,5]。TKI通过抑制激酶活性阻断信号传导通路,可以抑制肿瘤的生长和增殖,达到抗肿瘤的作用[6]。
2 酪氨酸激酶抑制剂临床应用现状
伊马替尼自2001年批准上市以来,为慢性髓系白血病治疗带来革命性变化,为TKI类药物打开市场带来机遇,2017年有3种TKIs(依鲁替尼、达沙替尼、伊马替尼)销售总额突破19亿美元。优异的疗效与良好的回报,使TKI类药物数量增长趋势迅猛,已有30多种TKIs经FDA批准上市,中国已批准19种TKIs上市(截至2018年 6月,见表1),内有埃克替尼、安罗替尼、阿帕替尼3种国产原研药。该类药物正逐渐成为慢性髓系白血病、非小细胞肺癌、肾细胞癌和肝细胞癌等肿瘤的一线或二线疗法[7-9],为肿瘤患者带来新的希望。
随着临床应用的深入,TKIs的不良反应渐受关注,发现其在血液、消化、呼吸、皮肤等系统中不良反应发生率较高,且可能多系统并发。不良反应程度多为1~2级,患者多可耐受。在特殊情况下,发生胃肠道穿孔、间质性肺病(ILD)、肺动脉高压等,严重时可危及患者生命。不良反应的不耐受可能导致患者出现新的生理或心理伤害,成为TKIs治疗中断或终止的一个重要原因。
3 酪氨酸激酶抑制剂的不良反应
3.1 皮肤系统的不良反应
皮肤不良反应是酪氨酸激酶抑制剂治疗过程中最常见的毒性反应,主要有皮疹、皮肤干燥、瘙痒、甲沟炎、毛发颜色改变和手足综合征等[10,11],见表2。皮肤不良反应机制尚未完全明确,通常认为是表皮生长因子受体(EGFR)在皮肤中的表达通路受到干扰抑制,并可能与免疫反应相关[12-14]。
皮疹多于治疗后7~10天出现,35%的患者会率先出现皮肤干燥和瘙痒的症状,随后发展为更典型的湿疹和继发并发症[12,15]。皮疹可自愈或反复发生,病程可逆,停药后可逐渐消退。严重的皮肤系统不良反应还包括大疱性、水泡性和剥脱性皮肤改变,有些情况下是致命的。曾有中国男性在使用克唑替尼后、发生毒性表皮坏死松解症(TEN)的死亡案例报告[16]。在伊马替尼和阿法替尼的治疗过程中也有报道过非常罕见的Stevens-Johnson综合征[17,18]。皮肤不良反应会给患者带来很大的心理压力,造成治疗的中断。
患者在用药过程中应注意避光,保持皮肤清洁与湿润。对于已发生的皮肤不良反应,首先确定不良反应等级,患者是否耐受,对于1至2级不良反应一般只做简单的临床处理,使用皮质激素、炉甘石洗剂和皮肤保湿剂等缓解症状,无需减量或停药[19]。若患者不能耐受,且不良反应进行性发展,减量或停药是目前唯一被证实的有效手段。
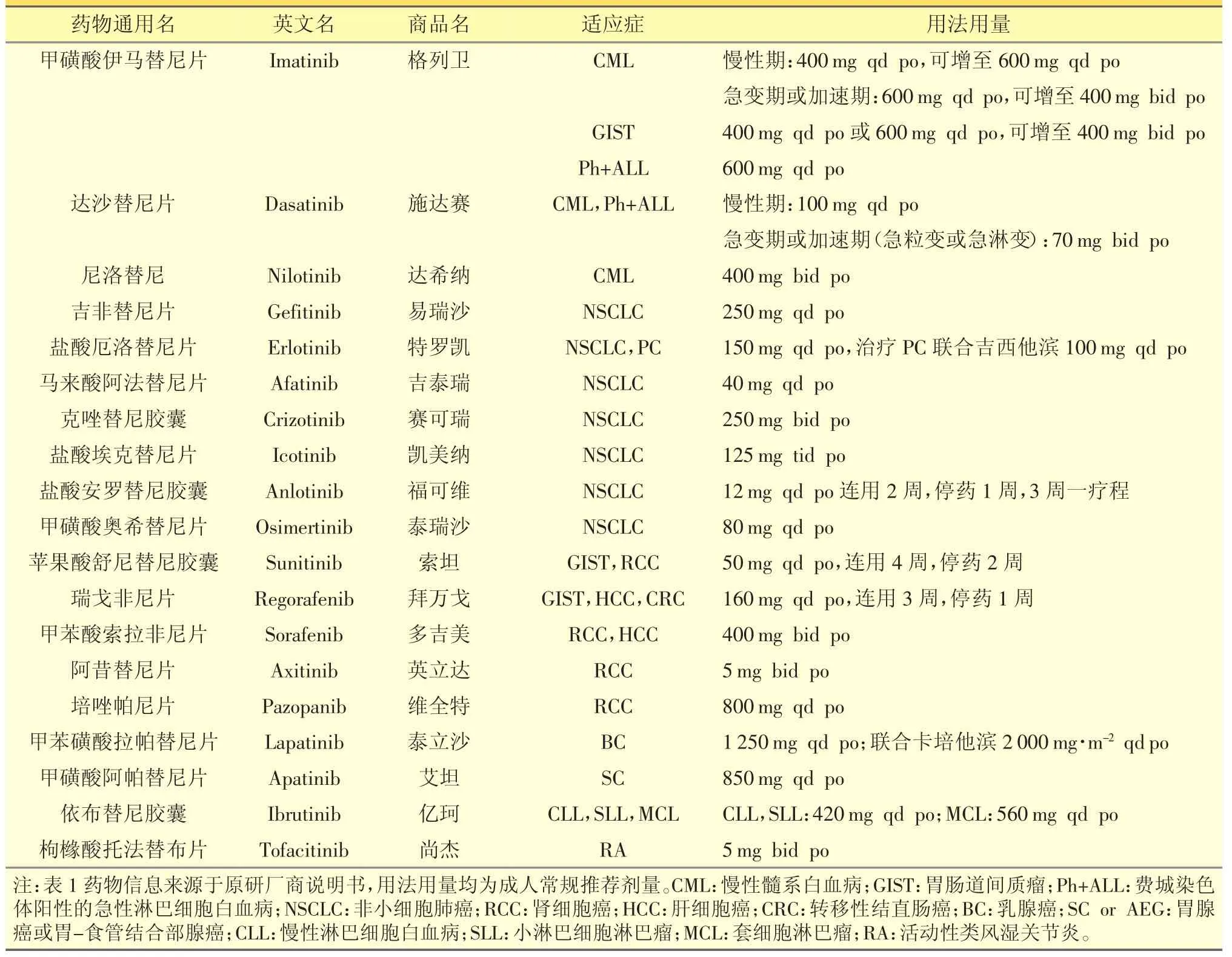
表1 19种CFDA批准的TKIs的适应症及常规用法用量

表2 TKIs皮肤系统的不良反应毒性部位及症状
3.2 消化系统的不良反应
目前国内上市的酪氨酸激酶抑制剂几乎都标注了消化系统不良反应,临床表现主要为恶心、呕吐、腹泻、腹痛、口腔炎等,通常发生的恶心、腹泻、口腔炎等多为轻度或中度,患者多可耐受。荟萃分析表明,阿法替尼在使用过程中最易发生消化系统不良反应,其腹泻发生率超过90%,口腔炎发生率超过 70%[20,21]。
肝毒性是临床上重点监测的消化系统不良反应,多数TKIs经细胞色素P450介导产生活性代谢产物,并通过多种协同通路最终造成肝毒性[22],主要表现为胆红素升高、转氨酶升高等。临床上肝毒性发病不典型,发病时间为1~72周,中位发病时间为7周;肝功能检测恢复正常时间为1~44周,中位恢复时间约为6周[23]。在多数情况下,TKIs造成的肝毒性大多是可逆的;而在肝毒性发现过晚或发生乳酸性酸中毒时,肝脏损伤是致命的[24]。
胃肠道穿孔或瘘管形成是另一需要关注的不良反应。该不良反应虽不常见,但部分病例发生后产生严重后果,在索拉非尼、阿帕替尼、厄洛替尼等药物的临床使用中均有报告[25,26]。患者应避免进食油腻、辛辣等对胃肠道有刺激的食物,进食低纤维、高蛋白食物并充分补液。当患者出现重度或持续性腹泻、恶心、呕吐、厌食症状时,应进行剂量调整并告诫即刻就医,因为这些症状均可能间接引起脱水,宜按照临床指征处理。当患者本身包含其他已知的风险因素(如同时服用类固醇药物、非甾体药物;消化道基础疾病、溃疡、穿孔部位的肠道转移肿瘤;年龄大、吸烟)时,应定期监测胃肠穿孔或瘘管形成的症状。一旦发生这类严重不良反应,应立即停药。
3.3 呼吸系统的不良反应
呼吸系统常见的不良反应表现为呼吸困难、咳嗽、声音嘶哑等,一般为轻、中度。间质性肺病是一种罕见、但可致命的呼吸系统不良反应,通常认为是肺部慢性炎症刺激成纤维细胞迁移、增殖导致肺纤维化的形成[27]。目前已有吉非替尼、厄洛替尼、伊马替尼等TKIs致ILD的个案报道。患者常呈急性呼吸困难伴咳嗽、低热,可在短时间内加重。影像学表现为双肺多发斑片状影或磨玻璃样改变[28,29]。TKIs致ILD的发生率可能存在种族差异,资料显示,日本ILD的发生率为1.6%~4.3%,高于世界范围内其他种族人群的发生率0.3%~1.0%[30]。ILD发生的主要危险因素包括吸烟、较差的体力状态(PS≥2),在CT扫描上正常肺组织覆盖范围≤50%,距非小细胞肺癌诊断时间较短(<6个月),原有间质性肺炎,年龄较大(≥55岁),伴有心脏疾病[31]。一旦确诊是ILD,则应永久停止相关用药,必要时给予适当的治疗。
3.4 血液系统的不良反应
血液学不良反应主要表现为骨髓抑制,包括中性粒细胞减少、血小板减少和贫血,见表3。在所有治疗慢性髓系白血病的TKIs中均将血细胞减少列为警告和注意事项[32]。在任薇如等[33]研究中发现,50例患者接受伊马替尼治疗期间,中性粒细胞减少、血小板减少、贫血的发生率分别为46.0%(23/50)、64.0%(32/50)及 74.0%(37/50)。总体而言,在使用酪氨酸激酶抑制剂治疗过程中发生的血液学不良反应,如骨髓抑制多为1~2级,通常也是可逆的,并且在大多数患者中不需要停药或剂量减少。3~4级血液学实验室异常均不常见,且均发生在治疗的前两个月内[34]。但血液系统不良反应在所有造成患者中断治疗的原因中占很大比例,据于露等[35]研究,在所有停药患者中,有超过50%的患者是因血液系统不良反应。若在CML的治疗过程中持续发生3~4级血液系统不良反应,可以换用达沙替尼、尼洛替尼等二代酪氨酸激酶抑制剂[36,37]。
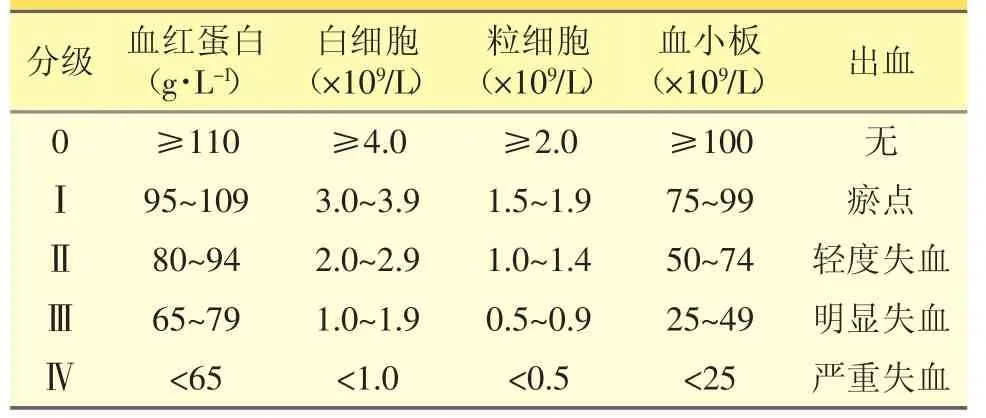
表3 抗癌药物血液系统不良反应分级
3.5 循环系统的不良反应
循环系统不良反应主要表现为高血压、QT间期延长、左心室射血分数下降和心肌梗死等[38],其发生率较低,主要见于索拉非尼、拉帕替尼、厄洛替尼等的不良反应报道。
研究表明,索拉非尼具有高血压、QT间期延长和心机梗死的风险。在一晚期肾细胞癌的治疗中,有16.8%(76/451)患者服用索拉非尼后出现高血压,其中16人处于3~4级;治疗过程中另有12人出现心肌缺血或梗死[39]。QT间期延长可导致室性快速性心律失常或猝死的风险增加[40]。拉帕替尼的循环系统不良反应主要表现为左心室射血分数下降和QT间期延长。目前数据提示,拉帕替尼单药使用或联合用药都具有相对良好的心脏安全性。一项荟萃分析表明,仅有1.4%患者会出现症状性心血管事件,且多为可逆,平均7.3周恢复正常[41]。肺动脉高压是达沙替尼使用过程中需重点关注的不良反应。刘兵城等[42]报道了一例23岁女性患者,在口服达沙替尼70 mg、2次/d治疗慢性髓系白血病,35个月后出现活动后呼吸困难的症状,诊断为肺动脉高压和肺实质病变。Nagasaki J等[43]报道,一例59岁男性患者在口服达沙替尼100 mg、一次/d治疗慢性髓系白血病,19个月后出现呼吸困难,当35个月后再次呼吸困难就诊时,诊断为肺动脉高压。这些病例是在开始达沙替尼治疗后一段时间 (包括治疗一年后)发生肺动脉高压,并在停止达沙替尼治疗后观察到血流动力学和临床参数的改善。
对于使用上述TKIs的患者应常规进行血压与心功能监测,患者应注意情绪激动、饱餐、用力等血压升高因素。在治疗过程中出现恶性高血压,应暂时中断治疗,使用利尿剂、β受体阻滞剂、ACEI等控制血压,若血压无法控制,则应永久停用TKIs药物。对于先天性长QT综合征患者应慎用此类药物,若发生3级不良反应,应暂停用药,待病况至≤1级时恢复用药或减量用药。
3.6 神经系统的不良反应
神经系统不良反应以头痛、眩晕、嗜睡和视觉障碍为主,在多数的酪氨酸激酶抑制剂中发生率超过10%。头痛、眩晕等多为1~2级不良反应,无需剂量调整或停药处理,但依然需要引起重视,妥善处理。可逆性后部脑白质病综合征(RPLS)是一种罕见、但十分严重的不良反应,通常表现为头痛、颅内高压、嗜睡、癫痫、不同程度意识障碍和视觉异常等[44]。Foerster R等[45]报道过1例62岁女性患转移性肾细胞癌,在使用培唑帕尼8周后出现严重头痛、癫痫大发作、左臂麻痹、步态不稳、恶心呕吐等症状,经MRI扫描诊断为RPLS,停药6天后神经症状消失,患者出院。Hadj JO等[46]报道过一例61岁男性患转移性肾细胞癌,在口服舒尼替尼50 mg·d-1第3周期后,发展为全身性强直阵挛性病症,MRI扫描与RPLS一致,抗癫痫药物使用及舒尼替尼停药后,临床症状迅速改善。RPLS发生后应立即停药,并给予降压等对症治疗,正确处理后临床症状即可缓解,因此快速诊断和及时停药是患者预后的关键。
3.7 内分泌系统的不良反应
酪氨酸激酶抑制剂导致的内分泌系统不良反应通常是甲状腺功能减退。在日本某研究课题中发现,有1.5%患者在使用瑞戈非尼时会发生甲状腺功能减退,而舒尼替尼的临床试验与上市后监测的发生率差别较大,分别为16%和35.4%[47]。多个临床实验的荟萃分析表明,有26%(52/197)患者在接受TKIs治疗后出现新发甲状腺功能减退[48]。靶向治疗导致的甲状腺功能亢进一般比较少见,在阿昔替尼某一临床试验中,有4/359例患者(1%)报告甲状腺功能亢进。甲状腺功能亢进常常是甲状腺功能减退前的先驱表现,而且往往伴随高代谢症状,如腹泻、体质量减轻和发热等[49]。因此,使用这3种药物前应进行甲状腺功能检查,所有患者在接受治疗时密切监测甲状腺功能异常的症状和体征,定期监测甲状腺功能。对有甲状腺功能异常症状和体征的患者应给予标准治疗。
3.8 泌尿系统的不良反应
临床上泌尿系统不良反应常表现为无症状的蛋白尿,严重情况下发展为肾衰竭。肾毒性机制复杂,靶向药物可对微血管、肾小球、肾小管、肾间质等造成损伤[50]。Beak SH等[51]报道,有17.6%的患者使用舒尼替尼后发生蛋白尿,0.9%患者出现肾病综合征;70%的患者在停止治疗后蛋白尿得到改善。据资料显示,在培唑帕尼和阿昔替尼的使用过程中蛋白尿发生率较高,可能与糖尿病、高血压的共病状态相关[50]。通常发生的蛋白尿为1~2级或无症状。Ruebner RL等[52]报道了4例儿童恶性肿瘤患者在分别使用伊马替尼、舒尼替尼、达沙替尼和奎扎替尼后、发生了肾病综合征,而在停用TKI后完全缓解了肾病综合征,且未再复发。通常发生的蛋白尿为1~2级,无症状,若出现4级蛋白尿,应立即停药,并注意控制血压,必要时可接受ACEI治疗。
3.9 其他的不良反应
其他不良反应包括感染、出血、伤口愈合并发症等,常见1~2级不良反应还包括水肿、骨骼肌异常、疲劳、发热等。
伊马替尼在治疗各适应症患者时,有50%以上会出现水肿这种常见毒性症状[53]。最常见为眶周水肿,而下肢水肿在某种程度上不常见。大约有2.5%新诊断CML患者服用甲磺酸伊马替尼时发生严重水潴留,如胸水、水肿、肺水肿等。
骨骼肌、结缔组织和骨异常在多数酪氨酸激酶抑制剂使用过程中会出现,包括肌痛、关节痛、骨痛和肌痉挛。这类不良反应发生率虽高,但多以1~2级为主,且无特殊致命毒性反应,对症处理即可缓解。
使用瑞戈非尼、阿昔替尼、阿帕替尼应注意伤口并发症,根据说明书指导用药;手术患者应在手术前30天停用阿帕替尼,至少两周停用瑞戈非尼,术前24小时停用阿昔替尼。术后视伤口愈合情况根据临床判断恢复用药。
4 小 结
酪氨酸激酶抑制剂具有高效、低毒、高选择性的优势,为恶性肿瘤患者带来希望并提高生存质量。在临床应用过程中存在着以下几个问题:(1)1~2级不良反应发生率较高,患者多可耐受,患者个体差异性大,不良反应类型复杂且可能多系统并发,医务人员应当为患者制定个体化的治疗方案,提高患者用药依从性。(2)临床使用过程中不乏3~4级不良反应或某些严重致命性不良反应,导致靶向药物治疗中断;治疗过程中应严密监测此类不良反应,及时发现后应立即停药,对症处理。(3)不良反应机制研究匮乏或尚未完全明确。在新药研发过程中,药企与医疗单位应对不良反应发生机制作进一步研究,开展更多的临床试验,对已知和潜在的不良反应进行长期监测。临床应用中重视不良反应的预防与治疗,保证患者用药获益最大化。

