化学综合实验题的审题策略和答题要领
■湖北省武汉市第三中学 胡承国(特级教师)
回顾近几年全国及各地高考卷的综合实验题,无论是物质制备实验题,还是物质性质探究实验题,背景材料都比较新颖,命题素材较广泛,知识容量较大,考查角度多元,并且难度大。主要考查化学基本仪器的识别和装置的连接,物质的制备原理,反应物及生成物的除杂与分离,物质性质的探究与验证,实验现象的分析与描述,实验结论的评价或计算,等等。若大家掌握了实验题的特点、审题方法及答题要领,就能在高考中提高成绩。
一、实验题的审题策略
解题过程的关键就是审题。具体要做到“五审”,现在结合高考题来分析化学综合实验题的审题策略与解题过程。
例1氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx的反应进行了探究。回答下列问题:
(1)氨气的制备。
①氨气的发生装置可以选择图1中的____(填字母),反应的化学方程式为____。
②欲收集一瓶干燥的氨气,选择图1中的装置,其连接顺序为:发生装置→____(按气流方向,用小写字母表示)。

图1
(2)氨气与二氧化氮的反应。
将上述收集到的NH3充入注射器X 中,往硬质玻璃管Y 中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图2装置进行实验。
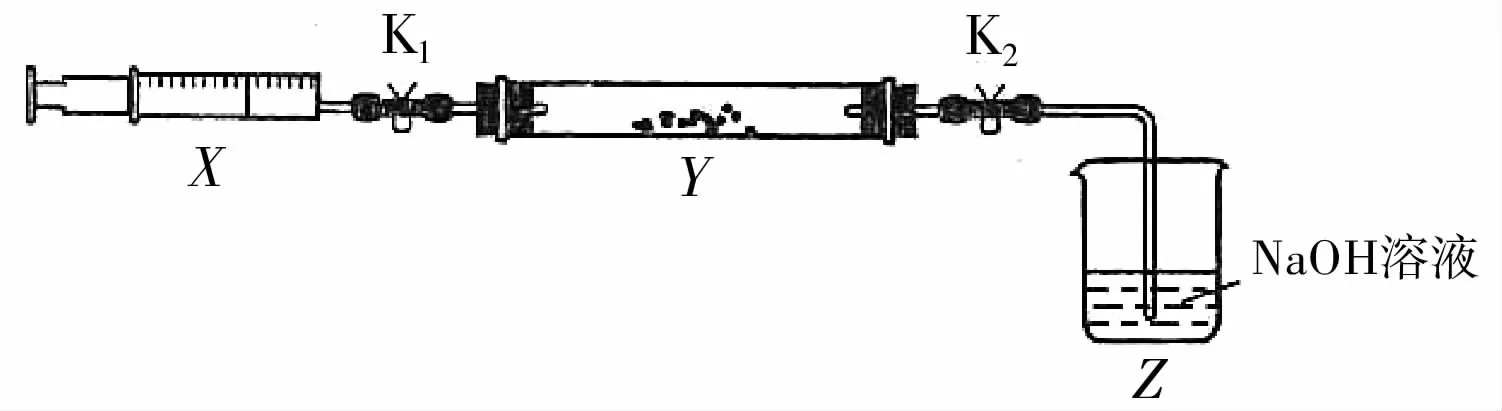
图2
请将表1补充完整。

表1
解析:(一)审主体。仔细阅读题干和实验装置,审查整个实验题的实验目的、实验原理、实验步骤或实验流程。该实验的目的是考查实验室制备并收集纯净的NH3的方法,探究NH3与NO2的反应过程,实验原理为:
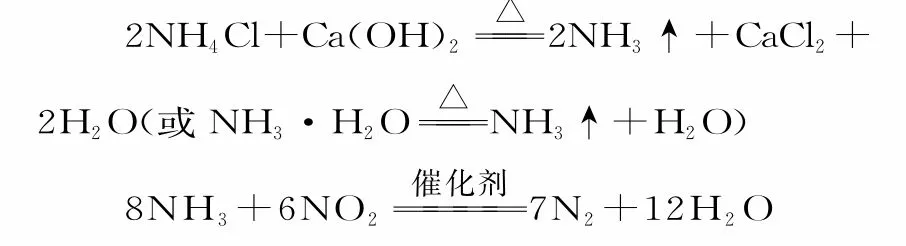
实验步骤为:①制备氨气→除杂→收集氨气→尾气处理;②NH3与NO2混合反应→现象观察→分析并解释。
(二)审信息。看清题目中未学过的知识信息,是解题的关键之一。题中“在一定温度和催化条件下用NH3将NOx还原生成N2”是问题(2)的实验原理。
(三)审装置。(1)依据实验原理(化学方程式)中反应物的状态、用量和反应条件选择合适的仪器。例如:①固体与固体混合物,多盛放在大试管中;②液体与液体混合物多盛放在烧瓶中;③固体与液体混合物,可盛放在大试管或烧瓶中。(2)反应若需要加热,应根据反应所需温度高低选择酒精灯(可满足普通加热条件的反应)、水浴(可满足低于100℃加热条件的反应)或酒精喷灯(可满足加热条件为高温的反应)。(3)反应物易挥发或有副产物生成的反应,需要选择除杂装置,如洗气瓶(除气体杂质)、过滤装置、分液装置、分馏装置等。(4)根据制备物质的量选择合适规格的仪器。(5)有毒尾气的吸收或燃烧,防止空气污染。本题中实验室制NH3:选A(或B)装置。干燥NH3:选C 装置。收集NH3(排空气法):选D 装置,f口进气,e口出气。尾气处理(防倒吸):选F装置。
(四)审操作。(1)仪器的连接。实验仪器大多按物质制备→纯化→性质探究或验证→尾气处理的顺序连接。①若制备物质为液体时,一般按制备(蒸馏烧瓶)→蒸馏(温度计测温)→冷凝(冷凝管)→接收(牛角管、锥形瓶)的思路连接仪器;②若制备物质为气体时,可根据气体的流动方向,按制气→安全瓶(防倒吸)→除杂→性质验证,或物质制备→所制物质的保护,或提纯→尾气处理的思路连接仪器。本题制备NH3的装置为:NH3的发生装置A 或B→d→c→f→e→i。
(2)实验操作。掌握以下常考的实验操作,并能准确描述:①检查装置气密性;②仪器的使用,检查分液漏斗、滴定管等是否漏液,冷凝管中冷却水的流动方向等;③常见气体(如O2、H2、Cl2或NH3等)的检验;④常见离子(如SO2-4、Cl-、Fe3+、Fe2+等)的检验;⑤气体、液体的分离;⑥有害气体的尾气处理;⑦分析某实验操作的作用;⑧某些实验操作的先后顺序;⑨实验题中要求的具体操作。本题第(2)问中的操作为:打开K1,推动注射器活塞,Y 管中现象为红棕色慢慢变浅。将注射器活塞退回原处并固定,待装置恢复到室温,打开K2,Z 中的NaOH 溶液沿导管上升(产生倒吸现象)。
(五)审问题。在前面审题的基础上,正确填好各问的答案。(1)描述实验现象时,一定要具体,要指明固体或溶液的颜色变化、沉淀的出现及溶解、气泡的产生等;描述滴定终点的现象时,一定要指出溶液由什么色变为什么色,且半分钟内不变色。(2)根据实验现象书写化学方程式时,要先分析发生的是什么类型的反应,然后依据相应的书写规则进行书写。(3)根据实验现象得出相关结论,一定要从现象入手推断结论,与现象无关的结论不要写。(4)解释实验现象时,要说明引起变化的具体物质的性质和具体的化学反应变化特征。该题中Y 管中现象:因为发生反应红棕色气体慢慢变浅,因为有水生成,冷凝时有水珠。Z中导管中的液面上升:由NH3与NO2反应的化学方程式可知,反应后气体分子数减小,Y 管中压强小于外界大气压。
答案:(1)①ACaCl2+2NH3↑+2H2O(或B NH3·H2O
②d→c→f→e→i
(2)①红棕色逐渐变浅
③Z中的NaOH 溶液倒吸入Y 管中
④该反应是气体体积减小的反应,Y 内压强小于外压,在大气压的作用下发生倒吸
二、实验题的答题要领
答题准确、具体、规范、全面、简洁是考试得分的最后保障。其中简答问题是综合实验题的主要答题形式,常见问题的答题要领可归纳如下:
1.加某过量试剂,使反应完全进行(或增大转化率、产率)等。
2.加氧化剂,氧化某物质,生成目标产物或除去某些离子。
3.判断能否加其他物质,要考虑是否引入杂质(或影响产物的纯度)等。
4.分离、提纯。过滤、蒸发、萃取、分液、蒸馏等常规操作;从溶液中得到晶体的方法有蒸发浓缩、冷却(蒸发)结晶、过滤、洗涤、干燥。
5.绿色化学。物质的循环利用、废物处理、原子利用率、能量的充分利用、尾气的处理。
6.在空气中或在其他气体中进行的反应或操作,要考虑空气中O2、H2O、CO2或其他气体是否参与反应,或能否达到隔绝空气,防氧化、水解、潮解等目的。
7.判断沉淀是否洗涤干净。取最后一次洗涤滤液少量,滴加合适试剂,检验其中是否还有其他某种离子存在。
8.控制溶液的pH。(1)调节溶液的酸碱性,控制水解(或使其中某些金属离子形成氢氧化物沉淀);(2)“酸作用”还可以除去金属氧化物(膜);(3)“碱作用”还可除去油污,除去铝片氧化膜,溶解铝、二氧化硅等;(4)特定的氧化还原反应需要的酸性条件(或碱性条件)。
9.控制温度(常用水浴、冰浴或油浴)。(1)防止副反应的发生;(2)使化学平衡移动,控制化学反应的方向;(3)控制固体的溶解与结晶(如趁热过滤能防止某物质降温时析出);(4)控制反应速率,使催化剂达到最大活性;(5)加热煮沸,促进水解,聚沉后利于过滤分离,促进溶液中某气体逸出或使某物质达到沸点挥发;(6)趁热过滤,减少因降温而析出的溶质的量;(7)降温,防止物质高温分解或挥发,降温(或减压)可以减少能源成本,降低对设备的要求,也可能使某物质液化分离。
10.洗涤晶体。(1)水洗,通常是为了除去晶体表面水溶性的杂质;(2)冰水洗涤,能洗去晶体表面的杂质离子,且防止晶体在洗涤过程中的溶解损耗;(3)用特定有机试剂清洗晶体,洗去晶体表面的杂质,降低晶体的溶解度,有利于析出,减少损耗等;(4)洗涤沉淀方法,往漏斗中加入蒸馏水至浸没沉淀,待水自然流下后,重复以上操作2~3次。
11.表面处理。用水洗除去表面可溶性杂质,金属晶体可用机械法(打磨)或化学消除表面氧化物,提高光洁度等。
12.常见的实验设计。(1)证明CO2中含有CO:先除去CO2,并证明已除尽,再把气体通入CuO 中,若黑色固体变为红色,生成的气体能使澄清石灰水变浑浊,则证明原混合气体中含有CO。
(2)证明SO2-4中含有SO2-3:往混合液中加入足量的BaCl2溶液,将沉淀溶于足量的盐酸中,若沉淀部分溶解且有刺激性气味(该气体使品红溶液褪色)的气体生成,则证明原混合液中含有SO2-3。
(3)证明含有Fe3+的溶液中含有Fe2+:加入酸性高锰酸钾溶液,若高锰酸钾溶液褪色,则证明原混合液中含有Fe2+(含氯离子以外)。
(4)证明是SO2漂白而不是氯气:加热褪色后的品红溶液,若恢复红色,则说明是SO2漂白。
(5)证明碳酸的酸性强于苯酚:把CO2通入苯酚钠溶液中,若溶液变浑浊,则说明碳酸的酸性强于苯酚。
(6)证明氯气的氧化性强于单质硫:把氯气通入硫化氢溶液中,若有淡黄色沉淀生成,则证明氯气的氧化性强于单质硫。
(7)证明H2C2O4是弱酸:测Na2C2O4的pH,若pH>7,说明H2C2O4是弱酸;或将pH=1的H2C2O4溶液稀释100 倍,pH<3说明H2C2O4是弱酸。
(8)证明SO2中含有CO2:先把混合气体通入足量的高锰酸钾溶液中,再通入品红溶液不褪色,最后通入澄清石灰水中,若澄清石灰水变浑浊,说明含有CO2。
例2某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:
(1)选用如图3所示装置及药品制取CO2。打开弹簧夹,制取CO2。
为了得到干燥、纯净的CO2,产生的气流应依次通过盛有____的洗气瓶(填试剂名称)。反应结束后,关闭弹簧夹,可观察到的现象是_____。不能用稀硫酸代替稀盐酸,其原因是____。
(2)金属钠与二氧化碳反应的实验步骤及现象如表2。
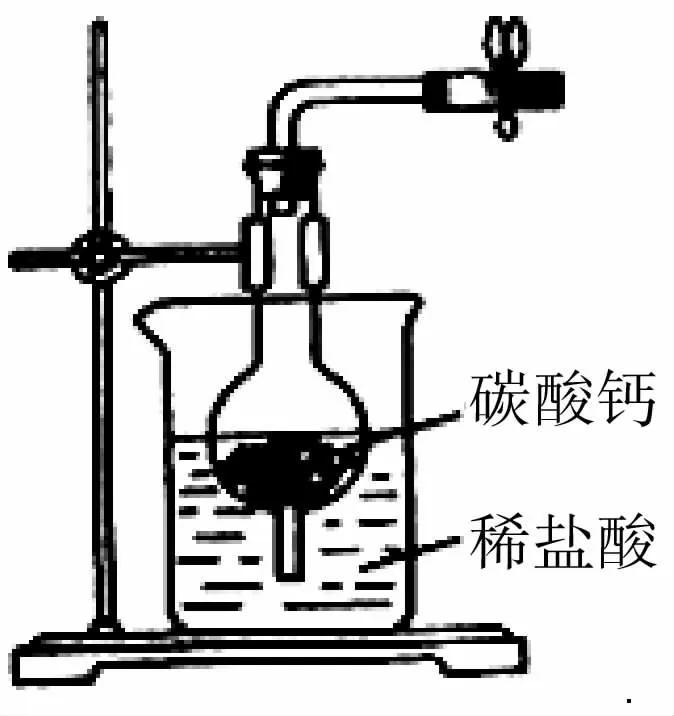
图3
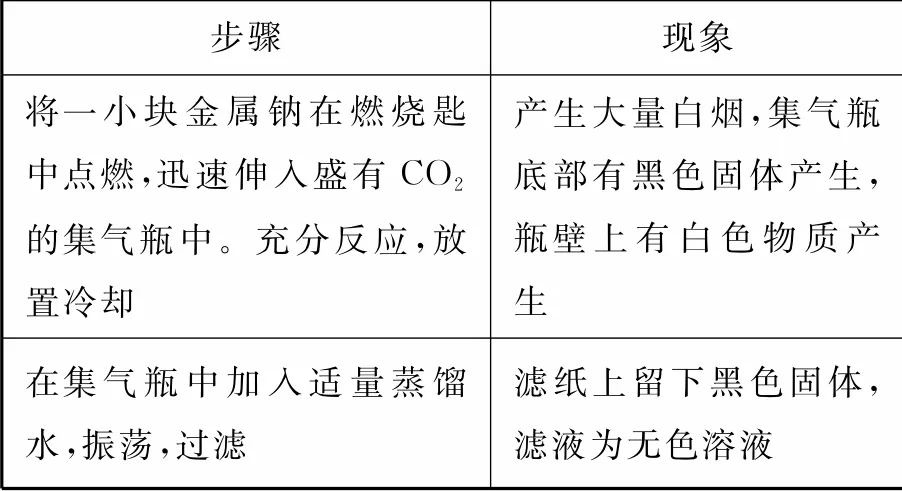
表2
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红;向第二支试管中滴加澄清石灰水,溶液变浑浊。据此推断,白色物质的主要成分是_____(填标号)。
A.Na2O B.Na2O2
C.NaOH D.Na2CO3
②为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是____。
③本实验中金属钠与二氧化碳反应的化学方程式为_____。
解析:(1)用碳酸钙与稀盐酸制备二氧化碳,因盐酸易挥发,需要用饱和NaHCO3溶液除去HCl,再通过浓硫酸干燥,则为了得到干燥纯净的CO2,产生的气流应依次通过盛有饱和NaHCO3溶液、浓硫酸的洗气瓶。反应结束后,关闭弹簧夹,利用气体的压强使固液分离,可观察到产生的气体使干燥管内液面降低,与碳酸钙脱离接触,反应停止。不能用稀硫酸代替稀盐酸,因生成硫酸钙微溶,包裹在碳酸钙的表面,阻止反应的进一步发生。(2)①取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红;向第二支试管中滴加澄清石灰水,溶液变浑浊,可知显碱性,且含碳酸根离子或碳酸氢根离子,显然只有Na2CO3符合。②检验黑色固体的成分,将其与浓硫酸反应,生成的具有刺激性气味的气体为二氧化硫,可知C与浓硫酸反应,即黑色固体是碳(C)。
答案:(1)饱和NaHCO3溶液、浓硫酸 产生的气体使干燥管内液面降低,与碳酸钙脱离接触,反应停止 生成的硫酸钙微溶,附着在碳酸钙表面,阻止反应进一步进行
点评:本题考查物质的制备及性质实验,为高频考点,把握物质的性质、实验装置的作用、实验现象与结论为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大。
三、实验题的强化练习
近几年的高考真题展示了高考题的命题方向,选取部分高考实验试题强化训练十分必要。
【练习一】实验室用图4所示装置制备KClO 溶液,并通过KClO 溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4。已知K2FeO4具有下列性质:
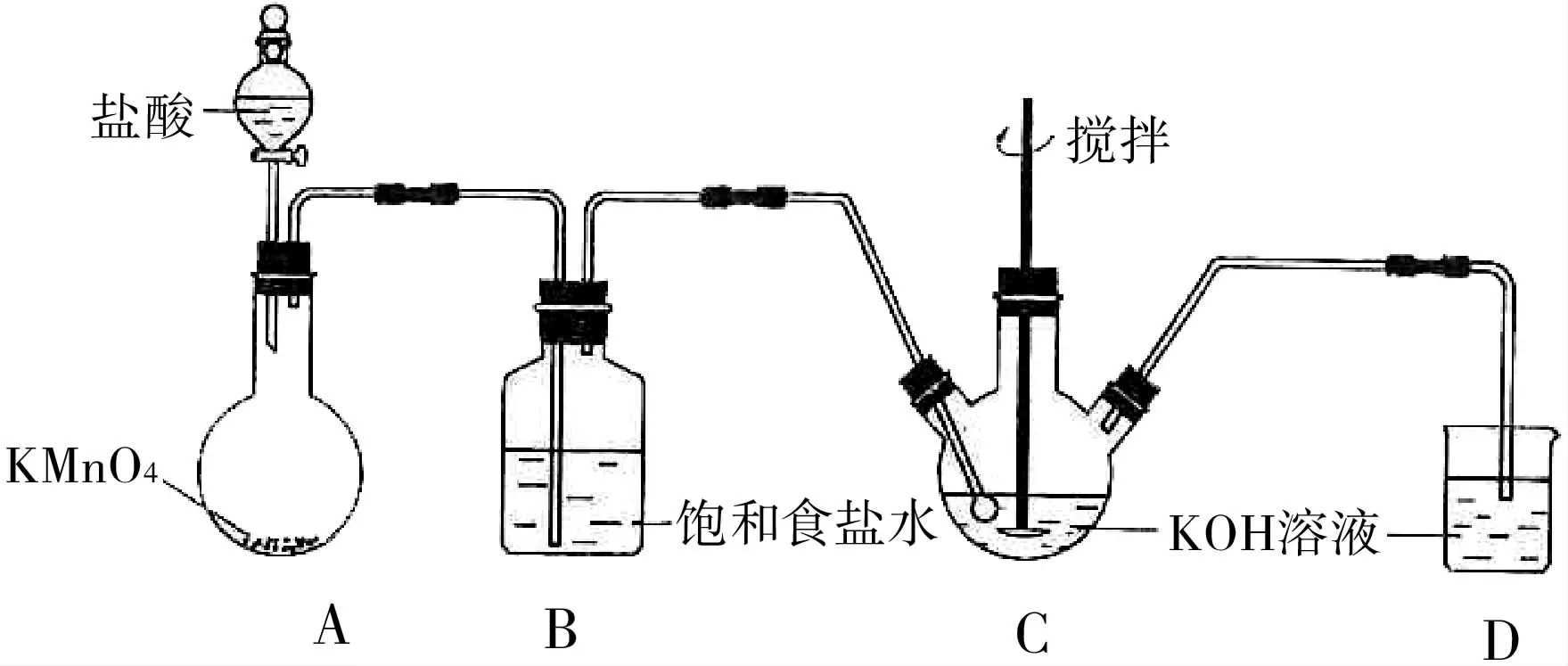
图4
①可溶于水,微溶于浓KOH 溶液;②在0~5 ℃、强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。
(1)装置A中KMnO4与盐酸反应生成MnCl2和Cl2,其离子方程式为____,将制备的Cl2通过装置B 可除去_____(填化学式)。
(2)Cl2和KOH 在较高温度下反应生成KClO3,在不改变KOH 溶液的浓度和体积的条件下,控制反应在0~5 ℃进行,实验中可采取的措施是____。
(3)制备K2FeO4时,KClO 饱和溶液与Fe(NO3)3饱和溶液的混合方式为_____。
(4)提纯K2FeO4粗产品[含有Fe(OH)3、KCl等杂质]的实验方案:将一定量的K2FeO4粗产品溶于冷的3 mol·L-1KOH溶液中,_____(实验中须使用的试剂:饱和KOH 溶液、乙醇;除常用仪器外须使用的仪器:砂芯漏斗、真空干燥箱)。
【练习二】草酸(乙二酸)存在于自然界的植物中,其中K1=5.4×10-2,K2=5.4×10-5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101 ℃,易溶于水,受热脱水、升华,170 ℃以上分解。回答下列问题。
(1)甲组同学按照如图5所示的装置,通过实验检验草酸晶体的分解产物。装置C中可观察到现象是_____,由此可知草酸晶体分解的产物中有____。装置B 的主要作用是____。

图5
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和如图6所示的部分装置(可以重复选用)进行实验。

图6
①乙组同学的实验装置中,依次连接的合理顺序为A、B、___。装置H 反应管中盛有的物质是____。
②能证明草酸晶体分解产物中有CO 的现象是____。
(3)设计实验证明。
①草酸的酸性比碳酸的强:_____。
②草酸为二元酸:____。
答案:【练习一】(1)2MnO-4+16H++10Cl══-2Mn2++5Cl2↑+8H2O HCl
(2)缓慢滴加盐酸,装置C加冰水浴
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO 饱和溶液中
(4)用砂芯漏斗过滤,将滤液置于冰水浴中,向滤滤中加入饱和KOH 溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥
【练习二】(1)有气泡产生,澄清石灰水变浑浊 CO2冷凝(水蒸气、草酸等),防止草酸进入C装置反应生成草酸钙沉淀,干扰二氧化碳的检验
(2)①F、D、G、H、D、I CuO(氧化铜) ②H 中的黑色粉末变红色,H 前的装置D 中的澄清石灰水不变浑浊,H 后的装置D 中的澄清石灰水变浑浊
(3)①向1mol·L-1NaHCO3溶液中加入1mol·L-1草酸溶液,若产生大量气泡,则说明草酸的酸性比碳酸的强
②用NaOH 标准溶液滴定草酸溶液,消耗NaOH 的物质的量为草酸的2倍,则说明草酸是二元酸

