紧扣热点物质 注重素养考查
江苏 徐 涵 陈仕功
温室效应和全球气候变暖一直是世界各国普遍关注的,减少二氧化碳的排放已是必然选择,科学家预测,如果现在开始有节制地对树木进行采伐,到2040年,全球暖化会降低5%。《普通高中化学课程标准(2017年版)》也要求学生具有节约资源、保护环境的可持续发展意识,从自身做起,形成简约适度、绿色低碳的生活方式。近几年的高考试题顺应这一趋势,围绕CO2多维考查的试题较多,体现了对学生科学态度和社会责任素养的考查与培养。
一、关注热点,增强社会责任
《京都议定书》是1997年12月在日本京都由联合国气候变化框架公约参加国三次会议制定的,其目标是“将大气中的温室气体含量稳定在一个适当的水平,进而防止剧烈的气候改变对人类造成伤害”。
【例1】(2018·江苏·1)CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
( )
A.光合作用 B.自然降雨
C.化石燃料的燃烧 D.碳酸盐的沉积
【答案】C

该类试题注重考查化学与环境保护、低碳经济等,树立绿水青山就是金山银山的理念,倡导可持续发展的理念。
二、绿色转化,贡献化学智慧
在改造了基因结构的微生物的帮助下,可将二氧化碳转化成可以作为汽车、内燃机燃料的异丁醇和异戊醇,使二氧化碳实现不可思议的“反向燃烧”和“闭合循环”,提高了二氧化碳高附加值的利用水平。
【例2】(2018·北京·7)我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下:
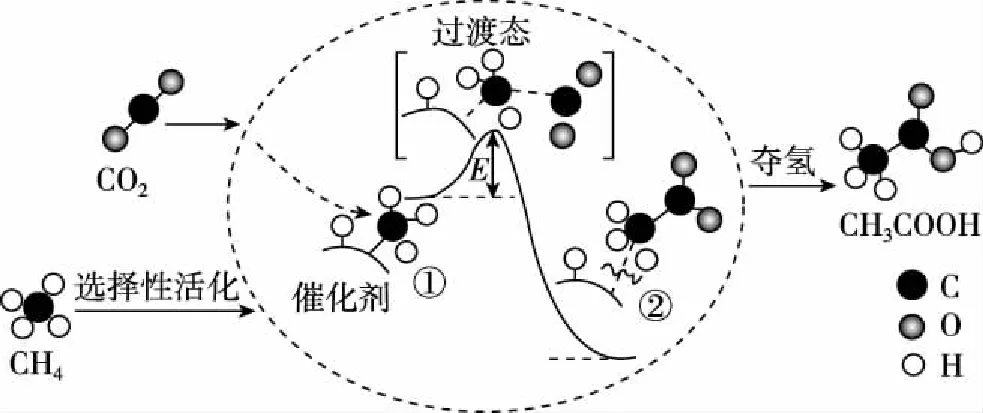
下列说法不正确的是
( )
A.生成CH3COOH总反应的原子利用率为100%
B.CH4→CH3COOH过程中,有C—H键发生断裂
C.①→②放出能量并形成了C—C键
D.该催化剂可有效提高反应物的平衡转化率
【答案】D

新型的CO2利用技术,即超临界CO2萃取技术(CO2-SFE),可生产高附加值的产品,且廉价、无毒、安全、高效。利用水热反应,在2.20×104kPa、374℃时,水成为“超临界状态”,将CO2转化为有机物,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。
三、变废为宝,提升创新意识
CO2的电化学转化可利用波谷电或可再生能源将CO2转化成高附加值的化学品或其他液态燃料,是一条能源存储及碳元素循环利用的绿色途径,对人类的可持续发展具有重要意义。
【例3】(2018·天津·10)CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:

(2)O2辅助的Al-CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。

电池的负极反应式:____________________。
反应过程中O2的作用是________。该电池的总反应式:________。

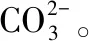

作为“碳捕获和利用”新技术,利用生物电化学系统还原二氧化碳生产甲烷和乙酸并利用阴极极化电势对微生物代谢产物进行调控的方法,对二氧化碳进行活化,合成出甲烷、甲醇、甲酸。富养罗尔斯通氏菌H16利用乙酰辅酶A,以二氧化碳作为原料或零件,将其拼装成含4个碳或5个碳的高能量有机化合物,形成如异丁醇、异戊醇等有机化合物。
四、节能减排,明晰平衡思想
甲烷和二氧化碳作为碳源,可以在一定条件下转化为合成气(CO和H2),即称之为甲烷-二氧化碳重整或者干重整。相比较传统的甲烷蒸气重整,甲烷-二氧化碳重整几乎不消耗水,而是大量利用二氧化碳,降低能耗的同时还缓解温室气体减排压力,受到世界的广泛关注。
【例4】(2018·全国卷Ⅱ·27)CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:



该催化重整反应的ΔH=________kJ·mol-1。有利于提高CH4平衡转化率的条件是________。
A.高温低压 B.低温高压
C.高温高压 D.低温低压
某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为________mol2·L-2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。
相关数据如表:

积碳反应CH4(g)C(s)+2H2(g)消碳反应CO2(g)+C(s)2CO(g)ΔH/(kJ·mol-1)75172活化能/(kJ·mol-1)催化剂X3391催化剂Y4372
①由上表判断,催化剂X________(填“优于”或“劣于”)Y,理由是________________。
在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是________(填标号)。

A.K积、K消均增加
B.v积减小,v消增加
C.K积减小,K消增加
D.v消增加的倍数比v积增加的倍数大
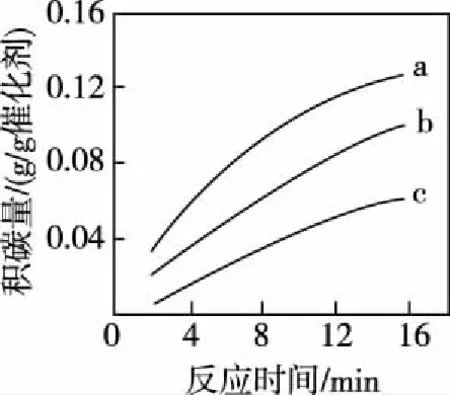
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为v=k·p(CH4)·[p(CO2)]-0.5(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为____________。



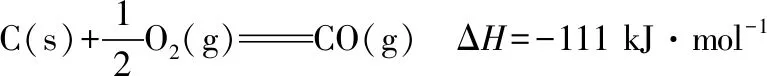


起始浓度(mol/L) 1 0.5 0 0
转化浓度(mol/L) 0.25 0.25 0.5 0.5
平衡浓度(mol/L) 0.75 0.25 0.5 0.5
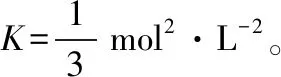
(2)①根据表中数据可知相对于催化剂X,催化剂Y积碳反应的活化能大,积碳反应的速率小;而消碳反应活化能相对小,消碳反应速率大,所以催化剂X劣于Y。
正反应均是吸热反应,升高温度平衡向正反应方向进行,因此K积、K消均增加,A正确;升高温度反应速率均增大,B错误;根据A中分析可知C错误;积碳量达到最大值以后再升高温度积碳量降低,这说明v消增加的倍数比v积增加的倍数大,D正确。
②根据反应速率方程式可知在p(CH4)一定时,生成速率随p(CO2)的升高而降低,所以根据图象可知pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为pc(CO2)>pb(CO2)>pa(CO2)。
甲烷超干重整指使用Ni、CaO/Al2O3和Fe3O4/MgAl2O4三种催化剂,利用氧化还原反应的过程将含氢物种(水)与含碳物种分离,拉动了平衡,提高了二氧化碳的转化率,得到了富一氧化碳的产物。
二氧化碳虽然是最主要的温室气体,但也是一种“碳源”,借助科技手段将其“变废为宝”,把二氧化碳转化为甲醇、甲酸等液体燃料,实现“人工碳循环”,不仅能缓解碳排放引发的温室效应,还将成为理想的能源补充形式,引领新一代能源革命。
——会偷偷侵蚀你的发动机!

