抓住“特殊节点”是破解问题的关键
甘肃 车 琳
新课改倡导培养学生的学科核心素养,高考将会有针对性地侧重考查。模型认知是化学学科重要的核心素养,建模思想突出体现了化学学科的思想与方法。化学从量的角度演绎着化学的具体与抽象,尤其是数形结合,会使化学由抽象到具体,辅助数学模型的构建是认识化学学科的重要工具。因此,着力考查“核心素养”落实的高考,图象题和体现定量化研究的试题,新高考将会占一定的比例。笔者发现“特殊节点”问题常常会造成矛盾的突变,问题的转折,使认知发生冲突;所谓“特殊节点”即曲线和曲线的交点,或是曲线的转折点,或是量的积累引发反应的突变点,或是平衡的建立与平衡移动的转折点。对“特殊节点”问题进行梳理和总结,能帮助学生破解难点问题,有助于提高做题的效率,或会峰回路转,柳暗花明,步入解决问题的坦途(转入解决问题的捷径),对于提高答题能力和解决问题的精准性大有裨益。
一、有效判断终点的到达
【例1】(2014·安徽·11)室温下,向0.2 mol·L-1Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1NaOH溶液,实验测得溶液的pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是
( )


B.a~b段,溶液pH增大,Al3+浓度不变
C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
【答案】C

二、分步反应的转折
【例2】25℃时,在向10 mL浓度为0.1 mol·L-1的NaOH和等体积等浓度的NH3·H2O组成的混合溶液中滴加0.1 mol·L-1盐酸,下列有关溶液中粒子浓度关系正确的是
( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH3·H2O)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
【答案】B

三、先拐先平(或条件改变、平衡移动)
【例3】(2018·河南洛阳质检)下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图象,其中图象和实验结论表达均正确的是
( )
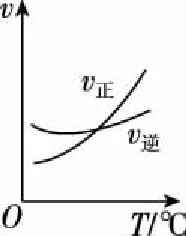
①

②

③

④
A.①是其他条件一定时,反应速率随温度变化的图象,正反应ΔH<0
B.②是在平衡体系的溶液中加入少量KCl晶体后化学反应速率随时间变化的图象
C.③是在有无催化剂存在下建立的平衡过程图象,a是使用催化剂时的曲线
D.④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强:p1>p2
【答案】C

四、反应过程中瞬间等量的呈现


下列叙述错误的是
( )
A.pH=1.2时,c(H2A)=c(HA-)
B.lg[K2(H2A)]=-4.2
C.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
【答案】D

五、平衡曲线,特殊环境的呈现
【例5】(2013·大纲卷·12)下图表示水中c(H+)和c(OH-)的关系,下列判断错误的是
( )

A.两条曲线间任意点均有c(H+)·c(OH-)=Kw
B.M区域内任意点均有c(H+) C.图中T1 D.XZ线上任意点均有pH=7 【答案】D 【解析】T1、T2两条曲线为不同温度下水的电离平衡曲线(Kw即为温度的状态函数),根据水的离子积定义可知,A项正确;X、Z两点可视为“特殊节点”,且氢离子浓度和氢氧根离子浓度相等,故XZ线上任意点都存在c(H+)=c(OH-),M区域内任意点均有c(H+) 【例6】(2017·全国卷Ⅰ·13)常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是 ( ) A.Ka2(H2X)的数量级为10-6 C.NaHX溶液中c(H+)>c(OH-) D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+) 【答案】D 综上所述,“特殊节点”是图象问题或与量有关的竞争反应问题的突变标志。因此,抓住其“特殊节点”往往会找到解决问题的突破口,“特殊节点”在可逆反应中往往是达平衡的标志,或条件改变造成平衡移动的源点,或是竞争反应的结局或起点,或是有关反应终点的到达。找到关键的“特殊节点”,往往会使问题简化,问题得到破解,从复杂中迂回,或见天开,成为我们建构认知的基点,思考解决问题的源泉。因此,总结“特殊节点”对于快速解决问题、理清思路,化繁为简,提高认知能力具有很重要的价值。六、特殊“点”体现量的关系