例析整体思维在高考化学复习中的巧妙渗透
安徽 葛胜文
整体思维是一种策略思维,具有思维的广阔性和综合性特征,其核心是把问题作为一个整体来看,从问题的全局出发,整体驾驭信息,分析构成问题的各要素与整体之间的关系,以及在整体中的作用,在整体变化中寻找不变的量,对有关的信息进行变形、替代、转化等技术处理,拓展思维空间,直接架设问题与结论之间的桥梁,将问题整合到一起,化繁为简,简化解题过程,巧妙解题。高中学生若能通过训练较好地掌握整体思维的解题方法,就能迅速解题,达到事半功倍的解题效果。
一、挖掘隐藏信息,整合电子守恒
一种缺条件类型的试题,对逻辑思想的考查层次更高,要求挖掘出试题中隐藏的条件,电子守恒是氧化还原反应的本质,属于隐藏很深的一个条件,通过细心审题才能挖掘出来,然后通过整合电子守恒,列出关系式,巧妙求解。
【典例1】将1.92 g Cu投入到一定量的浓HNO3中,Cu完全溶解,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,若这些气体完全被水吸收,则需要通入O2(标准状况下)的体积为
( )
A.33.6 mL B.168 mL
C.336 mL D.672 mL

【答案】C
【点评】按常规方法解题,本题属于缺条件试题,无法解答,必须挖掘出题干中的隐藏条件,从氧化还原反应视角,追踪浓硝酸中N的化合价变化,抛开反应细节,把氧化剂和还原剂得失电子数相等作为整体考虑,方可化繁为简,巧妙解答。
二、走出陷阱,整合质量守恒
巧妙应用质量守恒,也能达到出奇制胜的解题效果。从沉淀与滤液的质量守恒、固体与气体的质量守恒、固体与固体的质量守恒等,依据质量守恒,列出解题关系式,巧妙切入,迅速解题。
【典例2】200℃时,11.6 g CO2和H2O的混合气体与足量的Na2O2充分反应后,固体增重3.6 g,则原混合气体的平均相对分子质量是
( )
A.5.8 B.21.6
C.23.2 D.46.4

于是,可得关系式:
CO2和H2O的混合气体 ~ O2
2 mol 32 g
n(混) mol (11.6-3.6) g
2∶32=n(混)∶(11.6-3.6),解得n(混)=0.5。
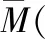
【答案】C
【点评】走出“固体增重3.6 g”的思维陷阱,立足题干信息,从整体反应考虑,抓住质量守恒,从固体质量入手,突破气体质量变化,求出生成O2质量为m(O2)=11.6 g-3.6 g=8 g,从而巧妙突出重围,求出n(混)=0.5 mol。
三、以不变应万变,整合定量关系
忽略反应细节,通过关系式的定量关系,紧抓不变量,找到解题的突破口,轻松审题。
【典例3】标准状况下H2和Cl2的混合气体aL,经光照充分反应后,所得气体恰好使溶液中bmol NaOH完全转变为盐,a与b的关系不可能是
( )


于是,可得关系式: Cl2~ 2NaOH
22.4 L 2 mol
V(Cl2) Lbmol
22.4∶2=V(Cl2)∶bmol,解得V(Cl2)=11.2b。


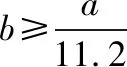
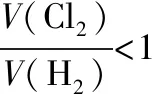
【答案】A
【点评】在多重复杂关系中,分析比较,整合氯气与NaOH的定量关系,Cl2~2NaOH,从整体出发,抓住不变量V(Cl2)=11.2b解题,可以简化思维,化繁为简,使问题迎刃而解。
四、抛开反应过程,整合原子守恒
不纠结化学过程的细枝末节,纵观全局,从整体上分析题意,抓住不变量——原子守恒,挖掘试题切入点,迅速审题,简化解题过程。
【典例4】向一定量Fe、Fe2O3的混合物中加入250 mL 2 mol·L-1的HNO3溶液,反应完成后生成1.12 L NO(标准状况),再向反应后溶液中加入1 mol·L-1NaOH溶液,要使铁元素完全沉淀下来,所加入NaOH溶液的体积最少是
( )
A.400 mL
B.450 mL
C.500 ml
D.不能确定
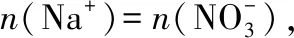
【答案】B



