奥美沙坦酯片的合成工艺研究
赵振鑫,龚娅琼
(1.福建天泉药业股份有限公司,福建龙岩 364000;2.云南沃森生物技术股份有限公司,云南昆明 650000)
作为临床常用的降压药物,奥美沙坦酯片在降压效果、安全性方面具有明显优势[1]。随着这种血管紧张素Ⅱ1型受体(AT1)拮抗剂效果的证实,奥美沙坦酯片的合成工艺逐渐引起了人们的广泛关注[2]。因此,分析奥美沙坦酯片的合成工艺具有一定的必要性。
1 材料与方法
1.1 试剂与仪器
试剂:乙醇、盐酸、无水乙醚、四氢呋喃,均为化学纯;碘甲烷(浓度≥99%);原丁酸三甲酯(浓度≥99%);N,N-二甲基甲酰胺(DMF);2,3-二氨基顺丁烯二腈等。
仪器:HHS2I-8型号恒温水浴锅、FA1204B型号电子分析天平、LC-10A型号液相色谱仪、BDW1-202-0ASB型号恒温干燥箱等。
1.2 方法
(1)制备格氏试剂。以乙醚无水处理碎片状镁条:于N2条件下,向反应瓶内加入镁条及30 mL乙醚,充分混匀后,将混合溶液(无水乙醚120 mL、碘甲烷20 mL)加入反应瓶内,将反应过程温度参数控制于60 ℃以下(控制方法采用滴加方法)。反应开始的标志为:加入溶液时可见反应瓶内变浑浊。格氏试剂制备完成标志:反应液转为黑色。
(2)合成2-丙基咪唑-4,5-二腈。取48 g原丁酸三甲酯、32 g 2,3-二氨基顺丁烯二腈,混于50 g DMF溶液中。充分混匀后,将混合溶液加热至100 ℃,充分反应(反应时长为10 h)。反应结束时,以减压浓缩法处理DMF,获得黑色油状产物。
(3)合成2-丙基咪唑-4,5-二羧酸。于320 mL HCl溶液(6N)混入上批全量。于低温条件下静置处理,直至溶液中析出结晶为止。经过滤、干燥处理后,获得45.3 g产物。经液相色谱仪检测产物含量为98.1%。熔点及两步总回收率参数分别为263~264 ℃、76.2%。
(4)合成2-丙基咪唑4,5-二羧酸二乙酯。与100 g无水乙醇中混入10 g 2-丙基咪唑4,5-二羟酸。向混合溶液中加入10滴浓硫酸溶液。冷却处理至10 ℃,向混合溶液中加入10 g二氯亚砜。于室温条件下持续反应2 h。按照1∶2比例(甲醇∶氯仿)进行TLC检测。反应后,将混合液pH值调至7(调节方法为碳酸氢钠溶液),去除多余乙醇。提取乙酸乙酯,正己烷及硫酸镁分别进行结晶、干燥处理。过滤结晶,获得11.9 g产物,经检测:含量为97.6%。熔点及回收率参数分别为82~84 ℃、92.3%。
(5)合成4-2-丙基咪唑-5-羧酸乙酯。于50 mL二氯甲烷中混入15 g 2-丙基咪唑-4,5-二羧酸二乙酯,于-10 ℃温度条件下,混入适量格氏试剂,搅拌后,于2 ℃条件下充分反应(反应时间以1.5 h为宜)。按1∶6比例(甲醇:氯仿)进行TLC检测。反应后,混入100 g氯化铵溶液及120 g乙酸乙酯,提取有机层后,经干燥、蒸发、结晶处理后,获得12.8 g淡黄色晶体,检测含量为96.0%,回收率为90.2%。
(6)合成4-2-丙基-1-甲基咪唑-5-羧酸乙酯。于500 mL三颈瓶内加入55.7 g 4-苯甲基溴、24.0 g 4-2-丙基咪唑-5-羧酸乙酯、41.1 g碳酸钾等,搅拌均匀后,以恒温水浴锅加热至60℃。持续反应5h后,按1∶1比例(正已烷∶乙酸乙酯)进行检测。经两次提取分液、洗涤、浓缩、析出、过滤、烘干处理后,获得67.5 g产物,检测含量为98.5%,回收率为94.3%。
(7)反应物合成。按照规范流程分别合成4-2-丙基-1-甲基咪唑-5-羧酸乙酯、4-2-丙基-1-甲基咪唑-5-羧酸甲基酯。二者含量检测结果分别为98.2%、99.5%。合成流程化学式如图1。
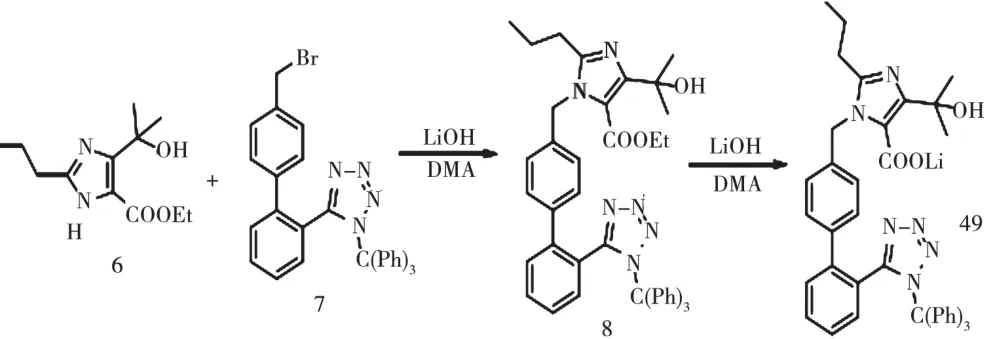
图1 合成流程
(8)合成奥美沙坦酯。于1 000 mL三颈瓶中混入80 g最后一步骤中获取化合物、448 g二氯甲烷,混匀后,缓慢加入243.2 g甲醇。于5 ℃条件下,向混合物中混入262.4 g 10%浓度盐酸甲醇。持续反应1 h。按1∶3比例(正己烷∶乙酸乙酯)进行检测。经过调pH、提取、干燥、脱色、浓缩、结晶、过滤、干燥处理后,获得50.4 g粗品奥美沙坦酯,含量水平为99.1%。对粗品进行重结晶处理,获得含量为99.7%的精品奥美沙坦酯。
2 结果
2.1 元素分析
产物各元素质量分数见表1。
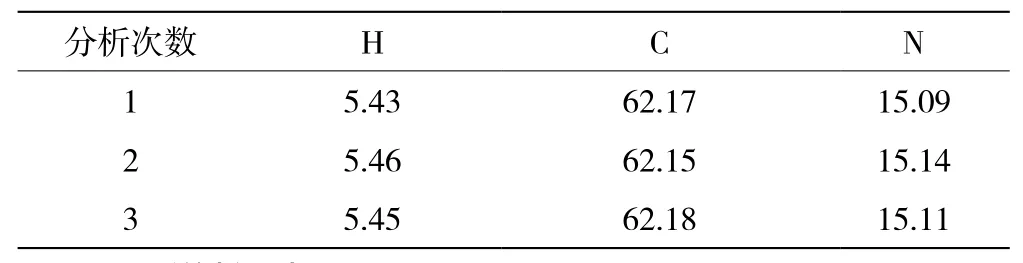
表1 产物各元素质量分数(%)
2.2 质谱检测
质谱检测结果见表2。

表2 质谱检测
2.3 HNMR图谱
见表3。
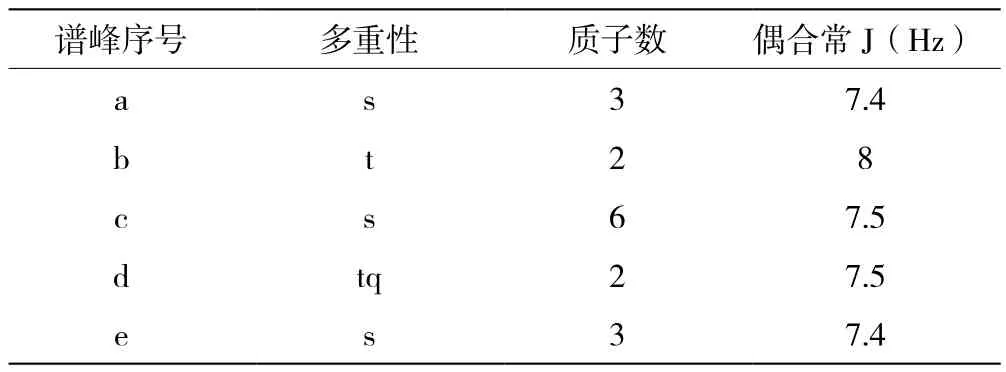
表3 HNMR图谱
3 讨论
奥美沙坦酯片治疗高血压的药理机制为:经口服给药后,由胃肠道进行吸收、水解,生成奥美沙坦产物,这一产物可对血管平滑肌AT1受体与血管紧张素Ⅱ之间的结合反应产生抑制作用,进而干扰血管紧张素Ⅱ经收缩血管这一机制造成患者血压升高[3]。随着奥美沙坦酯药效的发挥,高血压患者的降压效果可逐渐呈现出来。
奥美沙坦酯作为一种化合物,其合成工艺直接决定这种化合物的生产成本及生产效率[4]。近年来,随着高血压发病率的不断升高,生产企业对奥美沙坦酯片合成工艺的要求也随之变化。在这一背景中,奥美沙坦酯合成工艺所暴露出的问题也变得越来越明显。为了改善奥美沙坦酯的合成效果,需注重合成工艺的优化与改进。
本研究在奥美沙坦酯合成工艺基础上,针对各个工艺环节中所使用的溶剂、操作方法等进行优化,其目的为:提高产物纯度,缩短生产耗时,并改善产物质量。
相对于原有奥美沙坦酯合成工艺而言,本研究所选用合成工艺的优势主要体现在以下3方面。(1)以二氯亚砜替代少量浓硫酸。2-丙基咪唑-4,5-二羧酸二乙酯合成工艺无疑是奥美沙坦酯合成中的关键环节。原有合成工艺中,原料中含较多浓硫酸,溶剂采用乙醇,原料溶解环节的耗时在20 h左右。为了实现便捷化合成奥美沙坦酯的目的,同时缩短工艺耗时,本研究将这一工艺改进为:引入二氯亚砜原料,并将浓硫酸用量控制为10滴水平。经改进处理后,在这一环节中,所有原料充分反应所需时间降至2 h左右,而该工艺成本也下降约31.0%。(2)以碳酸钾干燥,并以乙醚进行结晶。干燥、结晶是合成4-2-丙基-1-甲基咪唑-5-羧酸乙酯工艺中的两个关键步骤[5]。在化学合成过程中,原有工艺选用叔丁醇为干燥剂。而本研究工艺流程则采用碳酸钾进行替代,这种工艺设计方法的优势为:这种干燥剂成本较低,且不易受环境因素(储存环境温度、湿度等)影响,将其用于奥美沙坦酯片合成,可在保障合成任务完成的基础上,充分发挥良好的控制成本作用。此外,本研究还将这一工艺中的结晶物质替换为乙醚,从结晶效果来看,所得产物的纯度较原有工艺上升3.9%左右,这一数据充分证实了乙醚在结晶环节中的应用价值。(3)以盐酸甲醇替代乙醇水溶液。奥美沙坦酯合成过程中,酯键水解环节的重要性不言而喻。这一工艺流程的难度在于酯键水解反应具有可逆性特征,如原料及反应温度控制不当,可能引发逆向反应,导致反应时间延长,甚至影响最终的奥美沙坦酯合成效果[6]。原工艺中选用乙酸水溶液为原料,而本研究工艺则以盐酸甲醇进行替代。这种工艺改进方法的优势在于:盐酸甲醇反应过程中无水的参与,避免了酯键水解反应的发生。此外,盐酸甲醇这种原料的溶解效果良好,将其用于奥美沙坦酯合成,可节约该环节的溶剂成本,使该工艺更加符合在工业生产中推广的要求。
采用本工艺合成奥美沙坦酯片,其优势较为明显,这种合成工艺可提高奥美沙坦酯片的回收率,整个合成操作较为简单,易于实施,且耗时较短,成本较少。上述优势充分满足其在工业合成奥美沙坦酯片中推广的要求。
综上所述,采用脱醇、闭环、水解、酯化系列工艺合成奥美沙坦酯,效果良好,这种合成工艺适用于奥美沙坦酯片的工业化生产。

