基于国家药品抽验工作的中成药质量和安全问题分析△
刘静,王翀,冯磊,朱炯,戴忠,马双成
中国食品药品检定研究院,北京 100050
中成药是以中药饮片为原料,在中医药理论指导下,为了预防及治疗疾病的需要,按规定的处方和制剂工艺将其加工制成一定剂型的中药制品,是经国家药品监督管理部门批准的商品化的中药制剂。中成药作为中医药的重要组成部分,其质量直接关系到临床用药的安全性与有效性。
药品抽验是对上市后药品质量总体水平和状态的全面考察,能为药品的质量监管提供科学依据[1-2]。药品抽验通过法定标准检验与探索性研究两部分工作的开展来对药品质量进行研究与评价,其中探索性研究是以问题为导向,以排查质量风险为目标,具体涉及药品安全性、真实性、有效性和均一性等方面的研究,有利于全面分析与评价药品质量,发现可能影响药品质量与安全的因素及隐患,为进一步强化对上市后药品质量的监管、不断提高上市后药品安全有效和质量水平的可控、保障公众的用药安全提供有力的技术支撑。笔者以2017—2018年全国中成药品种国家抽验数据为基础,结合具体品种实例对发现的主要质量安全问题进行汇总并提出有关建议,以更好地保障人民用药的安全与有效。
1 国家药品抽验中成药基本情况
2017—2018年,国家药品抽验中成药品种分别为40、42个,与历年品种数相当(见图1);全国31个省、自治区、直辖市分别抽取9787、9037批次样品,较往年提高近1倍(见图1)。抽样环节均以经营单位为主,此外还涉及生产单位和医疗机构抽样。剂型以口服制剂为主,涉及片剂、丸剂、颗粒剂、胶囊剂、口服液等,以及外用制剂、膏剂等多种传统剂型与新剂型。检验依据涉及《中华人民共和国药典》(《中国药典》)、卫生部部颁标准、国家药品监督管理局局颁标准、国家药品监督管理局补充检验方法等。
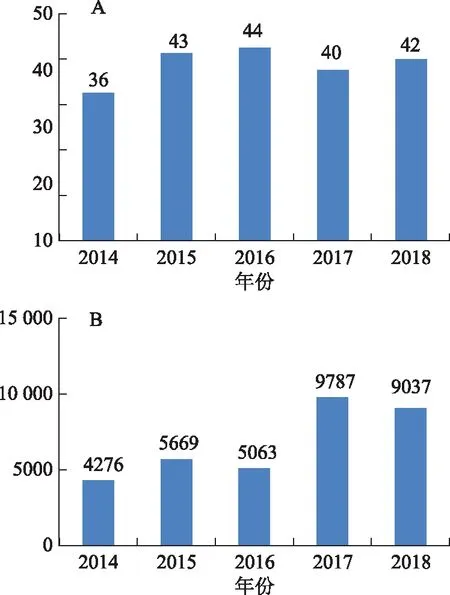
注:A.抽验品种数;B.抽样批数。图1 2014—2018年国家药品抽验中成药品种基本信息
2 质量安全情况评价
从法定标准检验的结果来看,2017—2018年国家药品抽检中成药品种的合格率高达96%~100%,表明质量状况良好,但进一步深入的探索性研究所揭示的问题表明总体质量一般。这是由于标准检验结果可以在一定程度上反映药品的质量,但由于中成药处方的复杂性,现行标准难以全面评价药品质量并发现潜在的质量问题。因此,在国家药品抽验工作中,除法定标准检验外,各承检单位还需要以原料药和制剂的质量问题为导向,围绕药品的安全性、真实性、有效性和均一性等方面开展进一步深入的探索性研究,从而更为全面、有效地评价中成药产品质量。
3 主要问题分析
中成药生产主要涉及原料药、辅料、生产工艺及包装等环节,各环节相关因素都会影响到中成药的质量。通过对2017—2018年全国中成药国家抽验品种探索性研究的结果进行梳理归纳,发现原料药质量和生产工艺是影响中成药质量的主要问题。
3.1 原料药质量问题
原料药是中成药生产的基础物质,其质量状况将会直接影响药品质量,尤其是中药材来源复杂,采收季节、产地、贮藏、炮制等都会直接影响药品的质量及其安全性和有效性[3-5]。近年来,在中成药品种的国家药品抽验工作中,也对不少品种从生产企业收集的原料药进行了质量考察,发现主要问题有掺伪、染色、非药用部位使用、外源性有毒有害物质残留等。
3.1.1 掺伪 由于资源短缺或因价格原因,近年来多基原品种掺伪混用的现象时有发生。例如《中国药典》2015年版一部规定柴胡来源于伞形科植物“北柴胡”或“南柴胡”,但本品用药较混乱,基原不清,常有掺伪问题。广东省药品检验所在对小柴胡颗粒处方中君药柴胡的探索性研究过程中,调研发现市场流通量较大的是藏柴胡;为明确是否存在藏柴胡掺伪的问题,通过寻找、确认藏柴胡特征成分柴胡皂苷K,建立液质联用检测方法,基于样品检验结果,建立了相关的补充检验方法,以打击藏柴胡掺伪的违规行为。
《中国药典》2015年版一部收载的贝母类药材有川贝母、平贝母、浙贝母、湖北贝母、伊贝母等,其中川贝母按性状不同又分为野生松贝、青贝、炉贝和栽培品。贝母类药材鉴定是公认的难题,加之目前川贝母与其他贝母价格差异悬殊,因此较常发现掺伪现象[6-9]。河北省药品检验研究院对川贝枇杷制剂研究了基于代谢组学分析技术的不同川贝母差异性,并建立了基于化学计量学的生物碱类成分特征图谱以及基于对照制剂的生物碱类成分含量分析,依据综合检测结果明确了部分样品中存在川贝母掺伪或投料不足的问题。
针对山银花代替或掺伪金银花投料生产的问题,在小儿咳喘灵制剂、金银花系列制剂研究过程中,以山银花所含灰毡毛忍冬皂苷乙、川续断皂苷乙等皂苷类成分为指标,建立了相应的高效液相色谱或液质联用分析方法,发现有企业样品存在金银花混杂山银花投料的问题。
人参归脾丸处方中含有人参,研究过程中发现有异常样品并确定异常成分为拟人参皂苷F11,进一步采用高效液相色谱-蒸发光散射检测器法(HPLC-ELSD)同时建立了人参专属性成分人参皂苷Rf的鉴别方法和西洋参专属性成分拟人参皂苷F11的检查方法,结果有企业样品检出拟人参皂苷F11,存在西洋参替代人参投料的现象。
树脂类药材的松香掺伪危害严重,主要是因为松香中所含松香酸具有一定毒性,目前发现的涉及松香掺伪的药材主要有乳香、没药、血竭、沉香等树脂类药材,并相继建立了有关中成药品种中松香酸检查项补充检验方法[10-11]。随着这些补充检验方法的颁布和实施,可以看到2017—2018年中成药品种松香掺伪的问题得到有效控制。
目前市场上驴皮供应紧张,价格高涨,因而有部分企业存在以牛皮、马皮投料生产阿胶的情况。山东省食品药品检验研究院建立了女金丸中阿胶驴皮特征肽定性鉴别方法、牛皮源成分和马皮源成分的补充检验方法,为打击阿胶掺伪或替代投料的问题提供了有力的科学依据。
3.1.2 染色 近年来染色原料药进入生产环节导致中成药检出染料的现象仍有发生。由于这些中药染料种类繁多,结构复杂,不断变化,且多为有害化工染料,对人体健康存在严重安全隐患。因此,国家药品监管部门相继批准了一系列补充检验方法作为这些问题药品认定的技术依据[12-13]。此外,目前中药染色的检测技术方法研究较为深入,涵盖经典的薄层色谱方法和现代的高效液相色谱及液质联用技术[14-16],为准确定性染料种类以及相应补充检验方法的建立提供了科学依据与参考。
2017—2018年国家药品抽验中的个别中成药品种中检出染料,主要涉及金胺O、胭脂红、柠檬黄、日落黄、亮蓝、苋菜红和酸性红73。随着近年来国家药监部门对染色问题的监管与重视,检出情况整体较往年明显改善。
3.1.3 非药用部位使用问题 柴胡用药较混乱,基原不清,也常有非药用部位混用的问题。银柴制剂探索性研究过程中,通过薄层色谱法发现有企业提供的个别批次柴胡中混有地上部分。
此外,近年来处方中含有贵细药材的个别品种有发现非药用部位使用的现象。以骨刺片为例,由于其处方中含有贵细药三七,因三七茎叶资源丰富、价格便宜,鉴于往年国家药品抽验工作中曾发现存在以三七茎叶代替或部分代替三七投料的问题,因此重点对原料药三七的真实性进行了探索性研究,结果显示实验样品批次中均未检出三七茎叶特有成分人参皂苷Rb3,表明这些样品不存在三七茎叶非药用部位使用的问题。
3.1.4 外源性有毒有害物质残留问题 外源性有毒有害物质残留通常涉及重金属及有害元素、真菌毒素、农药残留、二氧化硫残留等。目前,尽管中成药国家药品标准中尚无有害物质残留的限量标准,但考虑到这些有害物质残留与药品安全性密切相关,因此近年来国家药品抽验中成药品种基本都开展了此项研究,结果一般参考中药材的限量标准或药用植物及制剂绿色行业标准作为判断标准。
3.1.4.1 重金属及有害元素 以牛黄清胃丸为例,检测样品中铅、砷、汞超标率分别为12%、12%、14%,个别样品严重超出拟定限度[17]。小儿咳喘制剂中发现铬、镍超标。综合2017—2018年国家药品抽验中成药品种重金属及有害元素的检测结果来看,主要涉及铅、砷、汞超标,存在一定风险,提示中成药中重金属及有害元素超标问题不容忽视,应进一步加强控制。
3.1.4.2 真菌毒素类 目前真菌毒素的检测以黄曲霉毒素为主。2017—2018年国家药品抽验中的个别中成药品种,如开胸顺气丸、启脾制剂的个别批次黄曲霉毒素超限,总体情况表明黄曲霉毒素残留的风险控制效果良好,有个别品种检出赭曲霉素A。此外,对于处方中含有陈皮、酸枣仁、土鳖虫等易污染黄曲霉毒素的药材及制剂应持续关注真菌毒素问题。
3.1.4.3 农药残留 2017—2018年国家药品抽验中的个别中成药品种,如加味逍遥丸、通窍鼻炎片的个别批次检出有机氯农药残留超限,表明中成药中农药残留总体情况较好,但对于易受病虫害侵扰的中药材或全粉入药制成的中成药应注意农药残留检测。
3.1.4.4 辐照残留 2017—2018年中成药品种国家抽验结果显示,仅个别品种如加味逍遥丸、女金丸、炎立消制剂等存在不同程度的辐照灭菌处理,辐照灭菌对制剂安全性、有效性的影响尚待进一步研究。
3.2 辅料问题
随着药品抽验工作的开展,辅料的问题已引起重视与关注。近年的药品抽验结果显示辅料方面的问题主要涉及蜂蜜和防腐剂,应予以关注、考察并规范。其中,在考察人参养荣制剂辅料炼蜜时发现,不同炼制工艺会导致5-羟甲基糠醛含量差异大,水蜜丸制丸中的烘干过程会致其含量升高,表明工艺不统一的问题有待规范。在对石淋通制剂辅料蔗糖研究时发现有企业投料食用白砂糖。此外,在对五味子系列制剂、银翘解毒合剂、川贝枇杷制剂等6个品种防腐剂检测时发现,主要有非法添加防腐剂、实际使用防腐剂种类与说明书不符以及超量使用防腐剂3种问题。
3.3 生产工艺存在的问题
3.3.1 未按处方投料的问题 在考察黄芩投料情况时,利用黄芩饮片与提取物中黄芩苷含量的差异,建立了小柴胡颗粒中黄芩提取物的液相色谱-紫外检查方法,采用汉黄芩苷与黄芩苷峰面积的比值限度,可明确黄芩投料是否按法定工艺生产,结果发现个别企业采用提取物代替饮片投料。
通便灵胶囊经薄层色谱法筛查,并经显微鉴别确证有企业样品检出番泻叶显微特征,表明存在原料未经提取直接添加番泻叶粉末投料的情况。
对于处方含有贵细中药如人参、牛黄等的品种而言,由于原料价格昂贵、资源短缺,可能会导致出现不投料或少投料的现象。例如人参养荣丸/膏,通过利用液质联用技术测定人参皂苷Rg1、Re、Rb1的含量,结果发现部分企业所用人参原料质量差或存在投料不足的情况。
此外,中成药品种以多药味处方为主,而执行标准难以全面控制各处方药味投料情况。往年药品抽验工作中发现对于执行标准中未规定鉴别项的部分中药存在未投料现象,未规定含量测定项的部分中药存在少投料现象,因此需要通过深入的探索性研究才能全面反映这些中成药品种的真实质量。以骨刺片为例,研究人员采用经典的薄层色谱法建立了处方中桂枝、威灵仙、延胡索和骨碎补4味中药的鉴别方法,检测结果表明部分企业在这4味中药的投料方面存在问题,不排除其对现行标准尚未规定检测项目的中药未严格按照处方量投料的可能[18]。鉴于骨刺片多药味、多成分的特点,研究还采用液质联用技术建立了同时测定15种成分含量的方法,检测结果进一步验证了薄层色谱法所反映的问题。
3.3.2 交叉污染的问题 有企业的启脾制剂样品中检出非处方成分黄芩苷,表明企业生产线存在交叉污染的情况。
3.3.3 改变工艺的问题 有企业的启脾制剂样品检出苯酚与对羟基苯甲酸乙酯,表明企业擅自改变工艺,违规添加上述抗氧化剂与抑菌剂。
3.4 包装问题
近年来,随着药品抽验工作的开展,包装材料对制剂质量的影响已引起重视与关注。有品种考察发现不同包装材料对同一品种、同一包装材料对不同品种的影响不同,特别是挥发性成分含量高、易潮解或含对水、热、光等不稳定的品种,应重视包装材料对药品质量影响的研究。以开胸顺气丸为例,有1批样品水分测定结果超限,经调研该企业原先所用包装材料为双向拉伸聚丙烯/双向拉伸聚丙烯珠光膜,阻隔性差易造成药品吸潮导致水分超标,反馈现已将包装材料改为聚酯/铝/聚乙烯药用复合膜,增加了包装材料气密性,有利于药品的储运。
4 有关建议
4.1 源头控制
原料药、辅料是中成药产品生产的基础物质,特别是中药饮片原料非常复杂,其质量状况将会直接影响药品的质量及其安全性和有效性。因此,建议加强源头控制,只有从生产源头的基础物质抓起,严格把关,才能更好地保证合格、优质的原辅料应用于中成药生产。
4.2 过程控制
中成药的质量与其生产工艺密切相关。质量是疗效的保证,也是工艺的体现。目前,中成药仍以粗提取制剂为主,工艺水平相对较低,生产过程控制对保障药品质量至关重要。
国家药品抽验工作要求以发现问题为导向,以排查质量风险为目标,检验中发现的问题线索在防控中成药质量风险中发挥了重要作用,提供了有力的技术支持。药品质量是生产出来的,不是检验出来的。因此,药品质量必须在生产过程中控制,把质量不合格的因素和引起质量不一致的因素处理在生产过程中,控制原料、辅料、包装材料及工艺条件,对每一个环节进行严格的质量控制,以保证药品质量,保证人民用药安全与有效。

