应用自动消融标注软件分析环肺静脉消融损伤指标的差异
黄波 王禹川 李康 贺鹏康 陈尔冬 夏驭龙 蒋捷 盛琴慧 周菁 丁燕生
射频消融在心房颤动(房颤)治疗中扮演着重要角色。在众多射频消融策略中,通过环肺静脉消融、隔离肺静脉电位是确保消融手术成功的关键因素[1]。然而现有研究表明,环肺静脉消融的长期肺静脉电隔离率并不令人满意并成为房颤复发的重要因素之一[2-3]。除肺静脉电位易损伤静脉、隐匿性传导等原因外,主观的消融损伤标注方法或许是造成这一结果的重要因素[4]。VisiTag模块是CARTO 3三维标测系统(美国强生)中自动标测消融损伤的应用软件,已在临床工作中投入使用。通过应用VisiTag模块及设定VisiTag模块内参数,当消融损伤满足预先设置的消融损伤标注条件时,CARTO 3三维标测系统可以自动对消融损伤点进行标注,从而避免人为进行损伤标注的随意性。因此,VisiTag模块也为了解各部位消融损伤差异、探究肺静脉电位恢复的可能原因提供了一种方式。本研究旨在应用VisiTag模块对实现肺静脉电位即刻隔离的环肺静脉消融损伤指标进行分析,以期了解肺静脉电位恢复的可能原因。
1 对象与方法
1.1 研究对象
入选2017年1月至2018年1月在北京大学第一医院接受初次射频消融治疗,并由同一位术者完成的房颤患者。所有患者术前48 h内均经食管超声心动图或心房CT造影证实左心房及左心耳内无血栓存在,并排除严重电解质紊乱、甲状腺功能异常、贫血、严重肺疾病、急性心肌梗死、严重心功能不全[纽约心脏协会(NYHA)心功能Ⅲ级或Ⅳ级]情况的患者。患者均签署知情同意书。
1.2 研究方法
1.2.1消融前准备 所有患者在局部麻醉下完成双侧股静脉穿刺并置入鞘管。经左股静脉鞘管送入可调弯十极电极至冠状静脉窦,经右股静脉送入Swartz L1型和Swartz R0型长鞘。X线透视下行房间隔穿刺两次,将长鞘送至左心房。房间隔穿刺后立即根据体重静脉推注普通肝素100 U/kg,后续根据活化凝血时间检测结果追加肝素,使活化凝血时间维持在250~350 s。通过Swartz L1型鞘管行双侧肺静脉及左心房造影并送入射频消融导管进行标测与消融。经Swartz R0型鞘管送入多电极标测导管Lasso或PentaRay,在CARTO 3三维标测系统辅助下进行左心房三维电解剖标测、识别及记录肺静脉电位。
1.2.2环肺静脉电隔离术 因所有患者初次接受房颤射频消融治疗,消融策略仅为围绕双侧肺静脉连续消融实现环肺静脉电隔离。该过程由同一术者应用8.5 F SmartTouch冷盐水灌注压力感知消融导管完成。消融采用冷盐水灌注模式,灌注速度为非消融时2 ml/min,消融时17 ml/min。温度上限设置为43℃,功率设置为后壁20~30 W,非后壁30~40 W,应用VisiTag模块自动标注消融损伤点。当消融损伤标注点出现后,术者应结合消融部位局部电位振幅、极性变化及消融阻抗下降幅度等情况综合决定消融时间,但单点连续消融时间不超过60 s。完成连续的环肺静脉消融后,应用多电极标测导管和起搏方式验证心房-肺静脉电传导是否隔离及是否实现心房-肺静脉传导的双向阻滞。如果未实现上述目标,在多电极标测导管指导下对存在肺静脉电位部位进行补点消融,最终实现心房-肺静脉电传导的双向阻滞(图1)。
1.2.3VisiTag模块设置 VisiTag模块包含下列设置参数:导管最大移动范围、导管最短稳定时间、一定时间的导管-组织接触力(force over time,FOT)、阻抗下降和目标温度。消融时仅限定导管最大移动范围为3 mm和最短消融时间为20 s,对其他参数不予设定。术后在原参数设置基础上对FOT进行设定,以分析环肺静脉消融时各部位导管稳定性特点。因采用冷盐水灌注模式,不对目标温度进行设定。
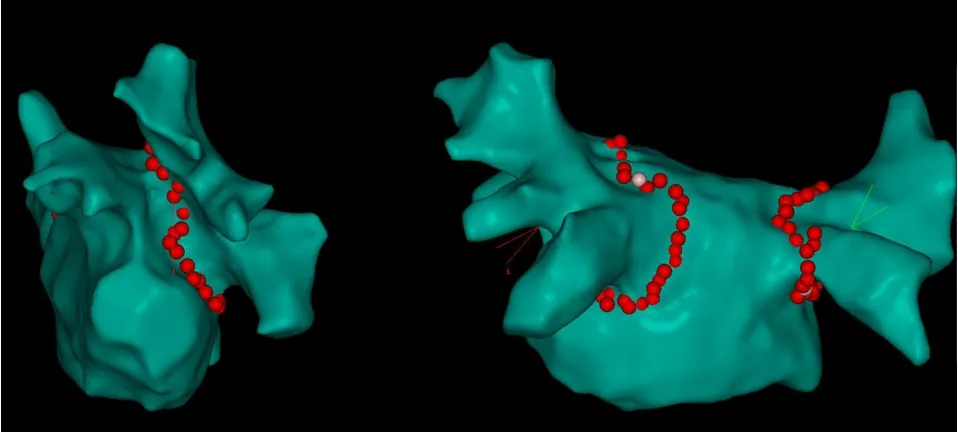
图1 应用冷盐水灌注压力感知消融导管和自动损伤标注软件VisiTag模块完成的双侧环肺静脉电隔离术
1.2.4环肺静脉消融损伤差异分析 参照既往研究的分段方法,将围绕同侧肺静脉的环形消融损伤线分为8个节段,分别为前上、前中、前下、底部、后下、后中、后上和顶部,双侧共16段[5]。应用VisiTag模块对消融损伤进行自动标注并对消融数据进行采集,包括消融点平均导管-组织接触力(contact force, CF)、最小CF、最大CF、初始阻抗值、阻抗下降值、接触力-时间积分(force-time integral, FTI)等参数。将消融点按上述分段分为16组,比较不同节段消融点平均CF均值和FTI均值,平均CF<10 g和FTI<400 g · s消融点百分比。此后设置FOT参数为最小CF 5 g和限定时间百分比为50%,统计在此参数设置下消失的消融点数目,计算各段中消失点占关闭FOT设置时自动消融标注点的百分比。
1.3 统计学分析
所有数据应用SPSS 20.0统计软件进行统计分析。正态分布计量资料以(±s)表示,计数资料以百分率表示。同一患者同一节段内的多个消融点平均CF、FTI取平均值,多组间平均值的比较应用单因素重复测量方差分析,多组间率的比较应用卡方检验。以P<0.05为差异有统计学意义。
2 结果
2.1 患者基线及手术一般资料
共入选28例患者,年龄39~82(62.9±11.2)岁,其中男性22例(78.6%),阵发性房颤19例(67.9%),术前左心房前后径(4.09±0.49)cm,术前左心室射血分数(65.41±6.74)%,所有肺静脉隔离即刻未发生手术相关并发症。
2.2 环肺静脉消融各节段损伤指标比较(表1)
共记录到2175个消融点,各消融点节段组间平均CF均值、FTI均值、平均CF<10 g的消融点百分比、FTI<400 g · s消融点百分比、打开FOT设置后消失点占关闭FOT设置时自动消融标注点的百分比比较,差异均有统计学意义(均P<0.001)。
左前各节段消融点平均CF均值显著低于其他节段,其中左前上及左前下两节段平均CF均值不足10 g,分别为(8.8±3.1)g和(9.3±4.2)g。尽管大多数消融节段平均CF均值超过10 g ,但每一节段都有平均CF<10 g的消融点。与各节段平均CF均值分析结果相仿,左前下、左前上和左前中三个节段平均CF不足10 g 的消融点所占百分比最高,分别为57.6%、55.8%和45.1%,而右顶部消融点平均CF不足10 g的百分比最小为9.0%。受到各消融点平均CF较低的影响,左前下、左前上和左前中三节段成为各节段中消融点FTI均值最低的区域,分别为(406.2±163.9)g · s、(388.5±141.0)g · s和(428.2±152.8)g · s。上述三节段消融点FTI<400 g · s
的百分比也最高,分别为41.5%、38.8%和40.7%。当进一步严格消融损伤自动标注标准,增设FOT参数,将消融损伤自动标注所需最小CF设定为5 g和限定时间百分比为50%时,不少原已标注的消融损伤点消失,其中仍以左前上和左前中节段最为显著,分别达到34.5%和29.0%。与左侧环肺静脉消融损伤线相比,右侧环肺静脉消融损伤线各节段消融损伤的各项指标相差不明显,且总体趋势优于左侧各节段指标。
3 讨论
STAR AF Ⅱ研究[1]结果表明,环肺静脉电隔离是房颤射频消融治疗的基石。荟萃研究结果显示,即使在持续性房颤患者,环肺静脉电隔离治疗可使66.7%患者在消融后1年仍维持窦性心律,其中80.5%的患者无需抗心律失常药物治疗[6]。实现心房-肺静脉电传导隔离对于房颤的消融治疗至关重要。然而有研究发现,无论房颤复发与否,心房-肺静脉电传导恢复率均高达90%以上,提示心房-肺静脉电传导恢复在房颤复发中扮演的角色仍需探讨。但该研究也表明,使用传统的冷盐水灌注非压力感知导管消融以及人工标注消融损伤的方式并不能取得持久的心房-肺静脉电传导隔离[2]。本研究尝试应用冷盐水灌注压力感知消融导管和自动消融标注软件VisiTag模块来探讨心房-肺静脉电传导恢复的可能原因。
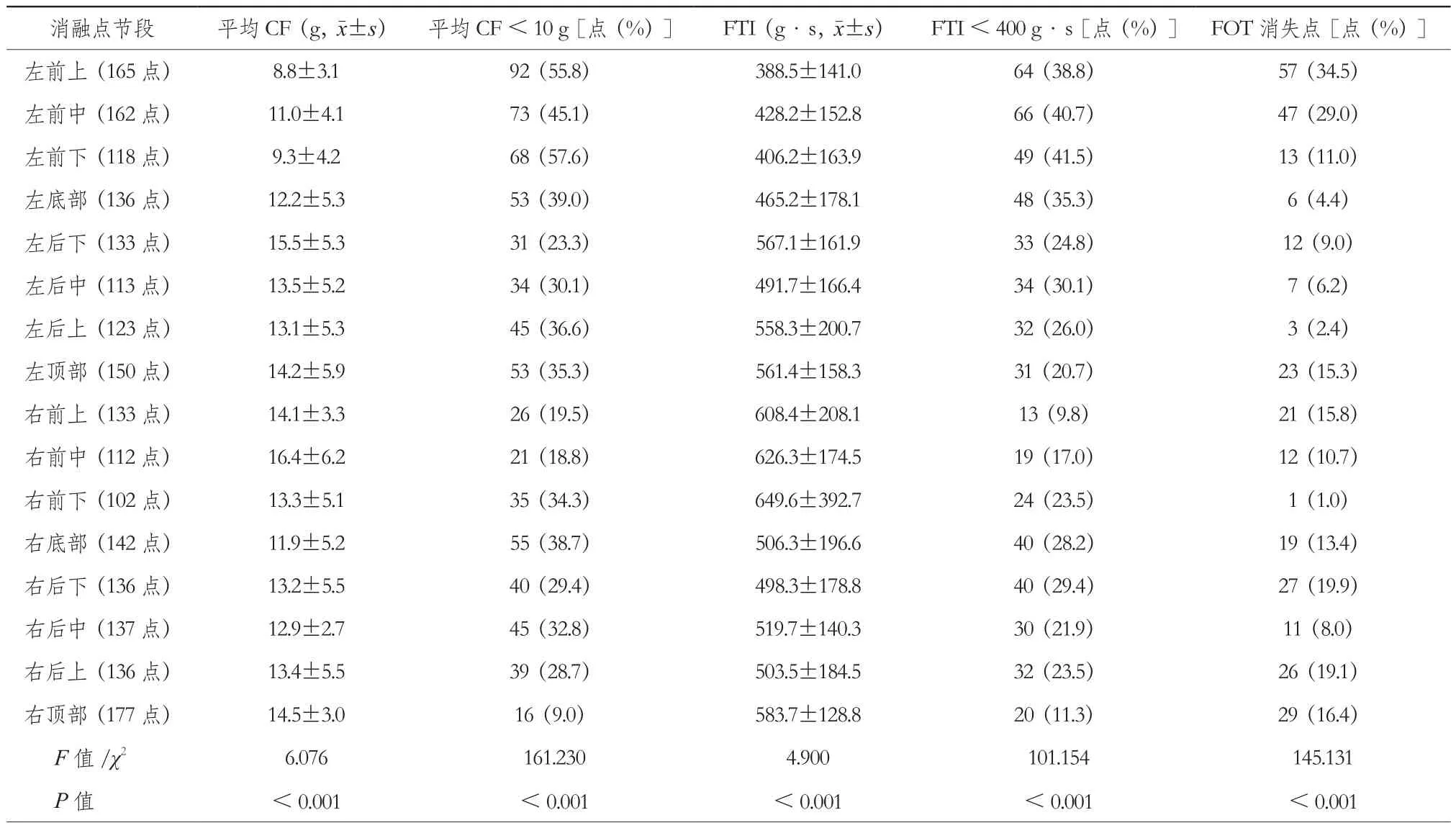
表1 环肺静脉消融各节段损伤指标
本研究在环肺静脉电隔离的逐点消融时应用传统的消融终止参照指标,联合设定了逐点消融时间不少于20 s和消融时导管移动范围不超过3 mm的自动消融损伤标注条件,因而消融损伤效果应该优于传统的消融方式。然而本研究数据分析发现,尽管对消融时间和消融时导管移动范围进行了严格设定,消融损伤指标仍不理想。将左前上节段FTI均值与其他节段FTI均值两两比较,左前上节段FTI均值与左前中、左前下和左底部节段差异均无统计学意义(均P>0.05),而与其他节段比较差异均有统计学意义(均P<0.05)。
国内外研究均表明,环肺静脉消融时左侧肺静脉前部为心房-肺静脉电传导恢复的好发区域[7-8]。目前认为,多因素导致该区域成为心房-肺静脉电传导恢复的好发部位,但确切机制仍需探讨。本研究利用冷盐水灌注压力感知消融导管和消融损伤自动标注软件VisiTag模块对环肺静脉消融损伤分析发现,左侧肺静脉前部消融损伤的平均CF均值和FTI均值低于其他消融节段,且不能达到FOT设置要求的自动消融损伤标注点最多,提示消融时左侧肺静脉前部FOT不足和导管稳定性不佳或许是心房-肺静脉电传导恢复的重要原因,从而影响房颤射频消融术后的房颤复发,而房颤患者射频消融术后房颤是否复发是生活质量的重要影响因素[9-10]。
然而,一系列因素导致本研究结果具有一定的局限性,包括入选患者例数较少、仅入选一位术者的手术病例、缺乏对消融患者的远期随访结果,并未随访房颤复发患者模块标测的结果和手术记录复发部位两者是否吻合。因此还需要大规模、多中心和长期随访的临床研究加以证实。

