基于多维视角考查“中和反应”解读
陆桂斌
(江苏省泰州市智堡实验学校 225300)
酸、碱“中和反应”是初中化学极其重要的一类反应,也是一种特殊的复分解反应,有关其概念辨析、实际应用、微观实质、质能变化等考查是历年各地中考化学命题的热点.本文结合近年典型中考试题,对其多维考查视角做一个梳理和解读,以提高复习备考效率.
一、考查“中和反应”的概念及其应用,彰显化学学科价值
例1(2013辽宁沈阳)下列关于中和反应的说法,正确的是( ).
A.纯碱和稀盐酸混合后发生中和反应
B.有盐和水生成的反应一定是中和反应
C.工厂废水中含有的硫酸可以用氨水中和
D.中和反应的发生必须借助酸碱指示剂进行判断
评析本题是一道基础题,试题难度虽然不大,但能较好地检测学生对“中和反应”的概念、常见物质所属类别等双基的正确理解以及灵活运用知识的能力.酸与碱作用生成盐和水的反应称为中和反应,常见酸与碱都能发生中和反应,不需借助指示剂进行判断,故选项D错误;酸、碱中和生成盐和水,但能生成盐和水的反应不只中和反应一种,如金属氧化物与酸、部分非金属氧化物与碱反应也能生成盐和水,故选项B错误;选项A中是盐(纯碱)与酸反应,与中和反应概念不符,故也不正确.选项C中硫酸(酸)与氨水(碱)发生了中和反应.答案:C
例2 (2017新疆)中和反应在生活中有广泛应用.下列应用不属于中和反应的是( ).
A.用盐酸除铁锈
B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤
D.用硫酸处理印染厂含碱废水
评析《义务教育化学课程标准》明确要求重视编制具有实际情景、应用性和实践性较强的试题,这既能了解学生掌握有关知识、技能和方法的程度,又能突出对学生解决实际问题能力的考查,本题则较好的体现了这一命题指导思想.试题的素材和背景源于生活、生产实际,既真实鲜活又符合学生的认知发展水平,彰显了化学学科价值.由例1评析可知:解答本题的关键首先是对常见物质所属类别做准确的判断,再结合“中和反应”概念作选择,答案:A
二、考查“中和反应”的微观实质,凸显化学学科特质
例3 (2016广东广州)向滴有几滴酚酞的氢氧化钠溶液中滴加稀盐酸至恰好完全反应.

(1)上述过程的实验现象为____.
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子____.(填离子符号)
(3)氨水(NH3·H2O)也能使酚酞变色,原因是氨水和氢氧化钠溶液中均含有一种相同离子,该离子是____.(填离子符号)
评析宏观辨识与微观探析反映了化学学科专属特性,也是化学学科核心素养的一个重要维度,化学的学习与研究,需要建构“宏观—微观—符号”三重表征的思维方式.近年来,以考查学生三重表征的意识、能力为意图的中考化学试题精彩纷呈,本题结构即较好地展示了“宏观现象——微观分析——符号表达”这一基本思维过程.(1)滴有酚酞的氢氧化钠溶液呈红色,向其中继续滴加稀盐酸,溶液由红色逐渐变成无色.(2)分析反应的微观示意图,反应前有四种离子——稀盐酸中含H+、Cl-,氢氧化钠溶液中含Na+、OH-;二者恰好完全反应后,只剩下两种离子,结合中和反应微观实质“H++ OH-→H2O”可判断反应后剩余离子为Na+(起始在氢氧化钠溶液中,对应图形“●”) 和Cl-(起始在稀盐酸中,对应图形“○”),而“○”代表离子起始也在氢氧化钠溶液中,则只能为OH-.(3)氨水中含NH4+、OH-,氢氧化钠溶液中含Na+、OH-,比较可知:两溶液中都含OH-,溶液都呈碱性,能使酚酞变红色.
解答这类试题要求学生能基于宏观现象从微观角度分析不同溶液中所含微粒,尤其是所含离子;其次对中和反应的实质“H++ OH-→H2O”要有明确的认知和理解,再比较分析试题具体素材、情境,从而找准答案.当然离子符号、化学方程式等化学用语的正确书写也应是一必备基本功.
变式训练1 (2016广西南宁)“宏观——微观——符号”三重表征是化学独特的表示物质及其变化的方法.请结合下图所示的氢氧化钠溶液和稀硫酸反应的微观示意图,回答下列问题.(1)写出氢氧化钠溶液和稀硫酸反应的化学方程式____.(2)写出图中C方框内甲、乙两种粒子的符号:甲____,乙____.(3)从微观的角度分析,上述反应的实质是____(填粒子符号,下同)和____结合成H2O.

三、围绕“中和反应”中温度、pH、导电性等变化,考查学生数据分析、图表解读等综合能力
例4 (2016 贵州遵义)向一定量的Ba(OH)2溶液中滴加稀H2SO4,下列图像能正确描述对应关系的是( ).
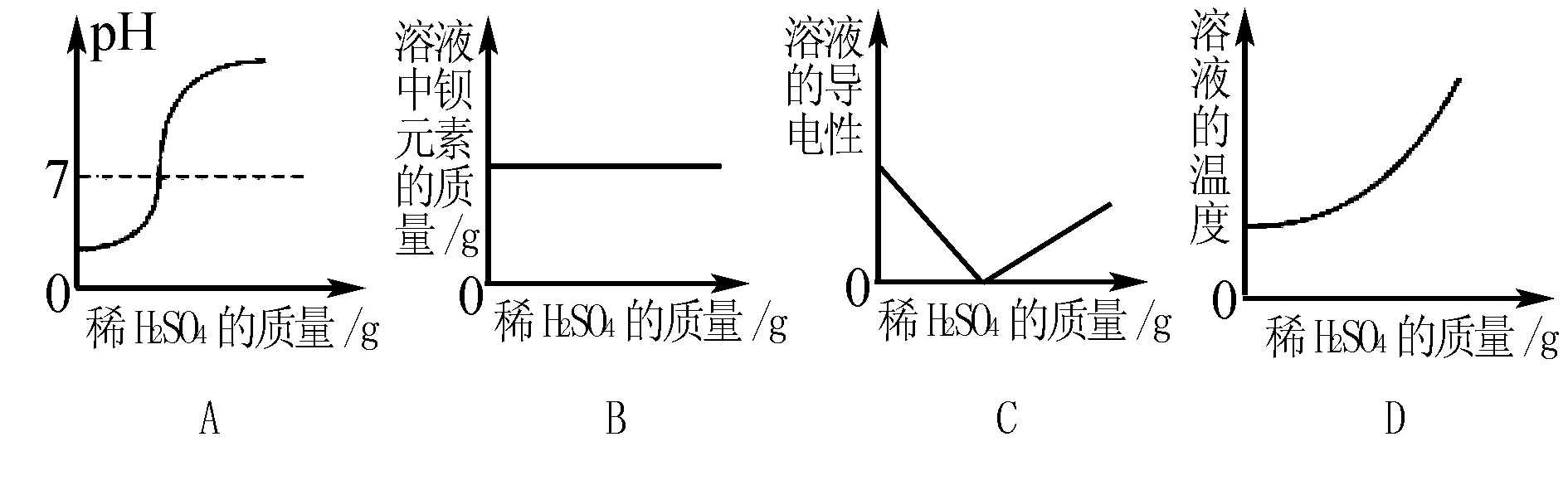
评析以图表的形式呈现酸与碱发生“中和反应”过程中溶液温度、酸碱度、导电能力等量的变化趋势,既直观、形象,又能综合考查学生观察分析、信息处理、判断推理等能力.图像类试题是中考化学经典题型,解答这类试题应抓住“三点一走势”——首先看清图像中横、纵坐标各表示的量,然后从图像的起点、转折点、终点及量的变化趋势来分析答题.


变式训练2 (2016黑龙江大庆)室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示.
(1)由右图可知,盐酸与氢氧化钠溶液中和反应是____(填“吸热”或“放热”或“无热量变化”)反应.
(2)在A处溶液中加入石蕊,溶液呈____色.
(3)B处溶液的溶质是____(填化学式).
(4)B到C的过程中溶液的pH逐渐____(填“增大”或“减小”
或“无变化”).
(5)在C点溶液中加入碳酸钙,现象为____,化学方程式为____.
四、实验探究“中和反应”后溶质的成分,考查学生实验方案设计、方案评价等学科能力
例5 (2017 山东临沂)某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动.请你和他们一起完成以下实验探究.
演示实验将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中.该反应的化学方程式是____.
查阅资料CaCl2滚液显中性
提出问题实验中未观察到明显现象,部分同学产生疑问:反应后溶液中溶质的成分是什么?
猜想与假设针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2;猜想Ⅱ:有____;猜想Ⅲ:有CaCl2和Ca(OH)2;猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是____.
实验探究为了验证其余猜想,各小组进行了下列三个方案的探究.

实验方案滴加紫色石蕊溶液通入CO2滴加Na2CO3溶液实验操作实验现象产生白色沉淀实验结论溶液中含有Ca(OH)2溶液中含有Ca(OH)2溶液中含有Ca(OH)2
得出结论通过探究,全班同学一致确定猜想Ⅲ是正确的.
评价反思(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____.
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑____.
评析初中化学课程承载着一般科学探究方法的学习,实验探究题也是化学中考经典题型.这类试题侧重考查学生对科学探究基本步骤与方法的熟悉和了解、化学核心知识的识记和应用以及实验方案的设计与评价、基于证据的推理与反思能力等诸多方面.因试题的情境、设问灵动而多变,考查的能力、素养开放而多元,对学生提出了较高要求.

猜想与假设中设问考查了学生常识性思维模型的建构水平,盐酸与氢氧化钙反应后溶液中溶质的成分有三种可能:二者恰好完全反应,即猜想Ⅰ;盐酸过量,有CaCl2和HCl,即猜想Ⅱ;氢氧化钙过量,即猜想Ⅲ.而不可能出现猜想Ⅳ的情形,因为盐酸与氢氧化钙不能大量共存.这种认知模型的建构,只要教师在平时教学中注意适当的引导,多数学生都能理解掌握.
实验探究中设问多为这类试题的中心内容,本题只要求学生按照既定的实验方案,根据实验结论反推实验现象,客观上降低了考查的难度.猜想Ⅲ正确,其对应现象分别为:紫色石蕊变红色;产生白色沉淀.
评价反思中的设问考查学生对实验方案的评价能力,意在引导学生在平时学习中注重培养科学、连续和严谨的思维品质,也是同类试题中的难点和失分点.从微观角度分析,本题要能证明溶质中有Ca(OH)2,实质是证明溶液中有OH-,而无须证明有Ca2+(因为所有可能的情形都有CaCl2,溶液中都含Ca2+).因此设计实验方案时,应认真阅读试题文本,对需要探究问题的实质有明晰的把握和认知,这样设计的方案才能科学、合理.如本题要证明溶液中有OH-,除方案1、2已选试剂外,还可选用CuSO4、FeCl3等盐溶液,但不可选用Na2CO3溶液.答案:(1)Na2CO3与CaCl2反应也生成白色沉淀,不能证明一定有Ca(OH)2存在;(2)反应物是否有剩余.其他答案参见评析.
综合上述分析,不难发现有关“中和反应”试题的命制,已不再仅仅停留在基本概念辨析、指示剂变色等浅表层面的考查,而是越来越体现出基于“素养为本”的命题特质:以“核心价值”为引领,既考查能反映化学学科本质的必备知识,也考查学生灵活运用所学知识分析解决问题的关键能力,同时还考查学生通过学习内化的、带有化学学科特性的品质素养.化学中考在经历了由知识立意向能力立意过渡后,正开始由能力立意向学科素养立意的转变,这种转变必将带来中考化学命题内容的重大变革,对此,作为一线化学教师应予以足够的重视.


