危重患者急救中心电图RT融合的危险性
郑文凯 林秋辉 刘林勇
RT融合现象是指心电图QRS波增宽、ST段消失、QT间期缩短,QRS波跟T波融合在一起的一种心电图表现,主要见于危重患者。部分RT融合可以在窦性心律下传心室QRS波中出现,但是多数为室性起源QRS波。
危重患者出现12导联RT融合多为心室起源,偶见窦律下呈12导联RT融合[1],可见于各种疾病如外伤、心肺功能衰竭、急性心肌梗死、心肌炎、糖尿病、尿毒症等疾病的抢救过程中。出现RT融合现象时,患者往往预后较差。本文探讨危重患者心电图显示RT融合与死亡率的相关性。
1 资料与方法
1.1 一般资料
收集漳州市医院2015年1月至2019年8月急诊科和住院危重疾病患者218例,具体包括急性颅脑外伤、多发伤、急性中毒、急性心梗、心肌炎、尿毒症与休克等。抢救时急查心电图诊断为室性逸搏心律,加速性室性逸搏心律,室性心动过速。其中,男123例、女95例,年龄2~90(53.92±10.41)岁。
1.2 方法
采用纳龙心电图机采集心电图,12导联同步记录,通过纳龙工作站报告端口,对患者心电图12导联进行叠加,形成12导联重叠波。见图1、图2。图1和图2上半部分为Ⅱ导联,下半部分为12导联叠加波。以P1、P2、Q、S、T1、T2表示的6条线为测量线,分别放在P波起点、终点(P波消失,这2条线不作为测量线,所得P、PR值无效),QRS波起点、终点,T波起点、终点。当RT融合时,QRS波终点与T波起点重叠,可通过重叠波的切迹或转折点识别QRS宽度,当部分导联完全融合成单相波时,12导联重叠波仍可见RT连接点,当电压极低无法识别时给予剔除。RT不融合时,测量QRS波起点到J点距离为QRS宽度。QT间期为测量QRS波群起点至T波终点的距离,
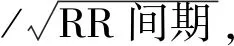

图1 不同心率的RT融合患者的12导联叠加波
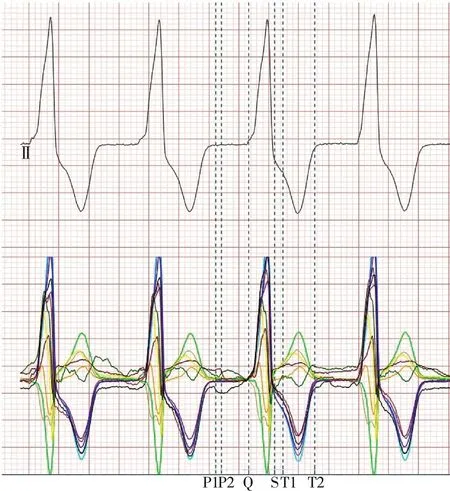
图2 不同心率的RT不融合患者12导联叠加波
Fig.212-lead superposition wave in RT non-fusion group with different heart rates
1.3 统计学方法
2 结果
2.1 RT融合组与RT不融合组心电图参数比较
将12导联心电图显示ST段消失、QRS波与T波融合的患者归入RT融合组,共84例。将12导联ST段不消失、QRS波与T波不融合的患者计入RT不融合组,共134例。与RT不融合组比较,RT融合组QRS波明显增宽(P<0.05),QT间期显著缩短(P<0.05),死亡率明显上升(P<0.01)。见表1。
2.2 按心率快慢分组及心电图参数
按心电图心率的快慢分组,心动过缓组(频率<60次/min)共94例(43.1%),其中融合组24例,不融合组70例。正常心率组(频率60~100次/min)共64例(29.4%),其中融合组23例,不融合组41例。心动过速组(频率>100次/min)共60例(27.5%),其中融合组37例,不融合组23例。各组心电图见图3、图4。
心动过速患者中,融合组与不融合组间QRS波宽度、QT间期、QTc间期无明显差异(P均>0.05),但两组死亡率间的差异有统计学意义(P<0.01)。心动过缓和正常心率患者中,RT融合组与不融合组间QRS波宽度、QT间期、QTc间期、死亡率差异均有统计学意义(P<0.05或P<0.01)。心电图指标比较见表2。
上述结果表明,RT融合可作为判断预后的独立指标。心率逐渐减慢预示心肌缺血逐渐加重,RT融合更易形成电机械分离,死亡率逐渐升高。
3讨论
本研究观察RT融合心电图变化表现为12导联QRS-T综合波从比较正常逐渐演变为QRS逐渐增宽,ST段逐渐缩短、消失,QT间期缩短,RT波完全融合最后形成单相形QRS-T综合波。其过程中的心电图的RT融合发展进程如图5。
心肌自身和心脏外的各种疾病发展到一定时期,导致心肌缺血。缺血可引起心肌细胞产生一系列复杂的电生理变化,如心肌代谢紊乱、动作电位离子电流异常和细胞内外离子浓度异常等,从而影响心肌细胞的电生理特性。RT融合变化即为心肌细胞缺血严重程度在心电图的表现形式。

表1 RT融合组与不融合组心电图各指标和死亡率比较

图3 不同心率的RT融合患者心电图

图4 不同心率的RT不融合患者心电图
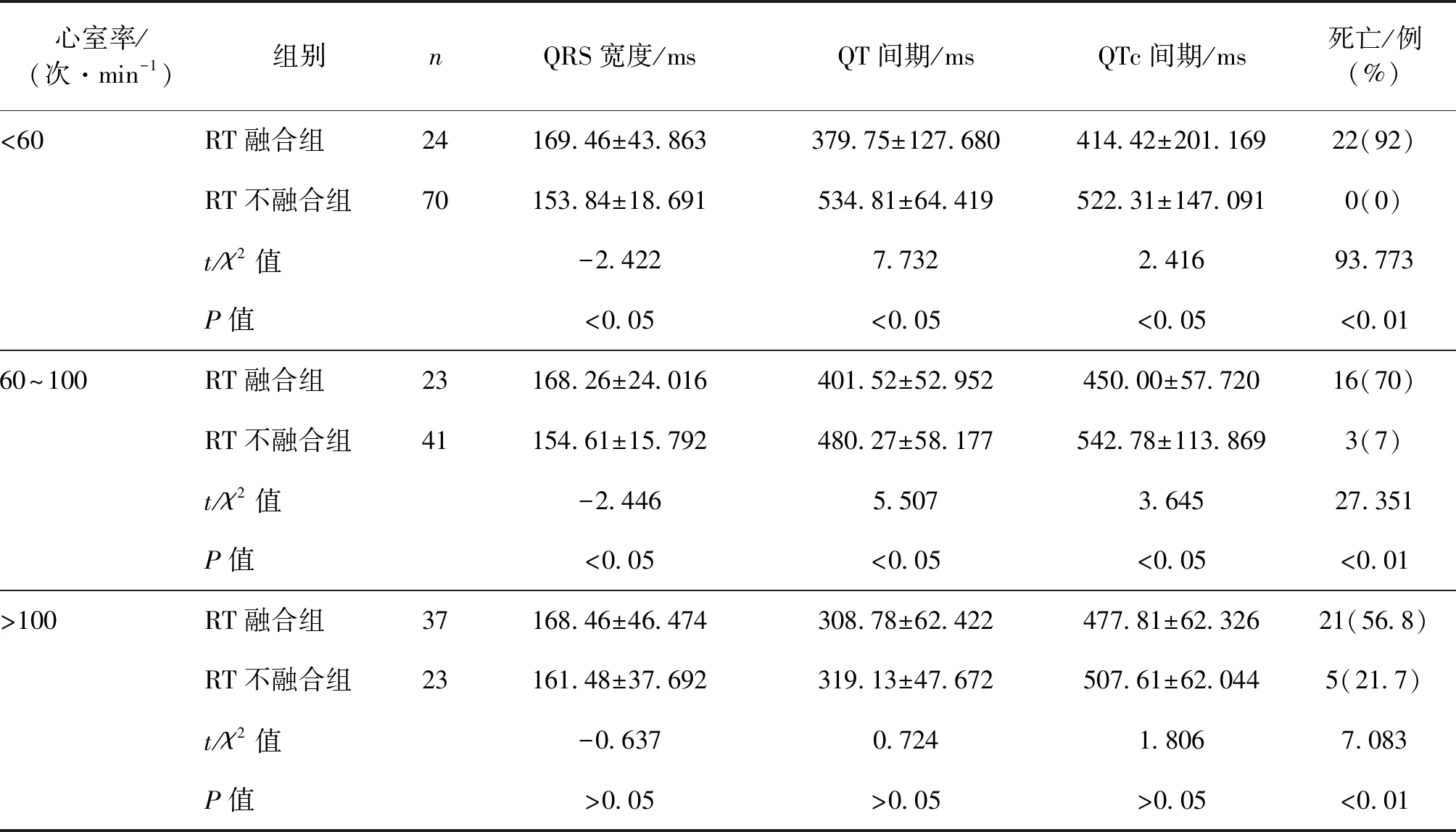
表2 RT融合组与RT不融合组不同心率患者心电图指标比较
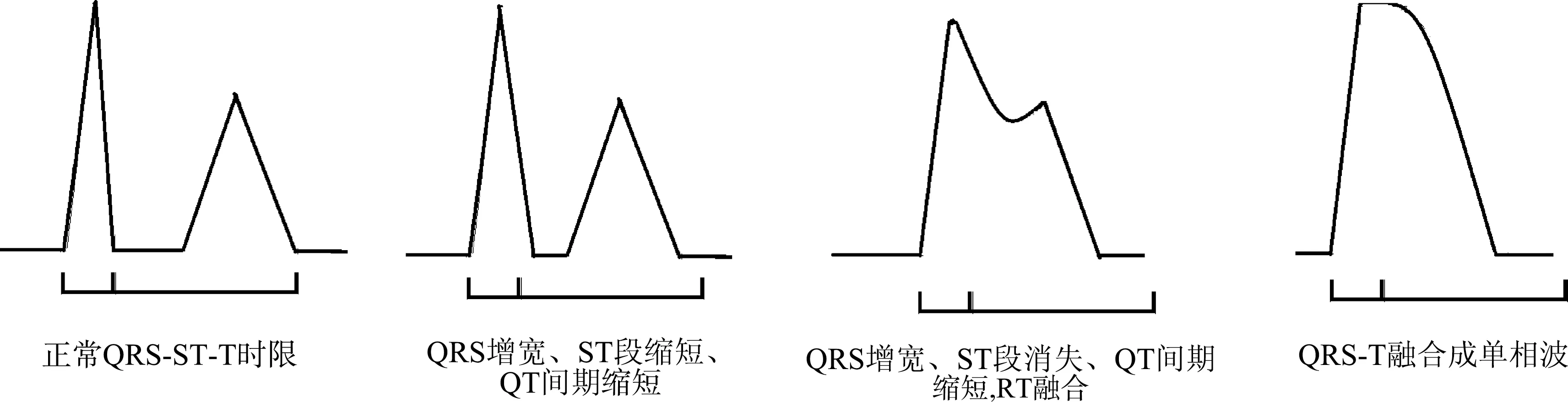
图5 心电图RT融合发展示意图
杜友爱等[2]研究了缺血所致心室肌跨膜电位的变化。结果显示,在缺血2 min时,心肌细胞开始出现动作电位改变;缺血5 min后所有心肌细胞均发生变化,最大舒张电位(MDP)轻度去极化,4相自动去极化速度减慢;缺血15 min后,所有心肌细胞4相自动去极化消失。动作电位持续时间(APD)缩短程度呈时间依赖性。同时,动作电位的2相随着APD的变化逐渐缩短并消失。由于APD 50缩短幅度大于APD 90,动作电位呈三角形,MDP进行性除极,动作电位振幅逐渐降低,最终标本失去兴奋性,不能产生动作电位。缺血至不能诱发动作电位的时间约为30 min[2-4]。
相关研究表明,缺血引起的心肌细胞膜微小结构改变,导致Na+通道受损,0相上升速度减慢,动作电位振幅降低,激动在细胞间和细胞内外的传导速度减慢,影响激动在心室内的传导速率,在心电图上表现为QRS波时限增宽。随着QRS波时限逐渐增宽,发生心室收缩机械不同步概率也显著增加,最终导致泵功能衰竭,更宽的QRS波可能代表更差的心室收缩功能和心室内心肌活动的不协调[5]。
正常情况下,人体细胞外Ca2+浓度远较细胞内高;生理状态下依靠膜的完整性维持Ca2+平衡,当这种完整性因急性缺血、缺氧、酸中毒等原因遭到破坏,钙通道阻断作用降低,Ca2+可持续性内流,2相平台期缩短,同时细胞膜对K+通透性增加,K+外流加速,使3相复极加快,时间变短,从而导致心室肌细胞的动作电位2、3相时间缩短。此外,心电图显示ST段几乎消失,T波上升支在QRS波结束后立即出现,出现RT融合现象。因此,Q-T间期的缩短实质上是由于ST段消失(或显著缩短)所致。由于Ca2+作为递质在心肌兴奋-收缩偶联中发挥作用,细胞内Ca2+浓度的异常升高导致心肌细胞不可逆损伤,一方面可引发恶性室性心律失常,另一方面心肌细胞从收缩活跃状态退化为不收缩状态,最终兴奋-收缩偶联消失,出现电机械分离,这可能是QT间期缩短后产生严重后果的重要原因[6-8]。
本组统计数据显示,RT融合患者中,心室率快慢对死亡率有明显影响,心率越慢,患者死亡率越高。心肌细胞在缺血、缺氧情况下,缺血区心肌激动延迟可诱发折返形成室性心动过速,或快反应自律性转化为慢反应自律性,慢通道激活心脏,潜在的起搏点转变为慢反应电位活动,随着膜电位减小,室性异位起搏点自律性不断增高,形成室性心动过速。室性心律出现后,心脏由主泵和辅助泵共同完成心脏泵功能转变成由心室单独完成,随着心室收缩顺序异常,有效射血减少,心输出量减少,机体组织缺血缺氧加重,可造成压力反射迟钝,心肌缺血进一步加重,异位起搏点自律性逐渐降低,最终心跳停止。RT融合反应表明心肌缺血严重,心室率由快到慢也反映心肌缺血的进展趋势[9]。
综上所述,RT融合实质是心肌严重缺血,心肌细胞膜完整性遭到破坏,细胞从收缩活跃状态向不收缩状态退变,最终造成电机械分离。抢救中,应及时判断RT融合(包括QRS波时限增宽、ST段消失及QT间期缩短)心电图特征性现象,结合心室率快慢,寻求纠正心肌缺血的方法以提高急诊救治成功率。

