纤维素基希夫碱铜配合物的制备及抗菌性能研究
徐永建 雷 凤 李 伟
(1.陕西科技大学轻工科学与工程学院,陕西省造纸技术及特种纸品开发重点实验室,轻化工程国家级实验教学示范中心,中国轻工业纸基功能材料重点实验室,陕西西安,710021;2.华南理工大学制浆造纸工程国家重点实验室,广东广州,510640)
自然界中存在各种形态各异的细菌、霉菌等微生物。在生活中人们不可避免地与这些微生物接触,其中有害的微生物会给人们的健康造成危害。据统计,全球每年约有1700万人死于细菌感染[1]。随着生活水平的提高,人们越来越关注自身的生活环境,对抗菌材料的关注也日益增多,新型、绿色、高效的抗菌剂及抗菌材料的研发逐渐成为研究热点[2-4]。纤维素作为一种可再生的天然高分子材料,具有来源广泛、生物可降解和价格低廉等优点,且分子链中具有大量的羟基,易于表面改性,进而能与许多小分子化合物或金属粒子发生相互作用,可作为一种良好的抗菌剂载体[4-5]。然而,纤维素纤维本身并不具有抗菌性能[6],因此需对纤维素纤维进行改性处理,将具有抗菌性能的抗菌剂负载在纤维上,或者对纤维素进行改性,使其具有抗菌性能,从而制备出具有高效抗菌性能、生物相容性好且生物可降解的绿色抗菌材料[7-9]。
目前抗菌剂分为无机抗菌剂、有机抗菌剂和天然生物抗菌剂三大类型。无机抗菌剂包括金属元素抗菌剂、光催化抗菌剂和纳米抗菌剂[10],这类抗菌剂具有安全、抗菌持久等优点,广泛应用于塑料、纤维、建材等制品。但也有不足之处,比如价格昂贵,不具有抗菌速效性及对霉菌没有效果等。有机抗菌剂主要有季铵盐、乙醇、双胍类化合物、甲醛、有机卤素化合物、卤代烷及碘化物等,能够起到杀菌、防腐、防霉、防藻等作用,广泛应用于生活中的各个方面。但是有机抗菌剂除了可以抗菌和杀菌之外,其本身也具有一定的毒性,这就限制了其在纺织、卫生、医药等领域的一些应用[11]。天然生物抗菌剂取材于自然,绿色环保,对其的研发和使用符合当代发展的潮流,主要有氨基酸类、天然肽类、高分子糖类等,资源十分丰富,然而天然生物抗菌剂存在量少,制备难度大且成本较高,从而限制了对其的研究开发与应用[12]。综上所述,单一的抗菌剂都各有利弊,所以将其两种或者多种协同起来应用,有望取得更加优异的抗菌效果。
希夫碱是指含有亚甲胺基C N的一类化合物,亦称亚胺[13]。近年来,由于希夫碱独特的光、电、磁等物理材料性能,良好的配位化学性能以及独特的抗菌、抗癌、除草等生理活性,引起了人们广泛、系统、深入的理论与应用研究[14-16]。氨基酸是有多个N、O配位原子的特殊结构,研究此类氨基酸配体的配合物,有助于了解生物体内金属离子-蛋白质间的键合作用,可用来进行生物模拟,并且它是细胞生长所必需的,而癌变细胞比正常细胞对氨基酸的需求量大得多,这样氨基酸希夫碱配体就可能将抗癌基因运载到癌变细胞内,从而增大杀伤癌变细胞的选择性,因此具有抑菌抗癌的活性[17-18]。Sevgi F等人[19]研究了甘氨酸希夫碱配体及其Fe3+、Co2+、Ni2+、Cu2+和Zn2+5种配合物的抗菌性能,结果显示配体及其5种金属配合物对5种革兰氏阳性菌和3种革兰氏阴性菌以及1种真菌都展示出比较优异的抗菌性能。Pervaiz M等人[20]研究了亮氨酸希夫碱配体以及Co2+、Mn2+、Cu2+和Cd2+4种金属配合物,通过傅里叶变换红外光谱仪 (FT-IR)、气相色谱/质谱联用仪 (GC-MS)、核磁共振技术 (NMR)等多种手段和途径表征配体及配合物的成功制备,且配体及其4种金属配合物都对细菌和真菌有较好的抗菌效果,配合物的抗菌效果相对于配体更优异。以上结果都说明,希夫碱及其金属配合物都具有良好的抗菌性能。
本研究采用针叶木浆板为原料,通过高碘酸钠溶液氧化针叶木纤维使其具有更多的醛基,制得针叶木氧化纤维 (DAC),进而与甘氨酸中的氨基进行希夫碱反应生成纤维素基希夫碱配体 (DAC-Gly),最后与铜离子以配位键的形式结合,制备出具有优异抗菌性能、绿色、新型的纤维素基希夫碱铜配合物(DAC-Gly-Cu)。利用扫描电子显微镜 (SEM)、能谱分析仪 (EDS)、FT-IR、X射线衍射仪 (XRD)、紫外-可见分光光度计 (UV-Vis)等手段对制备DACGly-Cu过程中纤维的形貌及结构进行表征分析,使用电感耦合等离子体 (ICP-AES)检测金属配合物中的金属离子含量,并对配合物的抗菌性能进行了研究。
1 实 验
1.1 实验原料
漂白硫酸盐针叶木浆板 (取自红塔仁恒纸业有限公司);Cu(CO2CH3)2、H2SO4、H2O2、HNO3(由上海化学试剂有限公司提供,分析纯);甘氨酸 (由上海阿拉丁生化科技股份有限公司提供);高碘酸钠(由天津市科密欧试剂有限公司提供,分析纯);无水乙醇 (由天津市富宇精细有限公司提供,分析纯);去离子水。
1.2 实验仪器
电热恒温鼓风干燥箱 (DHG-9075A,上海齐欣科学仪器有限公司);扫描电子显微镜 (VEGA 3 SBH,美国捷克TESCAN公司);能谱分析仪 (美国捷克TESCAN公司);傅里叶变换红外光谱仪 (德国Bruker公司);X射线衍射仪 (D/max2200Pc,日本理学公司);电感耦合等离子体质仪 (IRIS Intrepid II,美国热电公司);紫外-可见光吸收光谱仪 (Cary 5000,美国安捷伦科技公司)。
1.3 实验方法
1.3.1 针叶木氧化纤维 (DAC)的制备
称取针叶木浆板4 g,在水中浸泡24 h,经疏解、挤压、撕浆后放置于锥形瓶中,加入200 mL 0.1 mol/L的高碘酸钠溶液,在50℃下连续搅拌,氧化反应1.0 h,制得DAC,整个反应在避光条件下完成。将DAC用去离子水充分洗涤,再置于去离子水中浸泡3天,然后抽滤3次,撕散后置于密封袋中平衡水分并测定水分含量,保存备用。
1.3.2 纤维素基希夫碱配体 (DAC-Gly)的制备
称取0.75 g甘氨酸溶解在30 mL乙醇的水溶液中 (乙醇 ∶水=1∶2),待其完全溶解后,加入0.8 g(绝干)DAC,在60℃下连续搅拌1 h进行希夫碱反应,反应完成后将制得的DAC-Gly进行抽滤,然后用去离子水洗涤3次,再抽滤,在60℃真空干燥箱内干燥,保存,备用。
1.3.3 纤维素基希夫碱铜配合物 (DAC-Gly-Cu)的制备
称取0.6 g的Cu(CO2CH3)2,溶解于30 mL乙醇的水溶液中 (乙醇 ∶水=1∶2),待其溶解后,加入0.3 g DAC-Gly(绝干),在60℃下连续搅拌,反应1 h,反应完成后将制备的DAC-Gly-Cu进行抽滤,然后用去离子水洗涤3次,再抽滤,60℃真空干燥箱内干燥,保存备用。DAC-Gly-Cu制备反应机理图见图1。

图1 DAC-Gly-Cu的制备反应机理示意图
1.3.4 样品的表征
(1)FT-IR分析
采用FT-IR分析纤维官能团的化学结构变化,扫描范围为400~4000 cm-1。具体操作方法为:首先将一定量的样品碎化至粉末状,再分别将KBr和样品以一定的质量比 (约200 ∶1)放置在玛瑙研钵中研磨至混合均匀,然后在压膜机上进行压膜,制得透明的固体KBr压片,并进行后续样品测试。
(2)UV-Vis分析
紫外可见分光光度计用来分析物质的组成及含量。UV-Vis扫描范围为200~800 nm。
(3)XRD分析
XRD主要用来分析样品的结晶结构。具体测试条件:采用Cu Kα,管压40 kV,管流40 mA,扫描速度0.2°/s,采样宽度 0.02°,扫描范围 2θ=5°~60°。
(4)SEM分析
SEM主要用来表征样品的表观形貌。本研究采用SEM扫描样品的加速电压为15.0 kV。具体操作方法为:首先将样品进行喷金处理,然后采用二次电子成像模式观察样品的表面形貌。
(5)EDS分析
EDS主要用来对材料微观区域的元素分布进行定性定量分析。具体操作方法为:首先将样品置于载物台上,然后采用能谱分析仪检测样品的元素分布。
(6)ICP-AES分析
ICP-AES主要用于测定样品中金属离子的含量。首先将待检测的样品消解至澄清透明的溶液,消解步骤为:称取0.025~0.050 g绝干样品于聚四氟乙烯管中,加入6 mL硝酸和2 mL过氧化氢,在180℃下加热直至样品完全消解,待溶液冷却后,移入100 mL容量瓶中,聚四氟乙烯管用去离子水洗涤3次,洗涤液移入容量瓶中,定容,所得溶液采用ICP法测定金属离子浓度。
(7)抗菌效果检测
参照GB/T 20944《纺织品抗菌性能的评价》中琼脂平皿扩散法测定样品的抗菌性能。具体操作为:采用大肠杆菌对样品进行抗菌实验,将大肠杆菌的细菌悬浮液均匀分散在固体培养基中,再将直径为12 mm的圆形试样置于培养基中,将含有试样的培养基在37℃培养箱中恒温培养18~24 h。对抑菌圈拍照同时测定抑菌圈直径。
2 结果与讨论
2.1 FT-IR分析
为了表征纤维在制备DAC-Gly-Cu过程中的结构变化,分别对针叶木纤维、DAC、DAC-Gly以及DAC-Gly-Cu进行FT-IR谱图分析,结果如图2所示。

图2 针叶木纤维、DAC、DAC-Gly及DAC-Gly-Cu的FT-IR谱图
由图2(a)可知,与针叶木纤维相比,DAC在1730 cm-1处出现了一个较为明显的特征吸收峰,这是醛羰基的特征吸收峰[21-22],因此可以说明,针叶木纤维被高碘酸钠成功选择性氧化。除此之外,经高碘酸钠氧化后,纤维素的特征吸收峰没有发生改变,其特征吸收峰分别是3350 cm-1的—OH伸缩振动吸收峰、2901 cm-1处的C—H伸缩振动吸收峰、1431 cm-1处的—CH2对称弯曲振动吸收峰、1373 cm-1处的C—H弯曲振动吸收峰、1165~1034 cm-1处的纤维素骨架C—O伸缩振动吸收峰、896 cm-1处的葡萄糖单元间糖苷键的C—H变形振动吸收峰。这表明高碘酸钠选择性氧化的同时并没有破坏纤维素分子的结构。醛基含量是表示纤维素氧化程度的唯一量化指标,根据坎尼扎罗 (Cannizzaro)反应原理对针叶木纤维的醛基含量进行了测定,图3为经高碘酸钠氧化前后纤维醛基含量的变化情况。从图3可知,高碘酸钠氧化针叶木纤维使得纤维素中醛基含量大幅上升,这个结果也证实了DAC的FT-IR谱图中醛羰基吸收峰的出现。
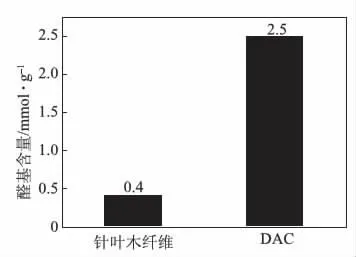
图3 针叶木纤维与DAC的醛基含量
由图2(b)可知,DAC-Gly和 DAC-Gly-Cu在1650 cm-1附近均出现了新的吸收峰,此峰为—C N的伸缩振动吸收峰,且配合物的吸收峰相对于配体有一定的红移,说明希夫碱配体上的氮原子参与了配位,在543 cm-1处出现了吸收峰,可以认为是Cu-N配位键的形成[20],配合物形成后,—COO的吸收峰也出现了红移,说明羧酸根参与配位,并且在460 cm-1处出现了新的吸收峰,可以认为是Cu—O配位键的形成。以上结果证明,DAC-Gly和DAC-Gly-Cu均已成功制备,且没有改变纤维素大分子的化学结构。
2.2 UV-Vis分析
采用UV-Vis测定了 DAC-Gly和 DAC-Gly-Cu的紫外光吸收光谱,测定结果如图4所示。
由图4可知,DAC-Gly的紫外光吸收峰分别出现在244、297、463 nm处,可分别认为是葡萄糖环和DAC-Gly的π→π*跃迁和DAC-Gly的n→π*跃迁产生的吸收峰[20],当制备DAC-Gly-Cu后,吸收峰均发生了较明显的红移,是因为亚胺基上的N与中心金属离子发生了配位作用[23],使电子离域程度增大,导致配合物中电子活动范围更大,相关共轭分子轨道的能级跃迁所需能量降低。
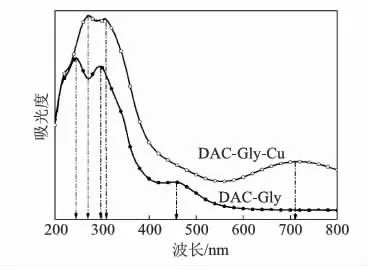
图4 DAC-Gly和DAC-Gly-Cu的紫外光吸收光谱

图5 针叶木纤维、DAC、DAC-Gly、DAC-Gly-Cu的XRD谱图
2.3 XRD分析
为了研究在制备DAC-Gly-Cu过程中纤维素晶型结构的变化,分别对针叶木纤维、DAC、DAC-Gly以及DAC-Gly-Cu的结晶结构进行XRD分析,结果如图5所示。
从图5可知,针叶木纤维具有较好的结晶结构,出现了4个衍射峰,分别是位于14.9°的101晶面,16.1°的 101-晶面,22.5°的002晶面以及34.4°的040晶面,属于纤维素 I型结晶变体[24]。另外,从图5中可以看到,高碘酸钠氧化对针叶木纤维的结晶结构产生了较为明显的影响,DAC的衍射峰强度降低并略有变宽,结晶度明显降低,说明氧化过程破坏了纤维素高分子链内和链间的氢键,纤维素内部结构变得疏松,高分子排列的规整度降低,结晶度下降。针叶木纤维的结晶度为68.52%,DAC的结晶度降低为57.94%,说明氧化过程中氧化反应生成的醛基使针叶木纤维素分子内与分子间的氢键受到很大的破坏,束缚分子运动的作用力就会减弱,再加上醛基的体积较大,使分子间距离增大,自由度增加,从而使氧化后纤维素的结晶度下降。从图5中谱图来看,希夫碱反应并没有改变纤维素I的结晶结构,但是结晶度相对于针叶木纤维原料略有降低,这都是因为纤维素经过化学反应,结晶结构有一定的破坏,这些变化也都说明希夫碱反应的成功进行。由图5中DAC-Gly-Cu的谱图可知,DAC-Gly与Cu2+配合后,依然没有改变纤维素 I的结晶结构,并在 2θ=9.4°、18.9°、28.5°处出现了新的衍射峰,这可能归属于希夫碱铜配合物晶体的衍射峰。这些特征峰的出现可以说明Cu2+成功地固载在DAC-Gly上[25]。

图6 针叶木纤维、DAC、DAC-Gly和DAC-Gly-Cu的SEM图
2.4 形貌分析
采用 SEM对针叶木纤维、DAC、DAC-Gly及DAC-Gly-Cu的形貌进行观察,结果如图6所示,并结合EDS对DAC-Gly-Cu进行局部面扫,测定纤维表面上各个元素含量,结果如图7所示。
由图6(a)、图6(b)可知,针叶木纤维表面光滑,而DAC表面皱缩,这可能是高碘酸钠氧化的结果。由图6(c)可发现DAC-Gly纤维有断裂的现象,说明希夫碱反应对纤维素产生了一定的降解作用。由图6(d)可知,DAC-Gly-Cu纤维表面变得粗糙不平,覆盖着颗粒状的物质,这可能是配合物形成的晶体。由图7可知,DAC-Gly-Cu含有C、O、N、Cu 4种元素。以上这些结果在一定程度上证明DACGly-Cu已成功制备。

图7 DAC-Gly-Cu的EDS结果
2.5 Cu2+含量分析及抗菌性能评价
通过ICP-AES分析法定量检测DAC-Gly-Cu中Cu2+浓度,进而绘制出Cu2+的质量分数柱状图,如图8所示。本研究选用大肠杆菌作为实验细菌,对样品进行抗菌实验,并采用琼脂平皿扩散法评价其抗菌性能,结果如图9所示。
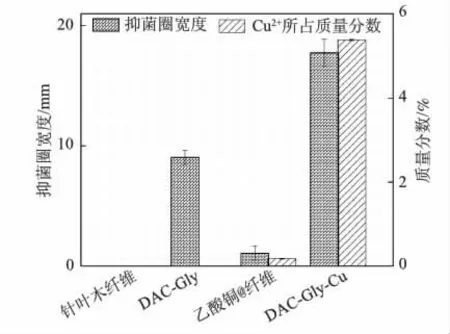
图8 Cu2+在针叶木纤维、DAC-Gly、乙酸铜及DAC-Gly-Cu中的质量分数

图9 针叶木纤维、DAC-Gly、乙酸铜溶液及DAC-Gly-Cu的抑菌效果
由图8可知,通过ICP-AES检测浸渍乙酸铜溶液的纤维中的Cu2+浓度,然后计算得其中的Cu2+所占质量分数仅为0.18%,但是在DAC-Gly-Cu中Cu2+所占的质量分数大幅增加,为5.39%。由图8抑菌圈宽度及图9的抑菌效果可知,DAC-Gly及DAC-Gly-Cu对大肠杆菌有较为明显的抑菌效果,分别出现了不同程度大小的抑菌圈 (宽度分别为9.06 mm和17.74 mm)。而针叶木纤维周围未出现抑菌圈,其抑菌圈宽度为0,说明针叶木纤维并无抗菌性。浸渍有乙酸铜溶液的纤维试样对大肠杆菌有微弱的抗菌性,抑菌圈宽度仅为1.095 mm,其原因可能是通过浸渍乙酸铜溶液的纤维试样上Cu2+含量远远低于纤维素基希夫碱铜配合物中的Cu2+含量,通过ICP-AES所得数据也证实了这个结果,因此DAC-Gly-Cu拥有更好的抗菌性能。
3 结论
本研究以针叶木浆为原料,采用高碘酸钠对其进行氧化制得针叶木氧化纤维,经希夫碱反应获得纤维素希夫碱配体,再与Cu2+以配合键形式结合,制备出一种新型的纤维素基希夫碱铜配合物,并对配合物抗菌性能进行了研究。
3.1 针叶木氧化纤维 (DAC)的FT-IR谱图在1730 cm-1处出现了新的吸收峰,表明高碘酸钠成功氧化了针叶木纤维,使其具有了更多的醛基;纤维素基希夫碱配体 (DAC-Gly)和纤维素基希夫碱铜配合物 (DAC-Gly-Cu)在1650 cm-1附近都出现了吸收峰,表明希夫碱反应成功进行,并且DAC-Gly-Cu 在 543 cm-1和 460 cm-1处都出现新的吸收峰,表明Cu2+成功地固载在DAC-Gly上。另外,与DAC-Gly相比,DAC-Gly-Cu的紫外光吸收峰均发生了较明显的红移;XRD结果表明,DACGly-Cu 在 2θ=9.4°、18.9°、28.5°处出现了新的衍射峰。这表明对针叶木纤维成功进行了希夫碱改性,制备了新型的抗菌材料。
3.2 对大肠杆菌的抗菌实验结果表明,针叶木纤维周围没有抑菌圈,浸渍乙酸铜的纤维周围出现了较小的抑菌圈,其宽度为1.095 mm,而DAC-Gly和DACGly-Cu周围抑菌圈宽度分别为9.06 mm、17.74 mm,表明 DAC-Gly和DAC-Gly-Cu都具有抗菌性,且 DACGly-Cu的抗菌性能更优。

