超临界流体吸附法制备负载化离子液体[Bmim][BF4]@SBA−15
甄梦媛,李卓剑,徐琴琴,詹华书,银建中
1. 大连理工大学 化工机械与安全学院,辽宁 大连 116024 2. 超临界流体技术与装备国家地方联合工程中心,贵州 遵义 563003
离子液体(ionic liquids, ILs)是一种在室温或接近室温下,呈液体状态的通常完全由有机阳离子和有机或无机阴离子组合而成的物质[1],其优良性能可用作分离或反应中。但因其黏度大、价格高等缺点无法实现广泛应用。因此许多研究学者将其负载至多孔材料中形成负载化离子液体(supported ionic liquids, SILs),作为吸附剂[2]或催化剂[3]。本文利用超临界二氧化碳(supercritical carbon dioxide, scCO2) 设 计 超 临 界 流 体 吸 附(supercritical fluid adsorption,SFA)法,将咪唑类离子液体[Bmim][BF4]负载到载体无机介孔氧化硅SBA−15上形成负载化离子液体。
1 研究背景
负载化离子液体的常用制备方法有浸渍法[4]、键合法[5]和溶胶凝胶法[6]。其中浸渍法因适用于不同离子液体和载体且操作简单所以最为常见,常规离子液体[Bmim][Cl][7]、[Bmim][PF6][8]、[Bmim][BF4][9]、[Emim][BF4][10],以及功能化离子液体氨基酸离子液体[apaeP444][AA][11]、含氨基离子液体[12−13]、金属功能化离子液体[14]等都已利用浸渍法实现成功负载以作为催化剂或吸附剂使用。但该方法的分散性较差,且容易堵塞孔道。键合法需要ILs与载体之间有可结合功能团,溶胶凝胶法可在载体制备的同时实现ILs负载,但工艺较为繁琐。为实现均匀可控的IL负载,银建中等[15−17]提出利用超临界二氧化碳制备SILs。
超临界流体(supercritical fluid, SCF)是指当物质同时高于临界压力和临界温度的状态,其具有类似气体的黏度和扩散系数,以及类似液体的密度和溶解能力,因此可作为萃取、反应及合成的有效溶剂。超临界二氧化碳由于其临界条件较为温和(Tc=31.1 °C、Pc=7.38 MPa),不会与载体或ILs反应,在负载完成后较易分离,廉价无污染等特点最常使用作为绿色溶剂。研究结果表明[18],在有机溶剂作为共溶剂的存在下,ILs在scCO2中的溶解度可大幅度提升,借助scCO2无表面张力、无孔不入的特性,负载至多孔材料的孔道内部,得到负载较为均匀的SILs,如图1所示,进而强化其催化或吸附性能。
图1 scCO2 制备 SILs示意
2 实验原料及研究方法
2.1 实验原料
离子液体[Bmim][BF4],纯度99%,购于中科院兰州化学物理研究所;乙醇,分析纯,购于华昊化工有限公司;SBA−15根据文献方法[19]自行合成(比表面积为 707.57 m2/g,孔容为 0.88 cm3/g,平均孔径为 4.97 nm)。
2.2 实验方法
超临界流体吸附法实验装置如图2所示。为本实验室自行设计搭建,气相与液相两路在反应器入口前混合并形成一路进入管式反应器,其容积约为6 mL。具体操作步骤如下:
1)将干燥后的的载体与石英砂按照图3的装填方式在反应器内形成固定床;
2)连通气路,并且将循环水浴调整至所需温度,向反应器中打入高压CO2,使其达到超临界状态;
3)将溶解有一定浓度IL的乙醇溶液通过高压恒流泵以一定流量输送至反应器,打开出口阀至特定流量,并开始计时;
4)保持反应器内压力在所需值,并且注意随时调节出口流量稳定于特定值,实验进行一定时间后结束,缓慢泄压后取出样品,经烘干后称取重量,计算IL负载量。

图2 SFA 法实验装置

图3 SFA 装置中固定床反应器的装填方式
2.3 SILs的表征方法
本文负载量的定义是单位质量载体中所负载IL的质量,称量负载前后载体质量可算得负载量。
采用Q600热重分析仪对负载前后载体以及纯IL进行热重分析,将样品进行干燥12 h除去吸附水分后在Ar氛围下,控制升温速率为10 K/min,测试温度为30~600 °C,根据不同时刻的样品质量绘制热重曲线,计算不同负载量载体的质量变化。
采用 Micromeritics ASAP 2460 2.01 物理吸附仪对样品进行表征。仪器分析可得到样品的比表面积、孔容等特征参数。
3 结果与讨论
3.1 制备条件对负载量的影响
影响SFA制备负载化离子液体的因素主要有IL的浓度、时间、流量、压力和温度等。
3.1.1 IL 浓度对负载量的影响
在实验条件为 200 mg SBA−15、16 MPa、50 °C液相流量 0.4 mL/min、CO2流量 0.8 L/min 时,考察IL/乙醇的浓度分别为 10、15、20 mg/mL,在 0~6 h的负载量,得到结果如图4所示。
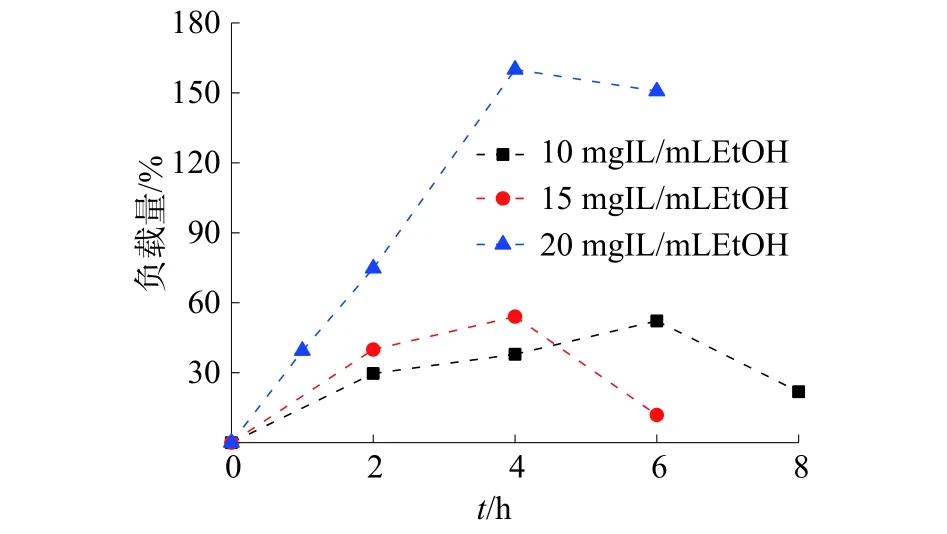
图4 不同 IL/乙醇浓度的时间负载曲线
由图可得,当浓度为10 mg/mL时,负载量随着时间的延长而增长,负载量从2 h的30.90%升至6 h时的54.20%,且负载量随时间的变化呈类似线性增长。这说明在该浓度条件下,气液两相流经载体会有一定浓度的IL与载体结合;当浓度为 15 mg/mL 和 20 mg/mL 时,负载量先随着时间的延长而增加,在时间为4 h时达到负载量的最高点;之后继续延长时间时,负载量不升反降。推测其原因为在流动体系中,IL、乙醇与scCO2三者的作用较为复杂,乙醇的存在可以作为共溶剂提高IL在scCO2中的溶解度,但同时也会使IL因溶解于超临界相在流通过程中随着scCO2与乙醇一同流出体系。当负载时间达到4 h时,在该浓度下已经达到饱和吸附量,继续增加负载时间会使原本与载体表面结合的IL会重新溶解于scCO2与乙醇中,造成IL负载量减小的情况出现。
对比 20 mg/mL与 10 mg/mL的时间负载曲线,可以看出,当IL浓度增加一倍时,相同时间下的负载量增加不止一倍。这说明在浓度较高的条件下,IL更容易与载体结合,要得到相同的负载量需要更少的时间和原料。但当延长时间至4 h及以上时,IL负载量均超过100%,会严重堵塞孔道且覆盖载体表面,此类材料无法发挥多孔材料与IL的协同作用,还会影响材料对CO2的吸附性能,不利于应用。因此在制备时应避免该类现象的出现。
3.1.2 流量对负载量的影响
1)液相流量对负载量的影响
固定其他实验条件为 200 mg SBA−15、16 MPa、50 °C、IL/乙醇浓度 20 mg/mL、CO2流量 0.8 L/min,考察改变液相流量对负载量的变化。
负载量随液相流量的增加而增加,如图5所示。这是因为增加液相流量会增加乙醇在体系中的摩尔分数,同时也会增加进入体系的IL量,两者均可促进IL的负载。

图5 改变液相流量对负载量的影响
2)气相流量对负载量的影响
固定其他实验条件为 200 mg SBA−15、16 MPa、50 °C、IL/乙醇浓度 20 mg/mL、液相流量 0.4 mL/min,考察改变气相流量对负载量的变化。
负载量变化如图6所示。液相流量不变时,相同时间内进入体系的IL绝对量一致;当气相流量增加时,IL与scCO2混合的更为充分,负载量也随之增加;当气相流量为1.2 L/min时,气液体积比为30∶1,负载量已达147.05%,与继续增加气相流量至1.6 L/min的负载量149.70%基本一致,认为已达到饱和吸附量。
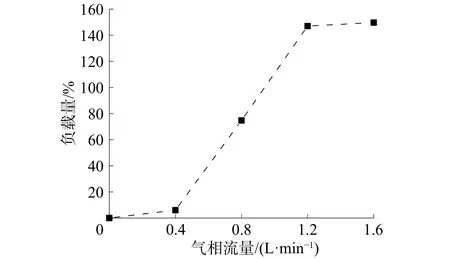
图6 改变气相流量对负载量的影响
3.1.3 压力对负载量的影响
固定实验条件为 200 mg SBA−15、2 h、50 °C、IL/乙 醇 浓 度 20 mg/mL、 液 相 流 量 0.4 mL/min、CO2流量0.8 L/min,考察压力变化对负载量的影响。
负载量随压力的变化如图7所示,可以看出升高压力有利于促进IL的负载。因压力升高,CO2密度增大,有助于IL在scCO2中的溶解,进而增大负载量。16 MPa时负载量为 74.75%;12 MPa的负载量与其相差仅为14.45%;而继续降低压力到9 MPa时,负载量仅为16.95%。从图中可以看出,在其他条件一定时,负载量与CO2密度随着压力的变化呈现相同的趋势。

图7 改变压力对负载量的影响
3.1.4 温度变化
反应温度会影响IL在scCO2中的溶解度和扩散系数,并且改变反应器内CO2的密度。因此需考察温度变化对实验负载量的影响。固定反应条件为:200 mg SBA−15;16 MPa;IL/乙醇浓度20 mg/mL;液相流量 0.4 mL/min;CO2流量 0.8 L/min;改变温度在40~70 °C进行实验。
由图8可以看出:在40~60 °C温度范围内负载量随着时间的延长而增加;而70 °C负载量稍有下降。温度的升高会降低scCO2的密度和IL在scCO2中的溶解度,对负载产生负效果;但同时也会降低IL在反应中的黏度,增大其扩散系数,对负载产生正效果。根据实验结果可以推测,在温度低于 60 °C 时,正作用较强;而高于 60 °C时,负作用较强。
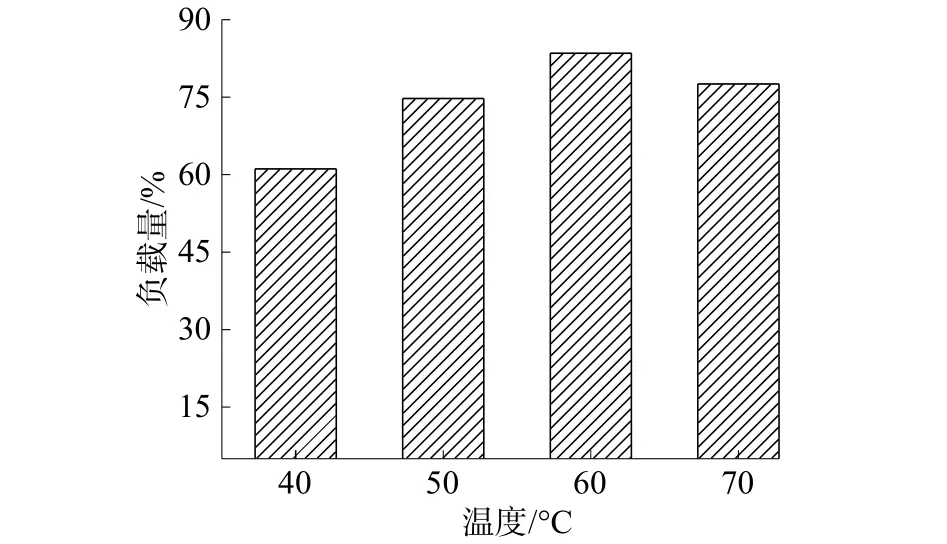
图8 改变温度对负载量的影响
3.2 样品表征
3.2.1 热重分析
对空白样载体、[Bmim][BF4]以及负载负载样品 进 行 热 重 分 析 (thermogravimetric analysis, TG),以判断称量法确定负载量的准确性以及载体与IL的结合程度。如图9所示为对SBA−15、[Bmim][BF4]、scCO2辅助法制备的负载量为76.75%的SILs(命名为SFD−76.75)以及SFA法制备的负载量为 80.85%的SILs(命名为SFA−80.85)的热重分析结果。

图9 不同样品的 TG 结果
由于样品在进行测试之前已进行了充分的干燥处理,故样品中已几乎没有残留水分。由图9可以看出:从室温至600 °C的温度范围内,空白SBA−15基本没有重量损失;烧至600 °C时重量还有99.70%,只有0.30%的失重,推测主要为结合水。SFD−76.75与SFA−80.85样品的失重与纯IL类似,在300 °C之前几乎没有失重,说明负载至载体的IL保持了自身的热稳定性;350 °C开始失重至分解完全时失重率为46.01%与48.19%。该样品经称量计算的负载率分别为76.75%和80.85,故其理论失重分别为43.42%和44.71%,除去0.30%的载体结合水,与称量结果的误差仅为2.29%与3.18%,证明了称量法的可靠性。
3.2.2 N2吸附
1)SFA实验样品N2吸附等温线
从图10可得,SFA法制备所得SILs与空白样的吸附−脱附等温线为标准的IV型曲线。在P/P0介于0.5~0.8时,曲线出现明显的滞后环,说明材料均具有介孔结构。从表1数据可得,SILs的比表面积和孔容上随负载量的增加而减少,因其孔道内部逐渐被IL填满。

图10 SFA 实验样品 N2 吸附等温线

表1 SFA 法制备样品孔道特征参数(2 h,50 °C)
2)与本组前实验方法对比
表2为选取不同制备方法所得样品的N2吸附对比结果。利用传统浸渍法制备负载量为50.30%的[Bmim][BF4]@SBA−15(命名为 IMP−50.30)时,比表面积仅为36.00 m2/g,占空白样载体的4.36%(因不同批次实验所用载体的孔道参数略有差异,故使用样品与空白样载体的参数比例作对比,下同),孔容仅剩6.67%。而使用另外2种方法制备得到的样品在更高的负载量下,仍能保持更高的孔道参数。对比静态的scCO2辅助法制备的样品与本文动态SFA法制备的样品,二者负载量相当,但SFA法制备样品可以保持空白样13.45%的比表面积以及23.68%的孔容,略高于scCO2辅助法的10.10%与18.68%。可以认为,利用scCO2制备SILs可以改善SILs的孔道特性,其中SFA法效果略优于scCO2辅助法。
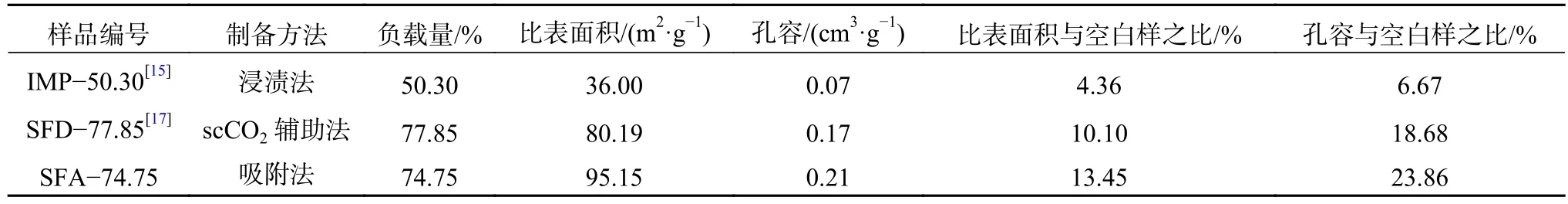
表2 不同方法制备样品孔道特征参数
3.3 SBA-15 与 IL 的相互作用
SBA−15的表面与孔道内部具有均匀分布的硅醇键(Si−O−H),作为官能团可以与其他可反应的化学键结合。除范德华力的物理作用之外,硅醇键倾向于失去电子,故易与IL的阳离子形成库仑力的相互作用,有助于IL的负载。
4 结论
为制备负载量可控以及保持载体孔道的负载化离子液体,利用scCO2的无孔不入的特性,在乙醇作为共溶剂条件下,采用SFA法成功制备负载化离子液体[Bmim][BF4]@SBA−15。1)实验结果表明,流量与时间为SFA法影响较为显著的因素;2)最佳实验条件为:IL/乙醇浓度 20 mg/mL、液相流量 0.4 mL/min、CO2流量 0.8 L/min、2 h、60 °C、16 MPa,负载量达 83.50%;3)在负载量相当时,SFA法制备样品相较于浸渍法以及scCO2辅助法具有更优良的孔道性能,更有利于作为吸附剂或催化剂使用。

