可见光催化剂钒酸铋的可控合成及性能研究
李杰, 宋晨飞, 逄显娟
可见光催化剂钒酸铋的可控合成及性能研究
李杰1, 宋晨飞2, 逄显娟2
(河南科技大学1. 医学院; 2. 高端轴承摩擦学技术与应用国家地方联合工程实验室, 洛阳 471023)
采用微波水热法, 以BiVO3·5H2O和NH4VO3为原料, 通过调控前驱液pH可控合成了不同晶体结构的可见光催化剂BiVO4。利用X射线衍射(XRD)、紫外–可见漫反射(UV-Vis)、拉曼光谱(Raman)和场放射扫描电镜(SEM)等手段对所制备的样品进行了表征和分析, 探讨了不同晶体结构BiVO4的形成机理; 同时以亚甲基蓝和一氧化氮为降解对象, 考察了样品的光催化性能。结果表明, 当前驱液pH为3~5时, 制备的BiVO4为四方锆石结构(z-t), 形貌为微米球; 前驱液pH小于2或大于7时, 制备的BiVO4为单斜白钨矿结构(s-m), 形貌为多面体。这可能是由于前驱液pH的变化, 致使前驱液中钒酸根离子和铋离子的存在形式发生了转变, 进而影响BiVO4的形成历程, 使得BiVO4样品的晶体结构、形貌、晶面裸露以及VO4四面体等发生了改变。光催化试验结果表明, BiVO4(s-m)光催化活性优于BiVO4(s-t)。当前驱液pH为9时, 制备的BiVO4(s-m)样品由于结晶度高、 (040)晶面暴露率高和VO4四面体畸变程度大, 表现出优异的光催化活性。
BiVO4; 微波水热; 可控合成; 光催化
钒酸铋(BiVO4)是一种可见光催化材料, 具有化学稳定性好、太阳光利用率高和无毒等特点, 引起了广泛关注。BiVO4主要有三种晶体结构, 即四方锆石结构(z-t)、单斜白钨矿结构(s-m)和单斜四方结构(s-t), 其中BiVO4(z-t)属于低温相, 经过670~770 K热处理会不可逆地转变为BiVO4(s-m), BiVO4(s-t)和BiVO4(s-m)可在528 K下互相转变。不同晶体结构的BiVO4表现出不同的光催化性能, 研究表明BiVO4(s-m)中Bi-O多面体畸变程度高于BiVO4(z-t), 有利于光生电子–空穴对的产生与分离, 显示出更高的可见光催化活性[1]。因此, 如何控制优化合成方法, 实现不同晶体结构的可控制备, 是当前研究BiVO4可见光催化剂的一个重要方向。
目前可控合成不同晶体结构的BiVO4的方法主要有液相法[2]、微波法[3]、沉淀法[4]、水热法[5-6]和微乳法[7], 但上述制备方法存在反应时间长, 煅烧温度高, 或者原材料和有机溶剂昂贵等不足。因此, 有必要寻找一种简易快捷、条件温和的制备方法来可控合成不同晶体结构的BiVO4。
微波水热法采用微波进行加热, 可以实现分子水平的加热和振动。并与水热法相结合, 充分发挥了微波和水热的优势。该方法除了兼具传统水热法的优点外, 还具有加热速度快、加热均匀、无滞后效应等特点, 可以在短时间内快速高效地制备纯相且粒径完整的纳米材料, 是纳米材料合成的一种新方法。目前, 利用微波水热法已成功制备了CdWO4[8]、ZnO[9]、Sn3O4/rGO[10]等多种具有光催化活性且形貌独特的纳米半导体光催化材料, 但采用微波水热法可控合成不同晶体结构的BiVO4还鲜见报道。为此, 本工作采用微波水热法, 通过调控前驱液的pH, 可控合成了不同晶体结构的BiVO4, 初步探讨了不同晶体结构BiVO4的形成进程, 借助XRD、SEM和UV-Vis DRS等表征技术对样品进行了分析, 并以亚甲基蓝(MB)和一氧化氮(NO)的降解性能评价分析了样品的光催化性能。
1 实验方法
1.1 主要试剂与仪器
试剂: 五水硝酸铋、偏钒酸铵购于国药集团化学试剂有限公司; 氢氧化钠、无水乙醇购于天津巴斯夫分析试剂有限公司, 所有试剂均为分析纯。实验用水均由Milli-Q3 UV-R超纯水系统制得。
仪器: 电子分析天平(德国Sartorius); Ethos TC微波仪(意大利Milestone Inc); D8 Advance X射线粉末衍射仪(德国Bruker; Cu靶Kα辐射=0.154 nm, 扫描范围2=10°~50°); JSM6700F扫描电子显微镜(日本JUL 公司); Escalb MK-II型X射线光电子能谱仪(美国Thermo-VG Scientific公司); Cary 500 UV-Vis-NIR分光光度计(美国Varian 公司, BaSO4为标准参比样品); 5415D高速离心机(德国Eppendorf公司); ASAP2020全自动物理化学吸附仪(美国Micromeritics公司); NEXUS 670傅立叶变换红外光谱仪(美国Thermo Nicolet公司); In Via Reflex激光拉曼光谱仪(英国Renishaw公司); 42I型氮氧化合物分析仪(美国Thermo Environmental公司)。
1.2 微波水热法制备钒酸铋
称取5 mmol硝酸铋溶于35 mL去离子水中, 称取5 mmol的偏钒酸铵加热溶解于35 mL去离子水中; 然后将偏钒酸铵水溶液滴加到硝酸铋溶液中, 得到黄色前驱液, 超声混合45 min, 然后继续磁力搅拌30 min后, 用精密pH试纸检测前驱液pH约为0.5, 然后用10 mol/L的NaOH溶液调节前驱液pH为1、2、3、5、6、7、9、11、13, 最后将前驱液置于100 mL微波仪反应器中, 在180 ℃下微波水热反应4 h。反应结束后, 自然冷却至室温, 离心, 用去离子水和无水乙醇洗涤3次, 80 ℃真空烘干, 得到产物。
1.3 光催化性能测试
光催化装置示意图见图1(a), 以1×10–5mol/L 的亚甲基溶液(MB)为模拟污染物, 在100 mL的反应器中加入80 mL的MB溶液和80 mg催化剂样品, 磁力搅拌使之悬浮。采用300 W金属卤钨灯为可见光源, 置于双层玻璃夹套(通冷凝水), 灯距上液面10 cm, 使用滤光片和饱和乙酸铜溶液滤掉紫外光和波长大于580 nm的光, 保证在400 nm<< 580 nm的可见光下进行光催化降解实验, 透射光谱见图1(b)。光催化降解过程中, 先避光搅拌3 h, 使反应物在催化剂的表面建立吸附–脱附平衡, 然后开启光源进行光催化反应, 每隔60 min取样, 10000 r/min离心分离后, 用紫外–可见分光光度计检测MB吸光度, 通过吸光度计算MB的降解率。

图1 光催化反应装置示意图(a)和组合滤光片的透射光谱(b)
1: Cylindrical pyrex vessel; 2: Tungsten halogen lamp; 3: Cutoff filter; 4: Reactor; 5: Saturated cupric acetate solution; 6: Petri dish
在上述光催化性能测试的基础上, 以NO为目标物进一步考察样品的光催化性能。光催化降解NO试验在敞口的不锈钢反应器中进行, 容积为4.5 L (30 cm×15 cm×10 cm), 敞口部分用石英玻璃密封, 上方30 cm处为300 W卤钨灯, 400和800 nm双滤光片使入射光波长在400~800 nm之间。称取0.4 g样品超声分散于100 mL去离子水中, 超声分散15 min后, 转移至两个玻璃皿中(直径12 cm), 60 ℃真空干燥, 然后置于反应器中避光放置。两个质量控制器分别调控NO标准气体(5 mg/L, N2平衡)和零空气的流速为150和1.35 L/min, 混合后气体中的NO浓度约为500 μg/L。混合气通过反应器后, 一部分排空, 一部分进入NO分析仪(流速为700 mL/min)检测NO浓度, 每隔1 min检测一次。待吸附平衡后, 打开光源, 进行光催化降解实验。
2 结果与讨论
2.1 物相分析
图2是不同pH条件下合成BiVO4样品的XRD图谱, 从图中可以看出, 前驱液的pH对钒酸铋的晶体结构有很大影响。如图所示, 在强酸、中性和碱性条件下合成的样品在(110)、(011)、(121)、(040)、(200)、(002)、(141)、(211)、(051)、(060)、(240)和(042)晶面处出现了较强的衍射峰, 与BiVO4标准卡片JCPDS 14-0688相吻合, 为单斜晶系结构的BiVO4。在中强酸条件下合成的样品在(101)、(200)、(211)、(112)、(220)、(301)、(103)、(321)和(312)晶面处出现了较强的衍射峰, 与BiVO4标准卡片JCPDS 14-0133相吻合, 为四方晶系结构的BiVO4。由上述结果可知, 通过调控前驱液pH可控合成了不同晶体结构的BiVO4, 这是由于Bi3+和VO3–的存在形态与前驱液的pH密切相关。在强酸条件下(pH<2), Bi3+主要以微溶的BiO+形态存在, VO3–主要以VO2+的形式存在, BiVO4的生成过程可能按以下反应式进行[11]:

图2 不同pH条件下制备的BiVO4样品的XRD图谱
Bi3++ H2O↔Bi(OH)2++ H+↔Bi(OH)2++ 2H+(1)
NO3–+ Bi(OH)2+→BiONO3↓+ H2O (2)
VO3–+ 2H+↔ VO2++ H2O (3)
BiONO3+ VO2++ 2H2O→BiVO4↓+ NO3–+ 2H+(4)
在强酸环境下, H+浓度高, 抑制了铋离子的水解, 有利于反应(1)向左进行, 因此只有少量微溶的BiONO3生成, 导致产物BiVO4的量较少, 由于BiVO4(s-m)的稳定性要优于BiVO4(z-t), 因此生成的BiVO4为单斜白钨矿结构。当前驱液的pH为中强酸时(pH为3~5), Bi3+仍以微溶的BiO+形态存在, 而VO3–聚合为V10O286–, 在BiVO4的形成过程中, 多聚钒酸盐分解成VO3–后与BiONO3反应生成BiVO4[2], 推测BiVO4的生成按以下反应式进行:
10VO3–+ 4H+↔ V10O286–+ 2H2O(5)
BiONO3+ VO3–→BiVO4↓+ NO3–(6)
在反应过程中, 由于BiVO4的生成, 使得溶液中VO3–的浓度降低, 为维持反应(5)的平衡, 促使反应(5)向左进行。研究表明BiVO4(z-t)是BiVO4(s-m)生成过程中的中间产物, 通过延长反应时间使BiVO4(z-t)转变为BiVO4(s-m)[12], 因此可能是由于微波水热反应时间不足, 导致生成的BiVO4具有四方锆石结构。当前驱液pH为6~7时, 钒离子主要以VO3–的形式存在, 反应按照(1)、(2)和(6)进行反应[13], 从图3可以看出, pH为6时制备的样品主要为BiVO4(s-m), 同时还残留一些BiVO4(z-t); pH为7时制备的样品为纯相BiVO4(s-m)。pH的升高促进BiVO4(z-t)向BiVO4(s-m)转变, 继续升高前驱液的pH至9~13时, Bi3+与OH–反应形成难溶的Bi(OH)3, VO3–聚合为[V2O6.OH]3–, BiVO4的形成可能按下式进行:
Bi3++ 3OH–→Bi(OH)3↓ (7)
2VO3–+ OH–↔ [V2O6.OH]3–(8)
Bi(OH)3+ VO3–→BiVO4+ OH–+ H2O (9)
在碱性条件下, 由于OH–的矿化能力较强, 会迫使生成的BiVO4(z-t)以溶解–重结晶的方式[14]转变为稳定的BiVO4(s-m)。
图3是不同pH条件下制备BiVO4(s-m)的局部图, 从图中可以看出, 随着pH升高, BiVO4(s-m)的(040)与(121)晶面的衍射峰强度比值(040/121)呈先升高后降低的趋势, pH为9时制备样品的040/121达到极大值, 且远大于标准卡片中(040)衍射峰的相对强度, 说明样品沿着{010}方向择优生长[15]。由金属氧化物的酸碱表面性质可知, 前驱液pH的变化会使沉淀表面的质子浓度发生改变, 进而改变系统界面张力。pH增大, 使得(040)晶面的表面自由能增加, 沿该晶面排布的规整性增强, 因此该晶面的衍射峰强度增大, 当pH为9时制备样品的040/121达到极大值。但是, 氢氧化钠具有平衡不同晶面生长速率, 减小晶面间表面自由能差异的作用, 因此, 当前驱液pH超过9后, 样品的(040)晶面衍射峰的相对强度逐渐减小[16-17]。
2.2 钒酸铋样品的光学性质
光吸收是光催化反应过程的第一步, 也是影响材料光催化活性的重要因素之一。图4是不同pH条件下制备的BiVO4(z-t)和BiVO4(s-m)样品的紫外–可见漫反射光谱图, 从图中可以看出, BiVO4(z-t)和BiVO4(s-m)在可见光区有陡峭的吸收边, 说明样品在可见光区的吸收光谱带是由带隙跃迁引起的, 而不是由杂质能级跃迁引起的[18-19]。前驱液pH为1、2、7、9、11和13时所制备的BiVO4(s-m)样品具有相似的吸收光谱, 利用外切法可得BiVO4(s-m)样品的吸收边分别为513、510、507、505、508和511 nm(图4插图), 吸收边与(040)和(121)晶面的相对强度呈现一定的规律性, 相对强度越大, 吸收边越向短波长方向移动(蓝移)。根据公式g=1240/, 估算出不同pH条件下制备的纯相BiVO4的禁带宽度分别为: 2.42、2.43、2.88、2.83、2.45、2.46、2.44和2.43 eV, 与文献[20]报道基本一致。根据密度泛函理论对BiVO4电子结构计算的结果可知, BiVO4(z-t)的吸收带是电子从O2p 轨道(价带)向V3d 轨道(导带)跃迁产生的, 而BiVO4(s-m)的吸收带是电子从Bi6s 和O2p 所形成的杂化轨道(价带)向V3d 轨道(导带)跃迁产生的, 杂化轨道的形成使价带范围变宽, 禁带变小。因此, BiVO4(s-m)的禁带宽度小于BiVO4(z-t)。纯相的BiVO4(s-m)的禁带宽度存在细微的差别, 这可能是由于不同pH条件致使各样品间的电子结构存在细微差别[17]。
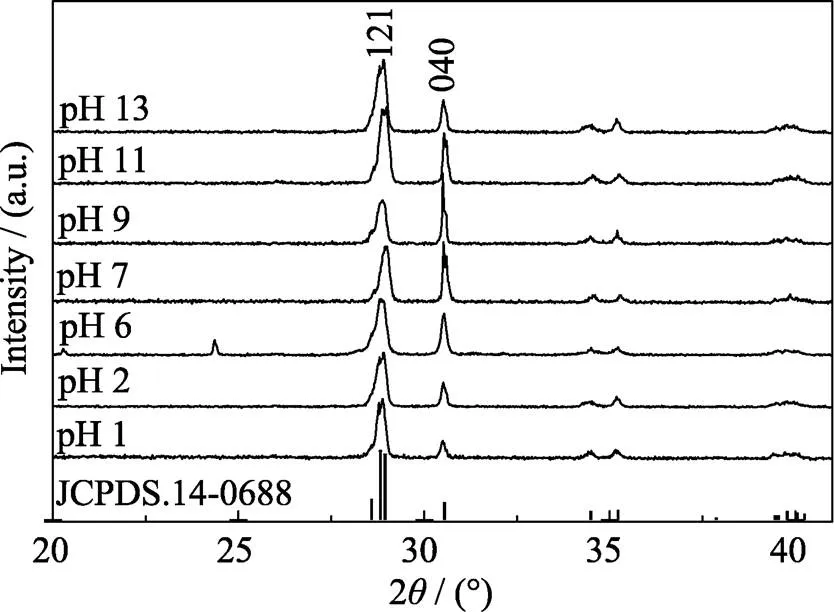
图3 BiVO4(s-m)样品的局部XRD图谱

图4 不同pH条件制备的纯相BiVO4漫反射(DRS)谱图
2.3 钒酸铋样品的FT-IR和Raman分析
图5是不同pH条件下制备BiVO4(s-m)的红外光谱和拉曼光谱。由图5(a)可知, 样品在~733 cm–1处出现BiVO4(s-m)的特征吸收峰, 对应于VO4中V–O键的反对称伸缩振动, 随着pH升高, 先蓝移后红移, 说明钒原子周围的化学环境发生了改变。图5(b)是BiVO4(s-m)样品的拉曼谱图, 所有样品在210、325、365、710和829 cm–1处出现了BiVO4(s-m)的特征峰[21], 其中210 cm–1峰是VO4基团中V–O键的自旋和频移产生的外模, 该峰几乎不提供结构信息; 325和365 cm–1处的峰是VO4基团中V–O的不对称伸缩振动模和弯曲振动模; 710和829 cm–1处的峰是V–O键的反对称伸缩模和对称伸缩模[22]。根据拉曼频移和金属–氧原子的结构关系(cm–1)=21、349 exp (–1.917 6)和(V–O)={0.291 2ln (21, 349/ν)}–5.1计算BiVO4(s-m)中的V–O键长和V的价态, 并利用高斯峰值函数对样品在829 cm–1处的拉曼峰进行拟合, 计算半峰宽, 结果见表1。
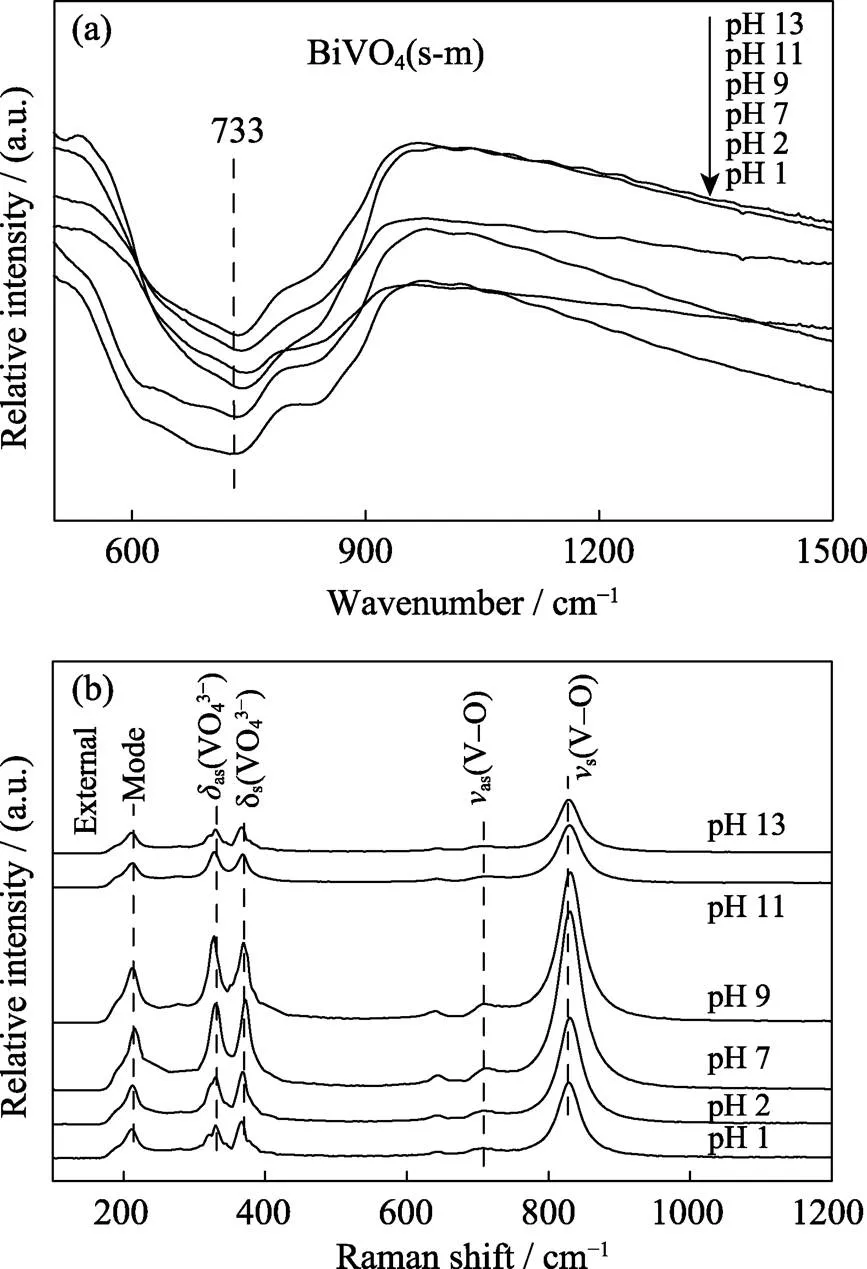
图5 不同pH条件下制备的BiVO4 (s-m)的红外光谱(a)和拉曼光谱(b)
由表1的计算结果可知, BiVO4(s-m)中含有两种V–O键(1和2), 键长大约为0.169和0.177 nm , 与文献报道相符。但随着pH升高, V–O键的键长有细微差别, 呈先减小后增加的趋势。键长的变化说明在BiVO4(s-m)晶粒生长过程中VO4四面体发生了不同程度的畸变。根据反对称和对称伸缩模V–O键的拉曼频移, 得到Pauling价态的V–O键长(V–O), 按照V(价态)=3×1+2公式可计算出BiVO4(s-m)中V原子的价态。由表1可知VO4四面体中V原子的价态都略高于+5价, 这主要是由于Bi3+的孤对电子偏移引起的, 根据文献报道, 计算的V原子价态越高, Bi3+中的偏移程度越大, 同时VO4四面体的畸变程度就越高[23]。半峰宽与晶体的结晶度和几何形貌有关, 半峰宽越大, 样品的结晶度越高, 几何形貌越规整[13,24]。结合表1的计算结果, 前驱液pH为9时制备BiVO4(s-m)样品的VO4四面体畸变程度最大, 结晶度最高、几何形貌最为规整。
2.4 钒酸铋样品的形貌和比表面积分析
图6是不同pH条件下制备的纯相BiVO4的SEM照片, 从图中可以看出四方相和单斜相的BiVO4在形貌上有很大的区别: BiVO4(z-t)主要由大小不一、表面粗糙的球形颗粒组成; BiVO4(s-m)主要由表面光滑的多面体组成。对于BiVO4(s-m), 当pH为1~2时, 样品由诸多表面光滑的多面体团聚在一起组成, 随着pH升高, 样品的粒径呈现逐渐减小的趋势, 样品呈现表面光滑、大小较均匀、具有高晶面暴露度的多面体形貌。当pH为9时, 样品晶面暴露最为完全和完整; 继续升高pH, 裸露的晶面开始遭到破坏; pH为13时, BiVO4(s-m)转变为无规则的纳米颗粒, 这与Raman的分析结果一致。同时, 对pH为9时制备的样品进行高分辨电镜分析, 从图中可以看到清晰的晶格条纹, 测得晶面间距为0.291 nm, 与BiVO4(s-m)中的(040)晶面相吻合[25], 与XRD的表征结果相一致。
比表面积是影响光催化剂活性的一个重要因素, 实验采用氮气低温吸附的方法测试了样品的比表面积, 分别为0.10(pH 1)、0.13(pH 2)、0.07(pH 3)、0.83(pH 5)、0.46(pH 7)、0.72(pH 9)、0.65(pH 11)、0.80 m2/g(pH 13)。从测试结果可以看出, 制备样品的比表面积都很小, 不会对样品的光催化性能产生显著影响。

表1 BiVO4(s-m)的拉曼峰位置及V–O键长和半峰宽

图6 不同pH条件下制备的BiVO4样品的SEM和HRTEM(pH=9)照片
2.5 钒酸铋样品的光电子能谱分析
在BiVO4中, 铋和钒均为变价元素。采用光电子能谱(XPS)对BiVO4(s-m)样品进行分析, 结果如图7所示。图7(a)是V离子的高分辨谱图, 图中V2p由两个能谱峰组成, 结合能分别位于516.5和524.4 eV左右, 对应于V2p3/2和V2p1/2的自旋–轨道分裂峰, 图7(b)是Bi离子的高分辨XPS谱图, 可以看出Bi4f由两个峰组成, 结合能分别位于158.8和164.1 eV左右, 对应于Bi4f 7/2和Bi4f 5/2的自旋–轨道分裂峰, 上述结果说明样品中的Bi离子和V离子分别以+3价和+5价存在, 同时V2p和Bi4f的结合能随着pH增大, 逐渐向高结合能方向偏移, pH为9时, 结合能达到极大值, 随后向低结合能方向偏移。这是由于随着pH升高, 样品中钒离子价态发生了变化, 从Raman的分析结果可知钒离子的价态表现为先升高后降低, 价态的变化使得钒离子的结合能先升高后降低。钒离子的价态与铋离子的孤对电子偏移程度呈正相关, 孤对电子的偏移使得铋离子周围电子云密度发生了改变, 偏移程度越大, 电子云密度就越小, 铋离子的结合能就越大, 反之亦然。因此, 铋离子的结合能先升高后降低。图7(c)是O1s的高分辨谱图, 结合能位于529.6 eV左右, 对应于BiVO4(s-m)中的晶格氧, 随着pH升高, O1s的结合能向高结合能方向移动, 这主要是由样品表面吸附氧含量增加引起的[26]。
2.6 光催化性能分析
图8为MB在BiVO4(s-m) (pH 9)光催化剂作用下的光谱变化, 从图中可以看出, 在可见光照射下, MB溶液的吸光度逐渐降低, 伴随着光催化反应的进行, MB的最大吸收峰从664 nm逐渐向短波长方向移动。这主要是由于MB在光催化降解过程中发生了脱甲基现象, 分别以天青B、天青A和天青C的形式存在[27]。
图9是在不同pH条件制备样品的光催化活性曲线, 由图可知, 不加光催化剂, 仅在可见光照射下, MB溶液无自降解现象。在催化剂存在的条件下, 进行光照, MB溶液开始降解。从图中可知, BiVO4(s-m)的光催化活性要优于BiVO4(z-t), 这是由于BiVO4(z-t)的吸收带主要在紫外光区, 而BiVO4(s-m)除在紫外光区有吸收外, 在可见光区也有明显吸收带, 对可见光的利用率要优于BiVO4(z-t)。另外, BiVO4(s-m)中的Bi-O多面体畸变程度要高于BiVO4(z-t)中的Bi-O多面体, 这种畸变促进了光生电子和空穴对的产生与分离, 使得BiVO4(s-m)表现出较高的可见光催化活性[28]。

图7 不同pH条件下BiVO4(s-m)样品的XPS能谱图

图8 BiVO4(pH 9)样品降解MB的紫外–可见吸收光谱随时间的变化
对于相同晶体结构的BiVO4(s-m), 其光催化活性也表现出明显的差异性。从图9中可以看出, 随着前驱液pH的升高, BiVO4(s-m)的光催化活性先升高后降低, pH为9时制备样品的可见光催化活性最高。XRD和SEM的表征结果显示, pH为9时, 制备的BiVO4(s-m)样品结晶度最高, 晶粒生长最为规整, 可显著改善光生电子和空穴对分离效率和迁移速率, 使得光生电子和空穴能够快速地从体相跃迁到表面, 加快光催化反应进程[29]。同时, DRS的结果表明, pH为9时制备样品的吸收边出现了明显的蓝移现象, 结合FT-IR、Raman、SEM的表征结果可知, 这种现象不是由量子尺寸效应造成的, 而是由于前驱液pH的不同导致BiVO4(s-m)中的V–O四面体发生了不同程度的畸变[21], pH为9时制备样品的畸变程度最高, 促进了光生电子和空穴的分离, 提高了BiVO4(s-m)的光催化活性。此外, XRD、SEM、HRTEM以及Raman的结果表明, pH为9时制备的BiVO4(s-m)样品的(040)晶面的裸露率最高, 晶面生长得最为完整, 研究表明(040)晶面是BiVO4(s-m)的高活性晶面, 该晶面的裸露有利于光生电子和空穴的分离和迁移, 从而提高其光催化活性[30-31]。

图9 不同pH下合成BiVO4样品的光催化性能
2.7 光催化剂稳定性试验
催化剂的稳定性是衡量其是否具有一定科研价值和实际应用价值的重要指标, 因此对BiVO4(pH 9)样品进行了稳定性试验。每次光催化活性试验结束后, 离心分离, 回收样品, 添加MB溶液, 再重新进行活性评价, 如此循环三次, 结果见图10。通过吸光度计算, 三次MB的降解率分别为84.6%、82.1%和80.6%。活性逐渐降低, 这是由于有机物吸附在催化剂表面, 导致活性中心减少, 使催化剂的活性降低。

图10 BiVO4 (pH 9) 光催化降解MB的稳定性
为了进一步考察样品的光催化性能和拓展催化剂的应用范围, 将BiVO4(pH 9)应用于NO的光催化降解, 结果见图11。由图可知在单独光照条件下, NO的浓度没有发生变化, 能够稳定存在。在光照和催化剂共同存在的条件下, NO的浓度迅速降低, 从图中可以看出BiVO4(pH 9)对NO的光催化降解率大约为10%, 重复三次后, 催化剂没有出现明显的失活现象, 说明该催化剂具有一定的稳定性和可循环利用性。
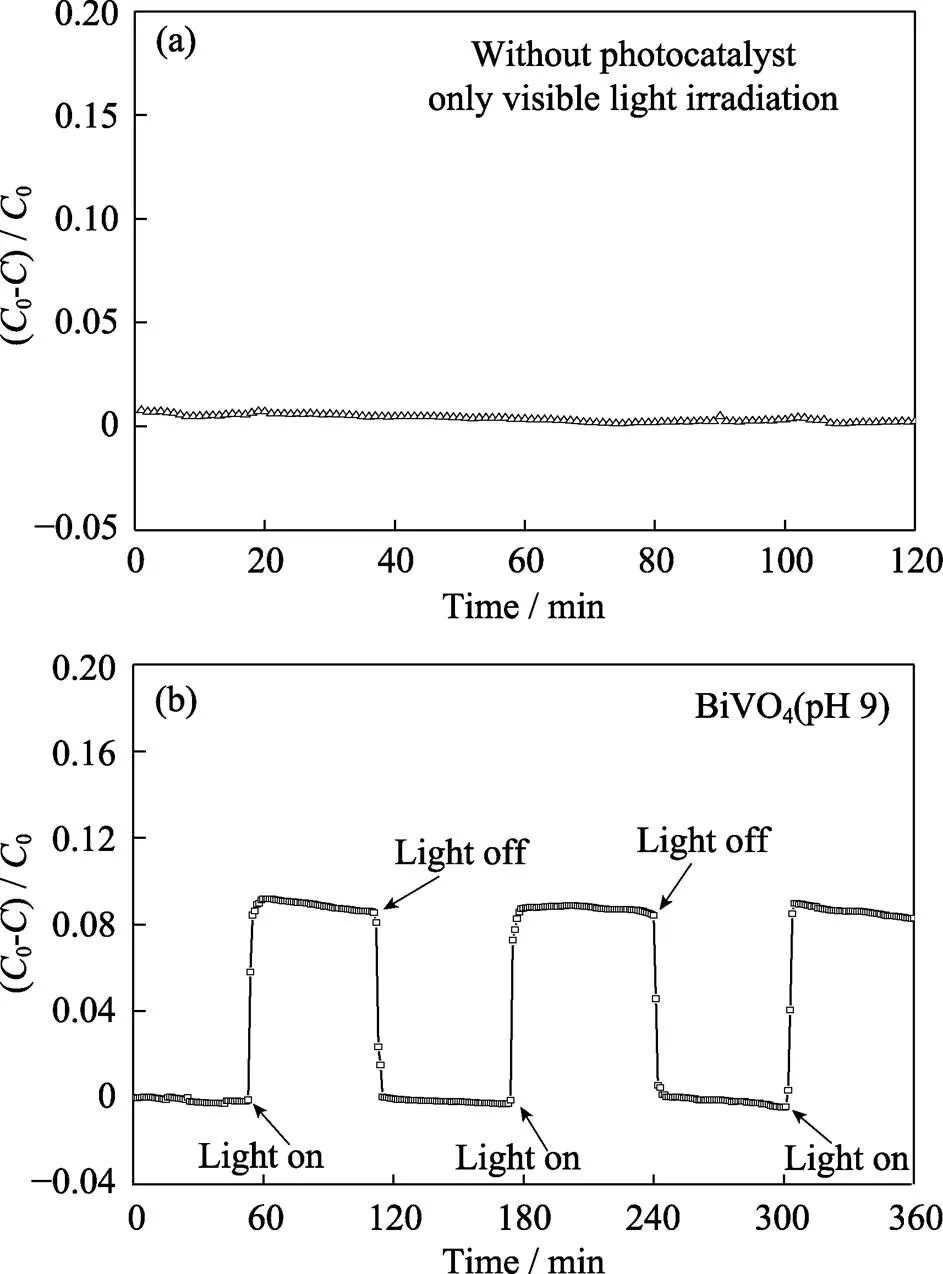
图11 BiVO4光催化降解的NO性能
3 结论
采用微波水热法, 快速可控合成了具有不同晶体结构和形貌的钒酸铋可见光催化剂。结果表明, 前驱液的pH对钒酸铋晶体结构和形貌均有很大的影响, 在pH小于2或pH大于7条件下, 制备的样品为单斜白钨矿结构, 微观形貌呈表面光滑的多面体; 在pH为3~5条件下制备的样品为四方锆石结构, 微观形貌呈大小不一的微米球。光催化活性实验表明, 单斜相结构的钒酸铋具有较高的光催化活性, 其中pH为9时制备样品的光催化活性最佳, 其原因在于该样品的晶粒生长规整、(040)晶面裸露率高和VO4四面体畸变程度大, 有效地促进了光生电子和空穴的分离和迁移, 提高了样品的光催化性能。稳定性实验表明, 催化剂重复使用三次后, 对亚甲基蓝和一氧化氮的降解率分别为80%和10%, 未出现明显的衰减现象, 说明该方法制备的样品具有较好的光催化稳定性。
[1] SHAN L W, MI J B, DONG L M,. Enhanced photocatalytic properties of silver oxide loaded bismuth vanadate., 2014, 22: 909–913.
[2] KUDO A, OMORI K, KATO H. A novel aqueous process for preparation of crystal form-controlled and highly crystalline BiVO4powder from layered vanadates at room temperature and its photocatalytic and photophysical properties., 1999, 121(49): 11459–11467.
[3] PHU N D, HOANG L H, VU P K,. Control of crystal phase of BiVO4nanoparticles synthesized by microwave assisted method., 2016, 27(6): 6452–6456.
[4] GAO S M, QIAO Q A, ZHAO P P,. Synthesis of different morphologies and structures of nano-sized BiVO4by precipitation method., 2007, 23(7): 1153–1157.
[5] KE D N, PENG T Y, MA L,. Effects of hydrothermal temperature on the microstructures of BiVO4and its phtotcatalytic O2evolution activity under visible light., 2009, 48(11): 4685–4691 .
[6] GUO Y N, YANG X, MA F Y,. Additive-free controllable fabrication of bismuth vanadates and their photocatalytic activity toward dye degradation., 2010, 256: 2215–2222.
[7] GE L, ZHANG X H. Synthesis of novel visible light driven BiVO4photocatalystsmicroemulsion process and its photocatalytic performance., 2009, 24(3): 453−456.
[8] HOU L R, LIAN L, ZHANG L H,. Microwave-assisted interfacial hydrothermal fabrication of hydrophobic CdWO4microspheres as a high-performance photocatalyst., 2014, 4(5): 2374–2381.
[9] BYZYNSKI G, PEREIRA A P, VOLANTI D P,. High-performance ultraviolet-visible driven ZnO morphologies photocatalyst obtained by microwave-assisted hydrothermal method., 2018, 353: 358–367.
[10] YU X, ZHAO Z H, SUN D H,. Microwave-assisted hydrothermal synthesis of Sn3O4nanosheet/rGO planar heterostructure for efficient photocatalytic hydrogen generation., 2018, 227(5): 470–476.
[11] PINGMUGANG K, NATTESTAD A, KANGWANSUPAMONKON A,. Phase-controlled microwave synthesis of pure monoclinic BiVO4nanoparticles for photocatalytic dye degradation., 2015, 1: 67–73.
[12] ZHANG H M, LIU J B, WANG H,. Rapid microwave- assisted synthesis of phase controlled BiVO4nanocrystals and research on photocatalytic properties under visible light irradiation., 2008, 10: 767–774.
[13] ZHANG A P, ZHANG J Z, CUI N Y,. Effects of pH on hydrothermal synthesis and characterization of visible-light-driven BiVO4photocatalys., 2009, 304: 28–32.
[14] TOKUNAGA S, KATO H, KUDO A. Selective preparation of monoclinic and tetragonal BiVO4with scheelite structure and their photocatalytic properties., 2001, 13(12): 4624–4628.
[15] XI G C, YE J H. Synthsis of bismuth vanadate nanoplates with exposed {001} facets and enhanced visible-light photocatalytic properties., 2010, 46: 1893–1895.
[16] FAN W L, SONG X Y, BU Y X,. Selective-control hydrothermal synthesis and formation mechanism of monazite-and zircon-type LaVO4nanocrystals., 2006, 110(46): 23247–23254.
[17] GUO J, ZHU Y, ZHANG Y M,. Hydrothermal synthesis and visible-light-photocatalytic properties of BiVO4with different structures and morphologies., 2012, 27(1): 26–32.
[18] KUDO A, TSUJI I, KATO H. AgInZn7S9solid solution photocatalyst for H2evolution from aqueous solutions under visible light irradiation., 2002, 17: 1958–1959.
[19] LI G S, ZHANG D Q, YU J C. Ordered mesoporous BiVO4through nanocating: a superior visible light-driven photoctotalyst., 2008, 20(12): 3983–3992.
[20] JIANG H Y, MENG X, DAI H X,. High-performance porous spherical or octapod-like single-crystalline BiVO4photocatalysts for the removal of phenol and methylene blue under visible-light illumination., 2017, 217-218: 92–99.
[21] YU J Q, KUDO A. Effects of structure variation on the photocatalytic performance of hydrothermal synthesized BiVO4., 2006, 16: 2163–2169.
[22] CHEN Y, ZHOU K C, HUANG S P,. Hydrothermal synthesis and photocatalytic property of BiVO4nanosheets., 2011, 21(7): 1570–1579.
[23] NIKAM S, JOSHI S.Irreversible phase transition in BiVO4nanostructures synthesized by a polyol method and enhancement in photo degradation of methylene blue., 2016, 6: 107463–107474.
[24] ZHANG Y F, GONG H H, ZHANG Y,.The controllably synthesized octadecahedron-BiVO4with exposed {111} facets., 2016, 6: 107463–107474.
[25] SHI W D, YAN Y, YAN X. Microwave-assisted synthesis of nano-scale BiVO4photocatalysts and their excellent visible-light- driven photocatalytic activity for the degradation of ciprofloxacin., 2013, 215-216: 740–746.
[26] OU M, NIE H Y, ZHONG Q,. Controllable synthesis of 3D BiVO4superstructure with visible-light-induced photocatalytic oxidation of NO in gas phase and mechanism analysis., 2015, 17(43): 28809–28817.
[27] PARK H, CHOI W. Photocatalytic reactivities of Nafion-coated TiO2for the degradation of charged organic compounds under UV or visible light., 2005,109(23): 11667–11674.
[28] DONG S Y, YU C F, LI Y K,. Controlled synthesis of T-shaped BiVO4and enhanced visible light responsive photocatalytic activity., 2014, 211: 176–183.
[29] CASTILLO N C, HEEL A, GRAULE T,. Flame-assisted synthesis of nanoscale, amorphous and crystalline, spherical BiVO4with visible-light photocatalytic activity., 2010, 95: 335–347.
[30] THALLURI S M, HUSSAIN M, RUSSO N,. Green- synthesized BiVO4oriented along {040} facets for visible-light- driven ethylene degradation., 2014, 53: 2640–2646.
[31] LI C J, ZHANG P, LV R,. Selective deposition of Ag3PO4on monoclinic BiVO4(040) for highly efficient photocatalysis., 2013, 9(23): 3951–3956.
Controllable Synthesis and Photocatalytic Performance of BiVO4under Visible-light Irradiation
LI Jie1, SONG Chen-Fei2, PANG Xian-Juan2
(1. Medical College, Henan University of Science and Technology, Luoyang 471023, China; 2. National United Engineering Laboratory for Advanced Bearing Tribology, Henan University of Science and Technology, Luoyang 471023, China)
Visible-light-driven photocatalyst BiVO4was synthesizeda facile microwave-hydrothermal method using BiVO3·5H2O and NH4VO3as raw materials. Crystal structure of BiVO4photocatalyst could be selectively controlled to be tetragonal or monoclinic by simply adjusting the pH of the precursor solution. The prepared samples were characterized by XRD, UV-Vis, Raman, and SEM. The mechanism of BiVO4formation with different crystal structures was discussed. Meanwhile, the photocatalytic performances of the prepared sample were evaluated by degradation of methylene blue and photocalytic oxidation of NO gas in air under visible light irradiation. The results showed that BiVO4(z-t) microsphere was obtained when the precursor pH is 3-5, but when the pH is less than 2 or greater than 7, the as-prepared powders are BiVO4(s-m) with polyhedron morphology. This may be due to the change of pH that could form transformation of vanadate and bismuth ion in the precursor solution, and then affect the formation process of BiVO4, resuting in the change of crystal structure, morphology, crystal surface, and VO4tetrahedron of BiVO4(s-m). The photocatalytic tests indicated that the activity of BiVO4(s-m) was much better than that of BiVO4(z-t). The BiVO4(s-m) sample prepared at pH 9 exhibits excellent visible-light photocatalytic activity, because of its higher crystalline, preferentially exposed facts (040), and higher degree distortion of VO43-tetrahedron.
BiVO4; microwave hydrothermal; controllable synthesis; photocatalytic
李杰(1982–), 男, 硕士, 实验师. E-mail: lijie@haust.edu.cn
O643
A
1000-324X(2019)02-0164-09
2018-06-07;
2018-09-17
国家自然科学基金(U1404504);河南省基础与前沿研究计划项目(162300410054) National Nature Science Foundation of China (U1404504); The Project of the Department of Science and Technology of Henan Province (162300410054)
10.15541/jim20180257

