经眶下神经注射ET-1复制三叉神经痛大鼠模型*
曹启旺,徐慧巧
(湖南省人民医院 疼痛科,湖南 长沙 410005)
三叉神经痛是一种临床较常见的神经病理性疼痛,主要特点是患侧三叉神经支配区域出现可触诱发性或自发性的剧烈疼痛。有研究表明,外源性内皮素-1(Endothelin-1, ET-1)可以诱发动物形成短暂且剧烈的痛觉过敏、自发痛等疼痛反应[1-6]。本实验经大鼠眶下神经干注射ET-1,力求复制一种与人类三叉神经痛相接近的动物模型。
1 材料与方法
1.1 材料
1.1.1 实验动物 采用健康清洁级成年雄性SD 大鼠,体重250~300 g,购自长沙天勤生物公司[动物许可证号:SCXK(湘)2014-0011],饲养于湖南省人民医院老年医学研究所动物实验中心。
1.1.2 主要设备与试剂 Von Frey 测痛仪(天津仪数科技),ET-1(美国Sigma公司)溶解在去离子蒸馏水中[7],卡马西平片(100 mg/片,上海三维制药)溶解在生理盐水中。
1.2 方法
1.2.1 动物模型的复制 健康 SD 大鼠术前禁食12 h,自由饮水,称重后用10%水合氯醛(0.3 ml/kg)腹腔注射麻醉,取右侧卧位,固定头部及四肢。右侧颊部颧骨下缘前1/3段脱毛、消毒、铺巾。取1 cm长切口,将皮下组织向触须垫方向钝性分离,在显微镜下找到眶下孔并分离出眶下神经,将针头插入眶下神经干的鞘膜内,用无菌纱条将周围组织与眶下神经隔离,然后注入不同剂量的ET-1溶液或生理盐水,术后缝合切口[8-9]。将术后5 min内苏醒的大鼠纳入本实验。
1.2.2 实验分组 ①实验 1:将 24 只 SD 大鼠随机分为A、B、C 3组,每组8只。A、B组分别经眶下神经注射8和16 nmol ET-1溶液,C组注射10μl生理盐水。观察各组大鼠给药后60 min眶下神经支配区域机械痛阈值和抓脸行为的变化。②实验2:将16只SD大鼠随机分为D、E组,每组8只。D、E组分别喂卡马西平 10 mg/(kg·d)、生理盐水,连续 3 d。然后按实验1的方法复制三叉神经痛模型,观察注射ET-1后60 min大鼠眶下神经支配区域机械痛阈的变化。
1.3 大鼠行为学检测
大鼠在实验前适应环境3 d,术前10 min,以及术后10、20、30、40、50和60 min分别进行行为学测定。采用Von Frey细丝测定大鼠右侧触须垫机械刺激阈值,刺激强度分别为0.5、1.0、2.0、4.0、6.0、8.0、10.0和12.0 g。大鼠出现≥1项表现即判定为阳性反应:①将头面部藏在身下以免受刺激的退缩反应;②连续≥3次搔抓面部刺激区域的抓脸行为;③抓咬刺激物并有攻击动作[10]。由4.0 g开始刺激,如有反应,则用低一级刺激力度的细丝;如没有反应,则加大一级刺激力度的细丝。以此类推,从有反应开始再给3次相同强度的刺激。如用大鼠对最大力度12.0 g的刺激无反应,则痛觉阈值为12.0 g。记录大鼠术后60 min自发性抓脸行为的次数(除外细丝刺激诱发的抓脸行为)。
1.4 统计学方法
数据分析采用SPSS 19.0统计软件。计量资料以均数±标准差(±s)表示,比较用单因素方差分析或重复测量设计的方差分析,两两比较用LSD-t检验,P<0.05为差异有统计学意义。
2 结果
2.1 A、B、C组大鼠术后机械痛阈值和抓脸行为的变化
A、B、C组大鼠右侧触须垫部术后10、20、30、40、50和60 min的机械痛阈值比较,采用重复测量设计的方差分析,结果:①术后不同时间点大鼠右侧触须垫部的机械痛阈值有差别(F=129.455,P=0.000);②3组大鼠术后右侧触须垫部的机械痛阈值有差别(F=41.630,P=0.000),B组较A、C组低,相对痛觉反应敏感性高;③3组大鼠术后右侧触须垫部的机械痛阈值变化趋势有差异(F=34.711,P=0.000)(见表1和图1)。A、B、C组大鼠术后抓脸行为分别为(4.875±0.835)、(8.000±0.756)和(2.625±1.061)次,经单因素方差分析,差异有统计学意义(F=53.127,P=0.000),B组高于A、C组,相对自发性疼痛反应次数多(P<0.05)。经眶下神经注射 16 nmol ET-1 更容易引起大鼠产生三叉神经痛样痛觉过敏和自发性疼痛反应。
2.2 D、E组大鼠术后机械痛阈值和抓脸行为的变化
D、E组大鼠右侧触须垫部术后10、20、30、40、50和60 min的机械痛阈值比较,采用重复测量设计的方差分析,结果:①术后不同时间点大鼠术后右侧触须垫部的机械痛阈值有差别(F=105.367,P=0.000);②两组大鼠术后右侧触须垫部的机械痛阈值有差别(F=32.870,P=0.000),D 组较 E 组高,相对痛觉反应敏感性低;③两组大鼠术后右侧触须垫部的机械痛阈值变化趋势有差别(F=37.249,P=0.000)。卡马西平可较好地抑制三叉神经痛大鼠模型最主要的疼痛行为学改变。见表2和图2。
表1 3组大鼠术后不同时间点机械痛阈值比较 (n =8,g,±s)

表1 3组大鼠术后不同时间点机械痛阈值比较 (n =8,g,±s)
组别 10 min 20 min 30 min 40 min 50 min 60 min A 组 8.50±1.41 7.25±2.12 6.25±1.28 6.50±0.93 7.50±1.41 8.00±1.51 B组 6.50±1.77 5.25±1.83 2.25±1.17 3.00±1.51 4.00±1.51 6.50±1.41 C 组 11.00±1.07 10.75±1.04 10.50±0.93 11.00±1.07 10.75±1.04 11.00±1.07
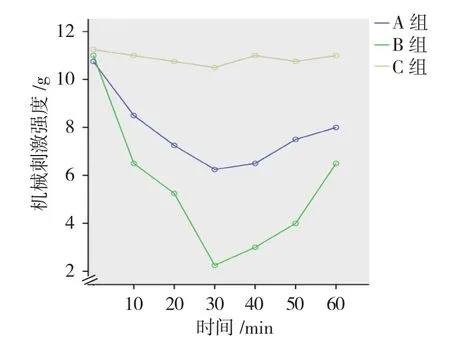
图1 3组大鼠术后机械痛阈值的变化趋势
表2 D、E组大鼠术后不同时间点机械痛阈值比较 (n =8,±s)

表2 D、E组大鼠术后不同时间点机械痛阈值比较 (n =8,±s)
组别 10 min 20 min 30 min 40 min 50 min 60 min D组 9.50±1.41 8.75±1.49 8.25±1.67 9.00±1.51 9.25±1.83 10.00±1.51 E组 6.50±1.77 5.25±1.83 2.25±1.17 3.00±1.51 4.00±1.51 6.50±1.41
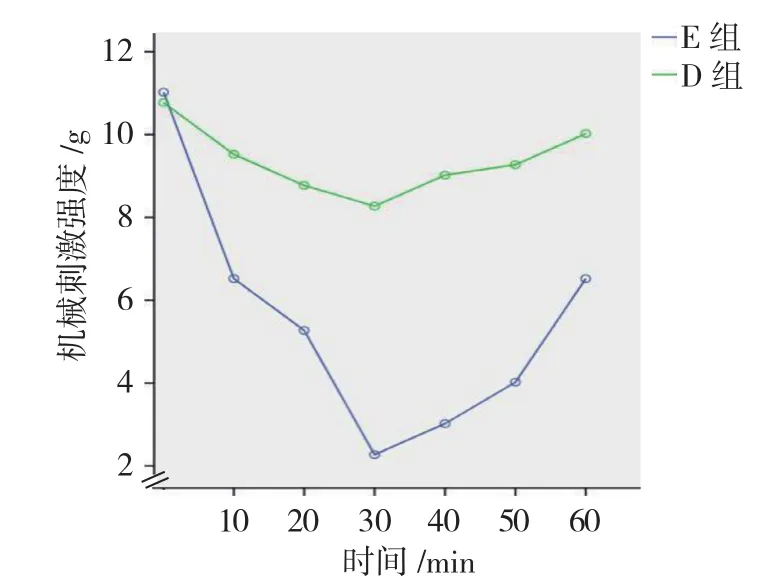
图2 D、E组大鼠术后机械痛阈值的变化趋势
3 讨论
三叉神经痛患者的患侧三叉神经支配区域可出现痛觉过敏、自发痛和触诱发痛等典型神经病理性疼痛症状,痛觉过敏和触诱发痛可因机械或化学刺激而诱发,自发痛则表现为疼痛区域可自发出现阵发性剧痛。临床上,三叉神经痛多因某种诱因作用于三叉神经感觉通路上某一部位而引起。ET-1是一种含有21个氨基酸的强效血管活性肽,作用于外周伤害性感受器的内皮素A受体可引起神经性疼痛痛觉过敏与自发痛[11-13]。本实验经大鼠眶下神经干注射16 nmol ET-1后60 min,大鼠眶下神经支配区域出现机械痛阈值降低(痛觉过敏)和自发性的抓脸行为次数增多(自发痛),笔者推测可能是ET-1使眶下神经感觉神经元内钙离子浓度升高和钠通道电流增强[14-15],增加神经元细胞动作电位产生的频率,使神经元过度兴奋,产生痛觉过敏和自发痛等典型三叉神经痛行为学表现。
卡马西平是临床上治疗三叉神经痛的首选药物,能降低神经细胞膜对钠离子和钙离子的通透性,从而降低神经细胞的兴奋性,延长不应期,抑制神经元的过度兴奋,提高患者的痛阈,降低疼痛强度及发作频率。本实验发现,卡马西平喂药大鼠术后右侧触须垫部对机械刺激的痛敏反应敏感性较对照组降低,说明卡马西平可抑制模型大鼠的触诱发痛和自发痛等典型三叉神经疼痛行为学改变,从另一个角度证明经大鼠眶下神注射ET-1复制三叉神经痛模型的可行性。
综上所述,经眶下神注射ET-1复制三叉神经痛模型是与临床三叉神经痛较接近的动物模型之一,但本模型也存在一定的局限性和不足。首先,本模型更趋向于炎症刺激所引起的三叉神经痛;其次,本模型持续时间太短。相信随着医学工作者对三叉神经痛发病机制认识的深入和实验方法的不断改进,这些缺点都可以克服。

