黄连解毒汤干预胃火炽盛证引起的口腔疾病患者尿液代谢组学研究
中国中医科学院中药研究所 北京 100700
黄连解毒汤原载于《肘后备急方》,由黄连、黄柏、黄芩、栀子组成,被视为清热解毒的代表方,具有泻火解毒之功效,主治一切实热火毒、三焦热盛之证[1]。黄连解毒汤广泛应用于治疗火热炽盛证引起的各系统疾病,是典型的证候类药物。症见大热烦躁、口燥咽干、目赤睛痛、错语不眠,或热病吐血、衄血、便血,甚或发斑、外科痈疽疮疡皆可使用。研究证实,黄连解毒汤在抗炎、抗氧化、抗血栓、降血糖、降血脂、降血压、抗肿瘤,以及保护心血管系统、护肝等方面都应用广泛[2-5]。目前,本课题组的研究评价了黄连解毒汤(颗粒剂)对胃火炽盛证引起的口腔科疾病患者的治疗作用,但是对于黄连解毒汤的具体机制尚不明确。在前期研究的基础上,本实验通过尿液代谢组学方法,利用超高效液相色谱-静电场轨道阱质谱(ultra performance liquid chromatography coupled with orbitrap tandem mass spectrometry,UHPLC-Orbitrap MS)法对胃火炽盛证引起的口腔疾病患者干预前和黄连解毒汤干预后,以及健康对照组的尿液进行分析,区分胃火炽盛证的代谢轮廓并寻找可能的生物标志物,同时初步阐明黄连解毒汤的干预机制。
1 材料和方法
1.1 研究对象 收集2018年1月至8月北京中医药大学第三附属医院、北京中医药大学东方医院和成都中医药大学附属医院口腔科门诊病例。所有患者1年内未接受任何牙周治疗;排除明显错颌畸形患者;排除近3个月有急慢性传染病史或者抗生素服用史的患者。患者根据中医证候和临床表现诊断为复发性口腔溃疡、智齿冠周炎和复发性疱疹性口炎,共计纳入58例,作为口腔疾病患者组(干预前)。相同的58例患者给予黄连解毒汤后作为黄连解毒汤干预组。纳入同时期的口腔健康志愿者10例作为健康对照组,要求全口牙附着无丧失,无牙齿缺损,近3个月无急慢性传染病史或者抗生素服用史。其中对照组男性6例、女性14例,年龄22~58岁,平均(33.30±13.33)岁。口腔疾病患者组男性22例、女性36例,年龄 21~60岁,平均(36.22±13.26)岁;其中复发性口腔溃疡10例、智齿冠周炎26例、复发性疱疹性口炎22例。
1.1.1 诊断标准
1.1.1.1 中医证候诊断标准 智齿冠周炎、复发性口腔溃疡、复发性疱疹性口炎胃火炽盛证诊断标准参照中医临床诊疗术语国家标准(证候部分)[6]、2017年发布的《中医病证诊断疗效标准》[7]《中医证候鉴别诊断学》[8]及《中医诊断学》[9]中胃火炽盛证候分类诊断标准拟定。胃火炽盛证病性(基础证候)辨证标准为:(1)发热(自觉燥热);(2)口渴饮冷;(3)口秽;(4)面红;(5)目赤;(6)大便秘结;(7)小便短黄;(8)舌红苔黄而干;(9)脉数或洪。(1)~(7)中具备两点,同时结合舌脉表现即满足胃火炽盛证病性诊断。
智齿冠周炎(胃火炽盛证)还需满足:(1)牙痛;(2)冠周牙龈红肿或盲袋溢脓。复发性口腔溃疡(胃火炽盛证)还需满足:(1)口疮疼痛,或伴口疮灼烧感;(2)冠周牙龈红肿或盲袋溢脓。复发性疱疹性口炎(胃火炽盛证)还需满足群集小疱,或伴灼痛刺痒。
1.1.1.2 西医疾病诊断标准 智齿冠周炎诊断标准参考“十二五”国家级规划教材《口腔颌面外科学》第7版[10]和《Peterson口腔颌面外科学》第2版[11]中智齿冠周炎的诊断标准拟定;复发性口腔溃疡诊断标准参照《口腔黏膜病学》[12]与《复发性阿弗他溃疡疗效评价试行标准》[13]拟定。复发性疱疹性口炎诊断标准则参考《口腔黏膜病学》[12]与Clinical Oral Medicine and Pathology[14]拟定。
1.1.2 纳入标准 (1)符合胃火炽盛证标准。(2)年龄18~60岁。(3)满足以下条件之一的可以纳入:患者症状符合智齿冠周炎诊断标准,试验开始前未使用过其他药物治疗本病;患者症状符合复发性口腔溃疡(轻型)诊断标准,发病史半年以上,且平均溃疡持续时间5d以上者,本次溃疡发作在48h之内,且未进行治疗;患者症状符合复发性疱疹性口炎诊断标准,本次病程(出现前驱症状、红斑或水疱)在48h之内,且未进行治疗,每年复发1次以上。(4)患者知情同意并签署知情同意书。
1.1.3 排除标准 (1)具有以下情况的智齿冠周炎患者需排除:重度吸烟者(>20支/d);伴有颌面部间隙感染及慢性扩散性冠周炎患者;在智齿冠周炎病灶区域合并牙周病;过去4周内全身应用抗生素。(2)具有以下情况的复发性口腔溃疡患者需排除:过去6个月内有毒品使用史;重度吸烟者(>20支/d);患有已知可能与复发性口腔溃疡有关的疾病,例如:溃疡性结肠炎、白塞病、赖特综合征、免疫缺陷病等;过去4周内全身应用抗生素,3个月内全身使用过皮质激素、免疫抑制剂者;佩戴有可能与溃疡直接接触的正畸固定器或保持器。(3)具有以下情况的复发性疱疹性口炎患者需排除:体温>38.5℃,和(或)外周血 WBC>11.0×109/L,和(或)中性粒细胞比例>85%;过去4周内使用过抗病毒药物或抗生素,过去3个月内进行过免疫抑制或免疫调节治疗。(4)伴严重心、肝肾功能不全等系统性疾病的患者。(5)妊娠期或哺乳期妇女,或当前没有采取有效避孕措施的育龄妇女。(6)对本研究用药过敏,或对含有黄连、黄柏、黄芩、栀子的制剂较为敏感者,如服用后易腹泻或平素为脾胃虚寒体质者。
1.1.4 脱落标准 (1)受试者自行退出;(2)研究者令其退出,如受试者依从性太差、出现夹杂症或发生严重不良事件等。
1.2 仪器 Ultimate 3000超高效液相色谱仪(含自动进样器、柱温箱、在线真空脱气机、低压四元梯度泵、PDA检测器)和LTQ Orbitrap velos pro质谱仪(高分辨静电场轨道阱质谱)均购自美国Thermo Fisher公司;KQ-250B型超声波清洗器购于昆山市超声仪器有限公司;Mix-3000震荡混匀器购于杭州米欧仪器有限公司;Mikro 220R台式高速冷冻离心机购于Hettich公司。
1.3 试药 黄连(Rhizoma Coptidis Franch.,产地为重庆石柱县)、黄芩(Radix Scutellariae Georgi,产地为河北承德围场县)、黄柏(Phellodendri Chinensis C.K.Schneid.,产地为重庆新都县)、栀子(Gardeniae jasminoides J.Ellis,产地为江西省樟树市),均购于北京仟草中药饮片有限公司,经中国中医科学院中药研究所何希荣教授鉴定可用于实验研究。黄连解毒汤配方颗粒(3.2g/袋)由中国中医科学院中药研究所提供(批号:1801001Y)。甲醇、甲酸、乙腈均购于赛默飞世尔科技(中国)有限公司(批号:174486、168642、175160);其它化学品和溶剂均为分析纯。
1.4 方法
1.4.1 黄连解毒汤配方颗粒服用方法 口腔疾病患者组予以黄连解毒汤配方颗粒口服,早晚饭后0.5~1h内以80℃以上热水冲调,1袋/次,2次/d。疗程为5d。
1.4.2 样品处理 健康对照组受试者、口腔疾病患者组(干预前)及黄连解毒汤干预5d后分别于清晨空腹收取尿样。取200μL尿液样本,加600μL乙腈,涡旋混匀,4℃、12 000r/min离心10min,取上清液待测。将3组的所有尿液样本取等量混合均匀后,按照上述样品处理过程处理,所得作为质控(quality control,QC)样品。
1.4.3 色谱条件
1.4.3.1 液相条件 Agilent Extend-C18柱(3.0mm×150mm,3.5μm);柱温:30℃;流动相为 A(乙腈)和 B(0.1%甲酸-水),梯度洗脱 0~10min,5%A;10~15min,5%~15%A;15~25min,15%~50%A;25~30min,50%~95%A;30~36min,95%A。流速 0.3mL·min-1;进样体积3μL。
1.4.3.2 质谱条件 电喷雾离子源(electrospray ion source,ESI)参数设定如下:正负离子扫描模式,正离子模式下毛细管温度为350℃,毛细管电压为35V,喷雾电压为 3.5kV,鞘气(N2)流速为 40psi,辅助气(N2)流速为10psi;负离子模式下毛细管电压为35V,喷雾电压为 3.5kV,鞘气(N2)流速为 35psi,辅助气(N2)流速为10psi。样品一级质谱在FT模式下进行全扫描,分辨率R为30 000,m/z扫描范围为150~1 000,二级及三级质谱采用数据依赖性扫描(data dependent scan)。数据采集和分析采用Xcalibur、Metworks和Mass Frontier 7.0软件。
1.4.4 数据处理 采用 Progenesis QI软件(Nonlinear)对采集的数据进行色谱峰识别、提取、峰对齐和归一化处理,在原始峰表中去除QC样品,测定相对标准偏差(relative standard deviation,RSD)>30%的变量,依据80%规则去除零值,处理原始峰表后,将归一化后的峰表导入SIMCA-P 14.1(Umetrics)数据处理软件,采用主成分分析法(principal component analysis,PCA)和正交偏最小二乘判别分析法(orthogonal partial least squares-discriminant analysis,OPLS-DA)对各组尿液的代谢物进行分析。通过变量重要因子(variable importance in the project,VIP)值(>1)及内源性代谢物在正常组与模型组之间的t检验,筛选与上火相关的潜在生物标志物。根据精确相对分子质量计算分子的不饱和度,结合同位素峰强度及对应的二级离子碎片信息与HMDB(http://www.hmdb.ca/)中的代谢物质谱数据库进行匹配,对可能的潜在标志物进行初步鉴定。
2 结果
2.1 健康对照组、口腔疾病患者组(干预前)和黄连解毒汤干预组尿液LC-MS质谱检测结果 建立UHPLC-Orbitrap MS分析尿液样品的方法,分别在正负离子模式下进行检测分析。分别将所有健康对照组、口腔疾病患者组(干预前)和黄连解毒汤干预组的尿液处理后进行质谱检测,总离子流图见图1。以正离子模式下为例,可见3组尿液的总离子流图存在明显差异,进一步采用PCA和OPLS-DA获得详细的信息。

图1 3组人群在正离子模式下的超高效液相色谱-质谱联用检测总离子流图Fig.1 Total ion current chromatograms for ultra-high performance liquid chromatography-mass spectrometric analysis of urine samples deriving from three groups
2.2 数据分析
2.2.1 PCA 采用PCA统计3组人群代谢物的变化趋势。以正离子模式下为例,QC样品评估PCA得分见图2。相对聚集的QC样品表明,系统重复性好,所采集的数据值得进一步研究。各组之间PCA得分见图3。每个点代表1个样品,每个样品的位置由其成分决定,处于相同病理生理状态的样本通常具有相似的代谢物组成,因此在得分图上也处于相似的位置。相反,彼此之间距离越远表示其病理生理状态相差越大。
2.2.2 差量变异研究 基于健康对照组、口腔疾病患者组(干预前)及黄连解毒汤干预组的PCA分析结果,确定存在代谢差异。以正离子模式下为例,健康对照组、口腔疾病患者组(干预前)及黄连解毒汤干预组样品OPLS-DA得分见图4。健康对照组和口腔疾病患者组(干预前),口腔疾病患者组(干预前)和黄连解毒汤干预组样品的S-plot载荷图及火山图见图5-6。S-plot载荷图中每个点代表样品中代谢物相关信息,距离原点越远的点对两组间区分贡献越大,为两组中差异较大的代谢物。火山图中每个黑色点代表样品中代谢物相关信息,距离原点越远的黑色点对两组间区分贡献越大,可认为是两组中差异较大的潜在生物标志物。

图2 QC样品评估的PCA得分图Fig.2 PCA score chart of quality control sample evaluation
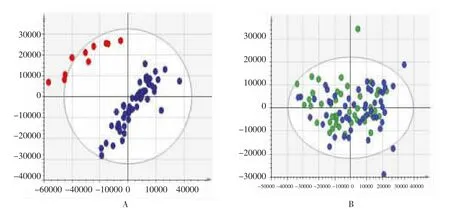
图3 健康对照组和口腔疾病患者组(干预前)、口腔疾病患者组(干预前)和黄连解毒汤干预组正离子模式下的PCA得分图Fig.3 PCA score chart of urine sample under positive ion mode from healthy control group and oral disease group(before intervention),oral disease group(before intervention)and Huanglian Jiedu Decoction intervention group
2.2.3 潜在生物标志物的鉴定 根据精确分子量和MS/MS结果以及与HMDB或标准品进行比较,健康对照组和口腔疾病患者组(干预前)之间初步鉴定出38个差异代谢物,其中正离子模式下32个、负离子模式下6个。口腔疾病患者组(干预前)和黄连解毒汤干预组之间初步鉴定出36个差异代谢物,其中正离子模式下28个、负离子模式下8个。3组尿样共有且给药后有一定改善趋势的差异代谢物共有10个,其中正离子模式下有9个,分别为癸酰肉碱、α-N-苯乙酰基-L-谷氨酰胺、反-2,顺-4-癸二烯酰肉毒碱、异亮羟基脯氨酸、3-氨基己酸、10,20-二羟基二十碳酸、菊蒿醇B、Sterebin A和亮菌素;负离子模式下有2个,分别为α-N-苯乙酰基-L-谷氨酰胺和L-谷氨酰胺。其中,α-N-苯乙酰基-L-谷氨酰胺在正、负离子模式下均检出。以α-N-苯乙酰基-L-谷氨酰胺为例,保留时间23.50min时,该化合物([M+Na]+m/z 287.1004(C13H16O4N2Na),[M+H]+m/z 265.1186),正离子模式下提取离子流图和质谱图如图7-1和图7-2中Ⅱ、Ⅲ所示。将结果与数据库中化合物进行比对,初步确定该化合物为α-N-苯乙酰基-L-谷氨酰胺。MS/MS质谱的结果也证实了这一点,m/z 270.0748(C13H13O4NNa)是由[M+Na]+峰裂解失去NH3得到的,进一步失去CO产生m/z 242.0797(C12H13O3NNa),再进一步失去C7H6基团得到 m/z 152.0323(C5H7O3NNa)。见图 7 中Ⅲ。根据以上信息,确定该化合物为α-N-苯乙酰基-L-谷氨酰胺。口腔疾病患者组(干预前)和健康对照组,以及黄连解毒汤干预组和口腔疾病患者组(干预前)潜在生物标志物的鉴定结果见表1、2。通过分析软件给出了口腔疾病患者组(干预前)和健康对照组,以及黄连解毒汤干预组和口腔疾病患者组(干预前)之间潜在标志物的变化趋势,标志物的增加或者减少反映了代谢通路的进行方向与趋势。
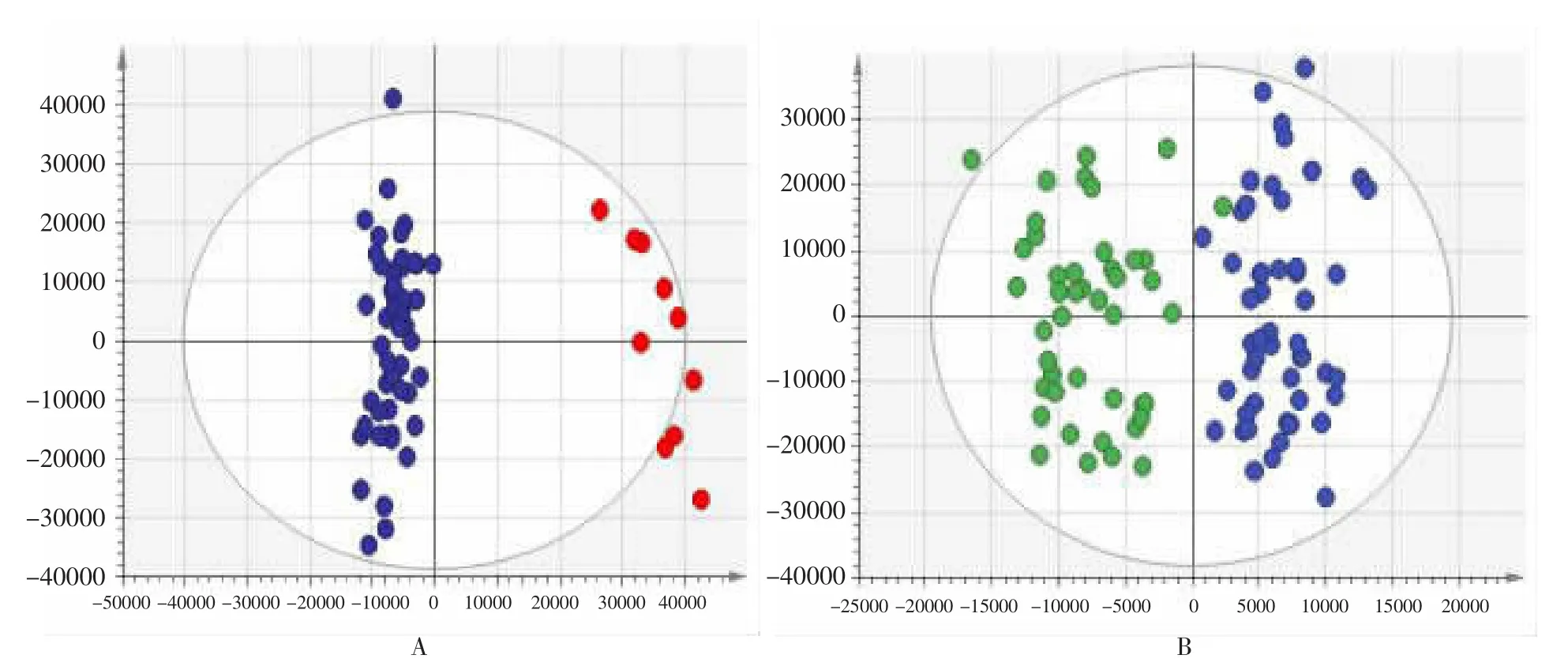
图4 健康对照组和口腔疾病患者组(干预前)、口腔疾病患者组(干预前)和黄连解毒汤干预组正离子模式下的OPLS-DA得分图Fig.4 OPLS-DA score plots of urine sample under positive ion mode from healthy control group and oral disease group(before intervention),oral disease group(before intervention)and Huanglian Jiedu Decoction intervention group

图5 正离子模式下健康对照组和口腔疾病患者组(干预前)的S-plot载荷图及对应火山图Fig.5 S-plot loadings plots and volcano plots of urine sample under positive ion mode from healthy control group and oral disease group(before intervention)
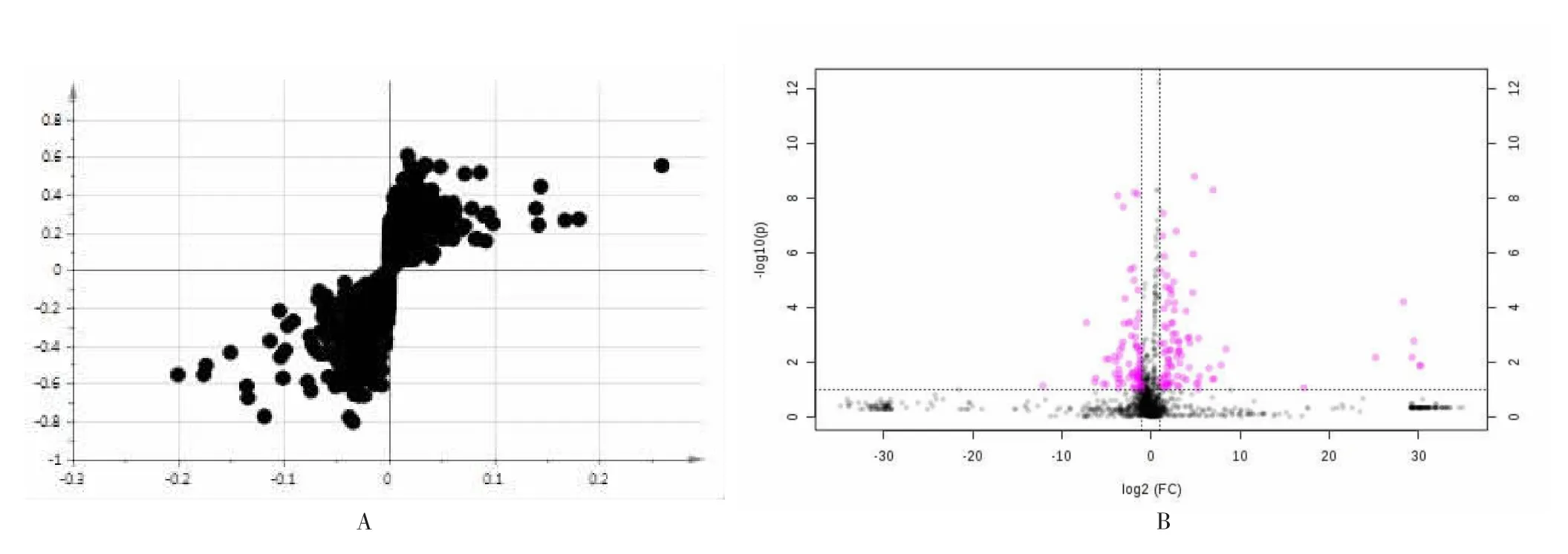
图6 正离子模式下口腔疾病患者组(干预前)和黄连解毒汤干预组的S-plot的载荷图及对应火山图Fig.6 S-plot loadings plots and volcano plots of urine sample under positive ion mode from oral disease group(before intervention)and Huanglian Jiedu Decoction intervention group

图7 -1潜在标志物α-N-苯乙酰基-L-谷氨酰胺的鉴定Fig.7-1 Identification of potential maker of α-N-phenylacetyl-L-glutamine
2.3 代谢通路分析 将10个通过模式识别筛选出的差异代谢物导入MetaboAnalyst软件进行代谢通路分析得到的结果见图8。推测黄连解毒汤治疗胃火炽盛证引起的口腔疾病主要涉及的代谢通路为三聚氰胺、天冬氨酸和谷氨酸代谢(alamine,aspartate and glutamate metabolism),D-谷氨酰胺和D-谷氨酸代谢(D-glutamine and D-glutamate metabolism)等。
3 讨论

图7 -2潜在标志物α-N-苯乙酰基-L-谷氨酰胺的鉴定Fig.7-2 Identification of potential maker of α-N-phenylacetyl-L-glutamine

表1 口腔疾病患者组(干预前)和健康对照组尿液生物标志物的鉴定结果Tab.1 Identification of biomarkers in oral disease group(before intervention)and healthy control group in urine

表2 黄连解毒汤干预组和口腔疾病患者组(干预前)尿液生物标志物的鉴定结果Tab.2 Identification of biomarkers in Huanglian Jiedu Decoction intervention group and oral disease group(before intervention)in urine
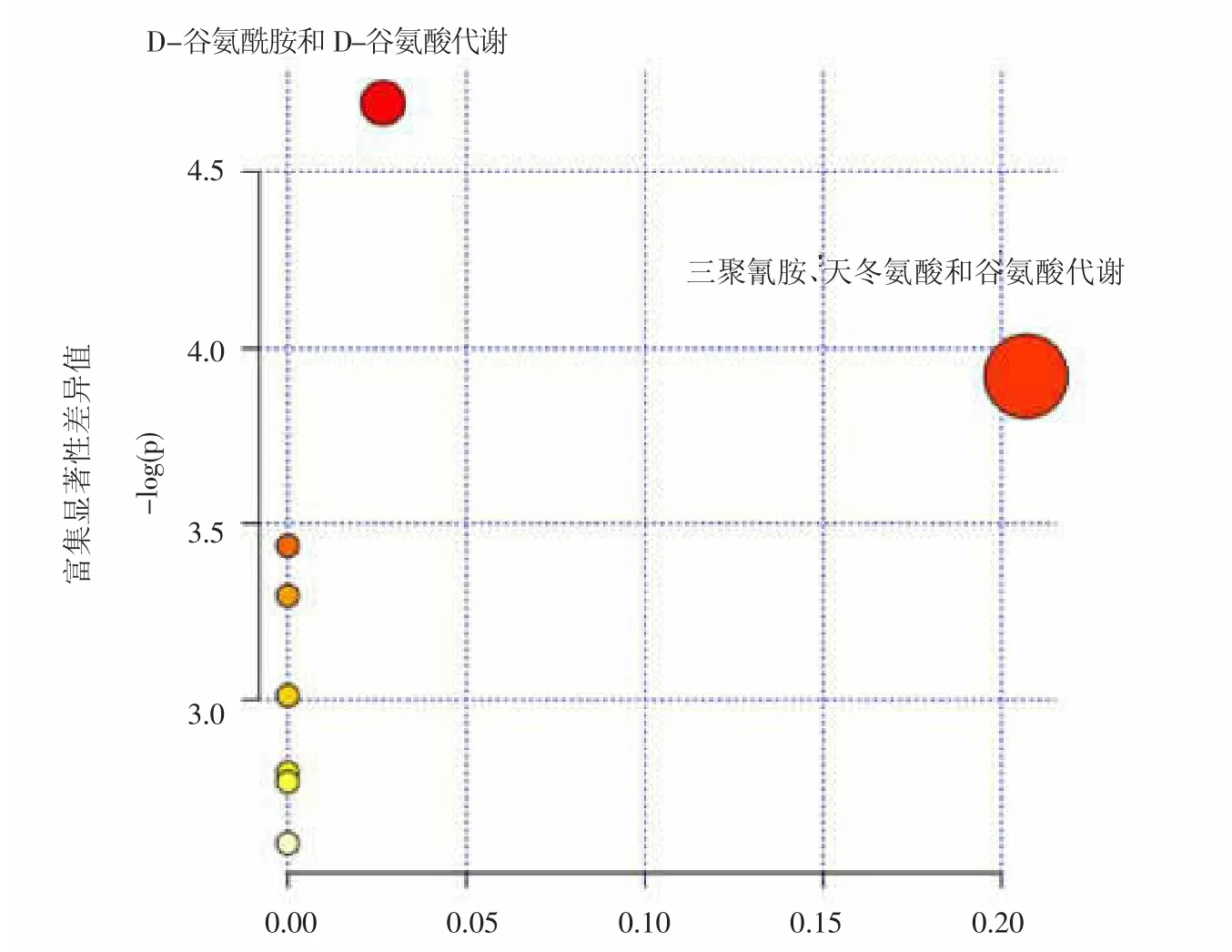
图8 黄连解毒汤干预胃火炽盛证引起的口腔疾病影响的代谢通路Fig.8 Metabolic pathway of Huanglian Jiedu Decoction influencing on oral diseases caused by syndrome of excessine heat in stomach fire
通过 UHPLC-MS方法对健康对照组、口腔疾病患者组(干预前)以及黄连解毒汤干预组3组人群的尿液进行检测,结果初步鉴定发现,健康对照组和口腔疾病患者组(干预前)存在38个差异代谢物,口腔疾病患者组(干预前)和黄连解毒汤干预组对比则存在36个差异代谢物,结果提示α-N-苯乙酰基-L-谷氨酰胺等10种化合物可能与黄连解毒汤干预胃火炽盛证口腔疾病的作用机制和代谢途径有关。
作为细胞内渗透剂,高水平的谷氨酰胺可引起脑细胞肿胀、脑水肿甚至颅内高压的发生[15]。本研究发现,口腔疾病患者组α-N-苯乙酰基-L-谷氨酰胺和L-谷氨酰胺明显升高,说明α-N-苯乙酰基-L-谷氨酰胺和L-谷氨酰胺含量过高可能促进上火的发生。肉毒碱种类或水平的变化在一定程度上可以提示体内脂肪酸或氨基酸代谢的紊乱,其水平升高与细胞线粒体脂质过载和脂肪酸不完全氧化有关[16],本研究结果提示黄连解毒汤可以通过调节体内脂肪酸或氨基酸代谢,如降低癸酰肉碱、反-2,顺-4-癸二烯酰肉毒碱、异亮羟基脯氨酸、3-氨基己酸的含量等,从而缓解胃火炽盛证的症状。10,20-二羟基二十碳酸可由环氧二十碳三烯酸经P450环氧化酶降解产生,同时会降低环氧二十碳三烯酸的活性[17]。10,20-二羟基二十碳酸在胃火炽盛证引起的口腔疾病患者尿液中含量升高,推测10,20-二羟基二十碳酸可能也是胃火炽盛证的生物标志物。
本研究将UHPLC-Orbitrap MS与PCA等统计方法相结合,分别对胃火炽盛证口腔疾病患者与健康对照组,以及口腔疾病患者黄连解毒汤干预前后的尿液进行快速分析,从中发现并鉴定出10种黄连解毒汤干预胃火炽盛证口腔疾病的潜在生物标志物,推测黄连解毒汤治疗胃火炽盛证口腔疾病主要涉及的代谢通路。本研究首次从代谢组学角度研究了胃火炽盛证口腔疾病的代谢轮廓,并初步阐明了黄连解毒汤的干预机制,为胃火炽盛证疾病的症状客观化提供科学依据。

