三维斑点追踪成像对阵发性房颤患者射频消融术前后左心室收缩功能的评价
文鹤龄 陈宇 梁中书电子科技大学附属医院四川省人民医院心内科(成都6007);中南大学湘雅三医院心内科(长沙4003)
心房颤动(atrial fibrillation,AF)是临床最常见的快速性心律失常,随着人口老龄化,房颤的发病率及房颤患者数量逐年增加。房颤可使心排血量下降,长期快速心室率房颤更可导致心动过速性心肌病。因此,与非房颤人群相比,房颤患者血流动力学不稳定,心力衰竭发生率增加[1]。由于抗心律失常药物长期治疗的疗效较差及药物本身潜在致心律失常的副作用,近年来非药物治疗手段引起了更多的关注,房颤导管射频消融术是转复窦律、改善心功的重要方法。
左心房的结构和功能对房颤的发生、维持起到重要作用[2],而既往研究亦多集中在对房颤患者左心房结构和功能的评估[3-5],对左心室结构和功能的关注则相对不足。现已明确房颤可导致左心室充盈压增高、舒张功能异常[6-7],左心室射血分数(left ventricular ejection fraction,LVEF)是临床上最常用的心脏收缩功能评价指标,但LVEF 正常是否能够说明房颤患者左心室收缩功能正常,尤其是对阵发性房颤(paroxysmal atrial fibrillation,PAF)患者左心室收缩功能的进一步评价,目前鲜见相关研究。三维斑点追踪成像(three dimensional speckle tracking imaging,3D-STI)是融合了实时三维超声和斑点追踪原理的前沿心脏超声诊断技术,可快速、准确地提供左心室所有节段及整体的应变参数,帮助临床评估心肌运动、心脏功能[8-10]。本研究拟采用3D-STI 评价PAF 患者在导管射频消融术前后左心室收缩功能的变化,探讨PAF 对左心室功能的影响,以期为临床治疗决策提供更多的理论依据。
1 对象与方法
1.1 研究对象将2015年1月至2017年1月在四川省人民医院、湘雅三医院心内科因PAF 接受导管射频消融术且在术后3 ~6 个月期间完成了超声心动图随访的35 例患者纳入本研究,其中男23例、女12 例,年龄32 ~69(55.54 ± 9.82)岁。纳入的PAF 患者均符合2010年欧洲心脏病学会心房颤动管理指南关于PAF 的诊断标准[13],术后随访期间均为窦性心律,无房颤复发证据。排除标准:合并心脏瓣膜病、心肌病、高血压病、冠心病、甲亢的患者;术后房颤复发者;过度肥胖、超声透声窗差等所致图像质量不符合3D-STI 要求的病例。选择年龄、性别匹配的30 例健康体检者作为正常对照组,其中男19 例,女11 例,年龄28 ~75(51.67 ± 10.17)岁。纳入的对照人群均经临床病史、体格检查、心电图、胸片、经胸超声心动图筛查无异常发现。所有受检者均对本研究知情同意。
1.2 仪器与方法采用日本Toshiba Artida SSH-880彩色多普勒超声诊断仪。所有接受导管射频消融术的PAF 患者(术前1 周、术后3 ~6 个月期间)及健康对照人群均在窦性心律下采集二维及三维超声心动图图像,检查时连接同步心电图。
二维超声心动图:应用二维探头PST-30SBT,频率2.5 ~5.0 MHz,进行常规经胸超声心动图检查。观测指标包括:左心房内径(LA)、左心室内径(LV)、二尖瓣E 峰血流速度(E)、组织多普勒二尖瓣瓣环e'峰速度(e')、采用双平面Simpson 法测量左心室舒张末容积(LVEDV)、左室收缩末容积(LVESV)及左心室射血分数(LVEF)。
3D-STI:应用三维探头PST-25SX,频率1.0 ~3.0 MHz,将探头置于心尖部,显示心尖四腔心切面,调节扇角与深度,图像满意后启动Full-4D 模式,图像自动转换成心尖四腔和两腔切面,采集左心室三维全容积图像。应用该超声诊断仪配套的3DT 图像分析软件进行分析。调出存储的三维全容积图像,启动3DT 软件,图像自动转换成心尖四腔和两腔切面及3 个短轴切面(心尖段、乳头肌水平、基底段),在心尖四腔和两腔切面上手动确定二尖瓣前、后叶根部2 个点及心尖处心内膜1 个点,程序自动描记出左心室内外膜边界,必要时可手动调节边界曲线以优化追踪效果,随之软件自动计算出左心室壁所有节段以及整体的应变值(图1A、B)。观测指标包括:左心室整体纵向应变(global longitudinal strain,GLS)、整体环向应变(global circumferential strain,GCS)、整体径向应变(global radial strain,GRS)、整体面积应变(global area strain,GAS)。
1.3 统计学方法采用SPSS 22.0 统计软件进行统计分析,定性资料采用卡方检验,定量资料以均数± 标准差表示,两组间比较采用独立样本t检验,多组间比较采用方差分析。P<0.05 为差异有统计学意义。
2 结果
2.1 基线资料两组患者在病例数、年龄、性别、基础心率、体表面积、体质指数的组间差异无统计学意义(P>0.05)。见表1。
2.2 二维及三维超声指标比较PAF 组手术前后LA 无明显变化,均较正常对照组增大,差异有统计学意义(P<0.05)。PAF组手术前后LV、LVEDV、LVESV 无变化,与正常对照组相比差异无统计学意义(P>0.05)。PAF 组LVEF 正常,手术前后无变化,与正常对照组相比差异无统计学意义(P>0.05)。代表左室充盈压及心肌舒张功能的E/e'比值,PAF 组手术前后无变化,均较正常对照组增大,差异有统计学意义(P<0.05)。见表2。
与正常对照组相比,PAF 组GLS、GAS 降低,差异有统计学意义(P<0.05),GCS、GRS 无明显降低(P>0.05)。与术前相比,PAF 组术后3 ~6 个月随访时GAS 增加,差异有统计学意义(P<0.05),GLS、GCS、GRS 无明显变化(P>0.05)。见表2。
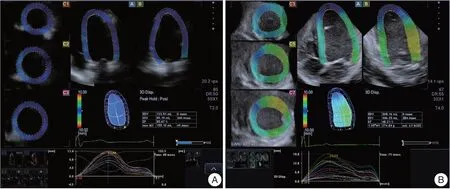
图1 三维斑点追踪成像示意图Fig.1 Representative recording of three-dimensional speckle tracking imaging in control group and PAF group
表1 PAF 组术前与正常对照组基线资料比较Tab.1 Comparison of clinical characteristics ±s
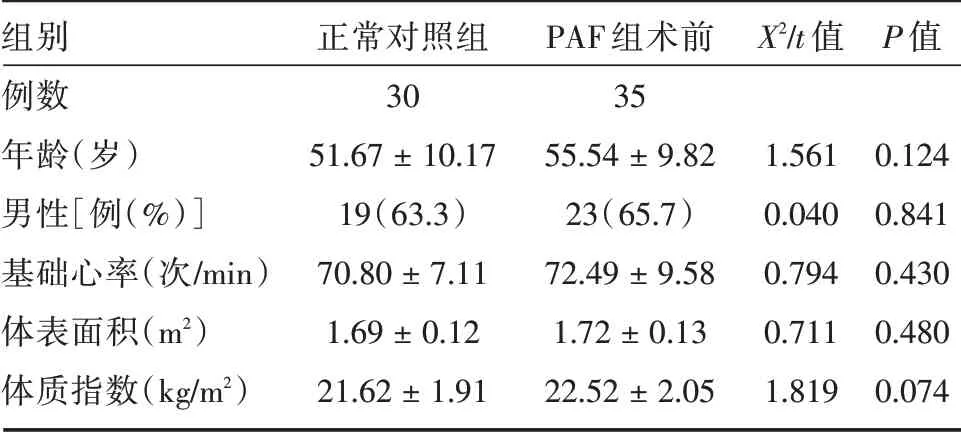
表1 PAF 组术前与正常对照组基线资料比较Tab.1 Comparison of clinical characteristics ±s
组别例数年龄(岁)男性[例(%)]基础心率(次/min)体表面积(m2)体质指数(kg/m2)正常对照组30 51.67±10.17 19(63.3)70.80±7.11 1.69±0.12 21.62±1.91 PAF 组术前35 55.54±9.82 23(65.7)72.49±9.58 1.72±0.13 22.52±2.05 X2/t 值1.561 0.040 0.794 0.711 1.819 P 值0.124 0.841 0.430 0.480 0.074
3 讨论
随着人口老龄化,AF已成为一种流行病,因心力衰竭、血栓栓塞等并发症,该病的致残率和致死率明显升高,严重危害人群健康,对房颤患者心脏结构和功能的评估及治疗方法的改进是近年来心血管领域的研究热点。本研究旨在探讨PAF 对左心室收缩功能的影响,以期为临床决策提供理论依据。
3D-STI 的原理是把心肌组织看作心肌内稳定的声学斑点,于心脏收缩期、舒张期在三维空间上连续追踪同一位置心肌的声学斑点,以此获得心肌在纵向、径向、圆周方向上的运动轨迹信息,并对心肌形变进行定量分析,可区分心肌主动运动和被动运动,早期发现心肌运动障碍,在综合评价心肌局部及整体收缩功能方面具有显著优势[8-10]。此外,3D-STI 具有非角度依赖和重复性好等优点,并克服了二维斑点追踪技术受限于左室几何模型假说、局限于所扫描的二维平面内追踪、易产生追踪错误等缺点,因此较二维斑点追踪技术更能全面、准确地评价心肌功能[11-12]。
表2 PAF 组术前、术后与正常对照组二维及三维超声指标比较Tab.2 Two-dimensional and three-dimensional ultrasound indices in PAF group(pre-and post-operation)and control group±s

表2 PAF 组术前、术后与正常对照组二维及三维超声指标比较Tab.2 Two-dimensional and three-dimensional ultrasound indices in PAF group(pre-and post-operation)and control group±s
注:LA,左心房内径;LV,左心室内径;LVEDV,左心室舒张末容积;LVESV,左室收缩末容积;LVEF,左心室射血分数;E,二尖瓣E峰血流速度;e':组织多普勒二尖瓣瓣环e'峰速度;GLS,整体纵向应变;GCS,整体环向应变;GRS,整体径向应变;GAS,整体面积应变。*与正常对照组比较,P <0.05;#与PAF组术前比较,P <0.05
组别LA(mm)LV(mm)LVEDV(mL)LVESV(mL)LVEF(%)E(cm/s)e'(cm/s)E/e'GLS(%)GCS(%)GRS(%)GAS(%)正常对照组30.63±1.92 45.60±3.53 97.03±18.32 36.47±8.60 62.39±4.11 83.13±17.82 12.38±3.11 7.00±1.99-16.93±2.28-30.27±4.43 28.43±8.32-43.85±4.35 PAF 组术前34.51±3.84*47.31±3.98 105.20±20.98 41.77±10.37 60.13±6.32 72.06±18.39*8.05±1.75*9.29±2.90*-15.35±2.19*-29.07±3.77 28.05±6.67-37.64±5.10*PAF 组术后33.97±3.67*47.29±3.44 105.74±18.71 41.89±9.99 60.39±5.52 74.09±16.27 8.95±1.94*8.61±2.48*-16.16±2.55-29.42±3.55 26.83±7.56-40.64±4.64*#
本研究采用3D-STI 对PAF 患者射频消融术前后左心室收缩功能的变化进行评价,发现与健康人群相比,PAF 患者虽然LVEF 正常,但左心室整体纵向应变、整体面积应变明显降低,说明其心肌收缩功能已经受损,也说明应变参数较LVEF 更能反映心肌收缩功能的真实情况,这一结果与MORRIS 等[13]的研究基本一致。与术前相比,PAF患者在术后3 ~6 个月整体面积应变增加,但其余应变指标无明显变化。作为经典的心功能评价指标,LVEF仅从心脏容量变化的角度来评价心功能,虽然能从一定程度上反映心脏的泵功能,但不足以敏感的反映疾病早期心肌特性的变化。既往研究表明,房颤患者的病理生理过程与心室纤维化密切相关,且随房颤持续时间而加重[14-16]。本研究发现,PAF 患者左心室心肌形变能力、收缩功能已经开始下降,这可能与房颤引起左室纤维化有关。基础状态下,左心室三层心肌的血流灌注和舒缩状态不尽相同,心内膜下心肌位于冠脉血供的远端且所受应力最大,最易发生微血管功能障碍、心肌纤维化等改变,PAF 患者左心室整体纵向应变较健康人群明显下降,这可能与心内膜下的心肌纤维主要为纵向心肌有关。而面积应变则代表了从形变前初始心内膜面积到形变发生后心内膜面积缩小的百分率,结合了心肌纵向应变及环向应变的整体变化[9,17]。笔者观察到PAF 患者左心室整体面积应变较健康人群明显下降,而射频消融术后仅有整体面积应变明显增加,说明面积应变是较其他应变参数更敏感的评价心肌形变的指标,同时说明PAF 患者心肌收缩功能受损在术后是部分可逆的。另外,在术后随访期间,PAF 患者LA、E/e'比值等指标无明显好转,可能与我们随访时间尚短有关。
综上,尽管常规超声心动图LVEF 正常,但PAF 患者左心室收缩功能已经受损,3D-STI 可敏感地反映其左心室心肌形变、收缩功能的降低,因此近年来指南提倡的房颤上游治疗药物[18],在这类患者中可考虑积极的使用。
本研究的局限性:目前三维超声技术的时间及空间分辨力还不理想,基于3D-STI 的应变分析对图像清晰度要求高,由于透声窗差、心律失常发作(术后房颤复发、持续性房颤等)对图像采集和图像分析有较大干扰,故未将这部分患者纳入本研究,可能造成研究的偏差。另外,本研究样本量较小,随访时间较短,只能得出初步结论,尚需大样本长期随访的结果来验证,为临床疾病诊治提供更准确有效的信息。

