外源性胰岛素抵抗综合征1 例
谭宇欣 高立超 郭晖
吉林大学白求恩第一医院二部内分泌科(长春130000)
患者男,61 岁,2009年前因“脑梗死”行检查发现血糖增高,明确诊断为糖尿病,应用“三短一长”胰岛素方案降糖,之后更换多种胰岛素,胰岛素每天总量最高达88 U,血糖控制不理想,表现为夜间及口服相对偏低,午晚餐后显著升高,血糖最高达31 mmol/L(图1);于2018年1月 查 血 清 胰 岛 素 水平>300 mU/L;C 肽0.62 ng/mL,抗胰岛素抗体(IAA)阳性,考虑外源性胰岛素抵抗综合征可能,加维格列汀50 mg,每天2次,格列美脲2 mg 1次/d,二甲双胍0.425 g 2 次/d,达格列净10 mg 1 次/d口服并减少胰岛素注射次数及用量,胰岛素减量至24 U/d。患者血糖控制在空腹7 mmol/L 左右,餐后12 mmol/L,方案改变6 d 后复查血清胰岛素水平159.21 mU/L。因口服二甲双胍出现呕吐,遂自行停用二甲双胍,再次将胰岛素加量至早18 U 午18 U 晚16 U,且血糖控制差,于2018年9月13日入院。
既往史:类风湿关节炎病史8年,曾服用激素(具体不详),近5年未应用糖皮质激素及免疫抑制剂;间断口服双氯芬酸钠片;白癜风病史5年,未系统治疗,湿疹病史3年,间断外用丙酸氟替卡松乳膏。查体:头面部可见不规则色素脱失样白斑,双手关节梭形样变。身高:165 cm;体质量:52 kg;身体质量指数19.1 kg/m2。辅助检查:葡萄糖18.2 mmol/L;糖化血红蛋白11%。血常规:白细胞计数2.50 ×109;中性粒细胞绝对值1.50 × 109/L。风湿检测:抗环胍氨酸多肽抗体64.90 U/mL;类风湿因子96.00 IU/mL;C-反应蛋白8.1 mg/L。甲功三项:游离三碘甲状原氨酸2.58 pmol/L;游离甲状腺素10.67 pmol/L;促甲状腺激素55.664 μIU/mL。
入院后(2018年9月15 日)使用PEG 沉淀后,血清胰岛素水平明显下降,由135.61 mU/L至2.14 mU/L,胰岛素抗体滴度>50 U/mL,C 肽1.82 ng/mL。肝、肾功能、血脂、外科综合、心电图、腹彩等未见明显异常;综上诊断为外源性胰岛素抵抗综合征,2 型糖尿病,甲状腺功能减退症,类风湿关节炎,遂于入院后停用胰岛素,加用口服降糖药阿格列汀25 mg 每天1 次,吡格列酮15 mg 每天1 次,阿卡波糖早100 mg午50 mg 晚100 mg,达格列净10 mg每天1 次,患者血糖整体下降,波动减小,停用胰岛素6 d 后复查胰岛素35.77 mU/L(图2)。
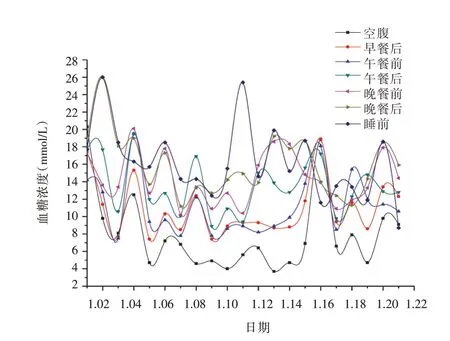
图1 2018年1月住院时血糖Tab.1 Blood glucose during hospitalization in January 2018
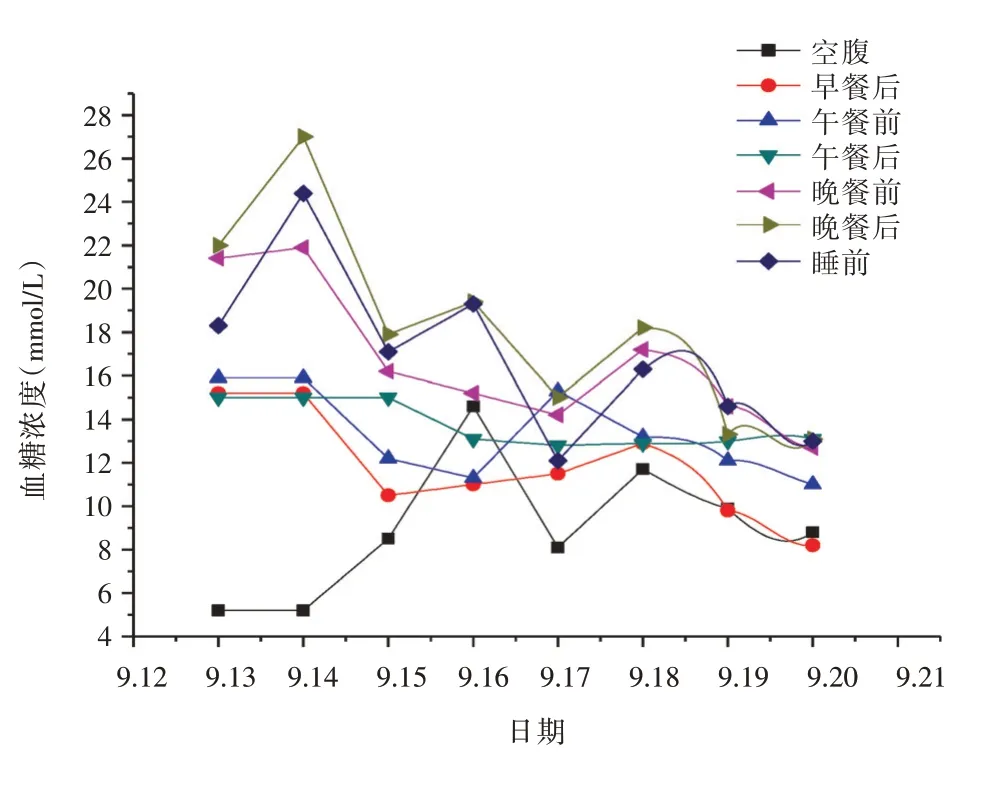
图2 2018年9月住院时血糖Tab.2 Blood glucose during hospitalization in September 2018
讨论EIAS 的诊断、机制及临床表现外源性胰岛素抵抗综合征(exogenous Insulin autoimmune syndrome,EIAS),是与糖尿病患者注射外源性胰岛素诱导的胰岛素抗体有关的临床综合征,表现为以对大剂量胰岛素不敏感的高血糖和自发性低血糖为特征的血糖波动。诊断标准为:临床表现:(1)血糖波动及低血糖反应:血糖与胰岛素治疗的剂量不相吻合,大幅度波动。夜晚及空腹血糖较低,可能出现夜间低血糖,白天及餐后血糖较高。(2)存在胰岛素抵抗,胰岛素降糖效果减弱。实验室检查:胰岛素自身抗体(IAA)升高,一般无抗胰岛细胞抗体和谷氨酸脱羧酶阳性,血清胰岛素水平显著升高,与C 肽水平不匹配,部分患者血清胰岛素水平大于可测定值。
1922年胰岛素开始用于糖尿病治疗。1956年首次报道在接受胰岛素治疗的患者血清里发现胰岛素抗体,后续在许多使用胰岛素治疗的患者中,检测到了高浓度的胰岛素抗体。
外源性胰岛素抗体的发生通常与胰岛素的应用时限、给药方式、胰岛素剂型、遗传因素等有关。应用外源性胰岛素<2 周者未测出IAA,1年以上IAA 阳性率明显升高,长于1年者高达95.12%。使用胰岛素强化治疗的患者,体内IAA 浓度比常规注射治疗的患者更高。胰岛素有三种类型:动物胰岛素、重组人胰岛素和胰岛素类似物。由于动物胰岛素的氨基酸序列与人胰岛素不同,动物胰岛素的免疫原性较高,当前较少应用于长期治疗,暂不赘述。皮下注射快速作用的胰岛素类似物和重组人胰岛素对胰岛素抗体的诱导无明显差异;但也有研究表明赖脯胰岛素的免疫原性比重组人胰岛素低,对于高滴度的胰岛素抗体引起的胰岛素抵抗的患者,赖脯胰岛素能够有效地控制血糖,及降低胰岛素抗体:常见的长效胰岛素类似物有甘精胰岛素和地特胰岛素,接受甘精胰岛素治疗的患者至少1年内未发现IA 水平升高,也许与甘精胰岛素以聚合物形式存在皮下,循环胰岛素浓度较低有关。
高浓度胰岛素抗体可逆性结合胰岛素,使游离胰岛素减少,临床表现为餐后血糖峰值更高。而夜间时,胰岛素-胰岛素抗体复合物解离,大量游离胰岛素释放,从而引起空腹及夜间血糖偏低,甚至低血糖,且对外源性胰岛素极不敏感。
由于C 肽和胰岛素的循环半衰期分别为5 ~10 min 和30 ~35 min,因此尽管等摩尔分泌,胰岛素与C 肽的比值通常小于1。而且C 肽和胰岛素结构不一样,两者无交叉免疫原性,对于存在胰岛素抗体的患者,C 肽对于内源性胰岛素分泌水平的评价更有意义。有研究表明胰岛素(mu/L)/c 肽(nmol/L)比值>8.6 时,有提示胰岛素抗体阳性意义,比值越大,阳性可能性越大,本例中,血浆胰岛素水平极高,>300 mu/L,同步C 肽水平为0.62 ng/mL,两者比值约1 451,显著升高,符合EIAS 特征。
与胰岛素自身免疫综合症(IAS)的鉴别 EIAS 需与胰岛素自身免疫综合征(IAS)鉴别,其在1970年首次报道,是无胰岛素应用史的非糖尿病患者发生的严重自发性低血糖症,IAS患者常有含巯基的药物服药史,常伴有自身免疫性疾病,如系统性红斑狼疮(最为多见),皮肌炎、自身免疫性甲状腺疾病等。目前IAS 的机制尚不清楚,最普遍接受的假说是由于自身抗体结合胰岛素,使其无法发挥其作用。血糖升高进一步促进胰岛素释放,血糖下降,胰岛素分泌随之减少,总胰岛素水平也会下降。胰岛素突然自身抗体解离,产生过多的游离胰岛素,引起严重的低血糖,因此具有高结合能力和低亲和力的胰岛素自身抗体,引起低血糖症状,而外源性胰岛素诱导产生的抗体通常有低胰岛素结合容量和相对高的胰岛素亲和力。因此,EIAS 通常表现为高血糖相关症状和严重胰岛素抵抗,而严重的自发低血糖较少。如本例主要以血糖升高及胰岛素抵抗为主要表现,未发生明确低血糖。
治疗首先停止外源性胰岛素,使用口服药替代,IAA 并不是终身性抗体,一项小规模的前瞻性研究表明,停止胰岛素后1 个月体内IAA 平逐渐下降,但抗体的完全消失可能需要超过1 或2年。一项对于11 例中国患者的回顾性研究中,抗体消失的中位时间为17 个。双胍类药物可以改善外周组织对胰岛素敏感性,促进胰岛素免疫复合物解离,磺脲类药物可以刺激胰岛细胞分泌胰岛素,及减弱抗体结合作用,双胍类、磺脲类药物单独应用或联合应用都可有效减少抗体,目前还有联合二甲双胍及α-葡萄糖苷酶抑制剂、DPP-IV 抑制剂成功改善反复低血糖,有效控制高血糖的案例报告。二线治疗为糖皮质激素,适用于对上述疗效差的患者,也有少量的使用血浆置换及免疫抑制剂治疗成功的报道。启动营养治疗,摄入低GI 食物,主食增加荞麦、大豆等谷物,对餐后血糖能产生长期的获益。
本例患者老年糖尿病患者,体型偏瘦,病程较长,合并多种自身免疫病,多次更换胰岛素,大剂量胰岛素血糖居高不下,实验室检查血清胰岛素水平明显升高,C 肽水平降低,胰岛素/C 肽比值明显升高,胰岛素抗体阳性,通过加用口服药,减少或停用外源性胰岛素,较有效的控制了血糖及胰岛素浓度。但患者自行加量胰岛素,血糖不降反升,在再次停止胰岛素注射后,血糖逐渐平稳,夜间和日间血糖波动显著减小,血清胰岛素明显下降,血糖水平总体下降,趋于平稳。
本案例提示,如有糖尿病患者对大剂量外源性胰岛素不敏感,日间血糖高,伴有夜间及上午血糖偏低或有低血糖发作,均应检查胰岛素抗体、胰岛素、C 肽水平,以排除EIAS 的可能,如血清胰岛素浓度显著升高,必要时可行PEG 沉淀法进一步确诊EIAS,治疗上应停止或减少外源性胰岛素使用,加用口服药物。

