足月胎膜早破的引产时机对妊娠结局的影响
马丽媛,李超,詹瑛,彭伟,马春玲,卢彩霞,李灿
胎膜早破指临产前的胎膜破裂,根据孕周不同分为未足月胎膜早破(孕周<37周)和足月胎膜早破(孕周≥37周)。足月胎膜早破的发生率为8%~10%[1],为产科常见并发症。胎膜早破导致孕妇产褥期感染率及新生儿患病率增加[2-3]。目前关于足月胎膜早破的临床引产时机尚缺乏一致的结论[4],临床工作中各医疗卫生机构根据临床经验、用药习惯采取的引产时限也不尽相同,有观点认为为了减少宫内感染等感染并发症应破膜后积极引产[5],但也有观点认为单纯根据破膜时间决定引产时机是不合理的,应采用个体化治疗原则,尤其应考虑孕妇宫颈成熟度对引产成功率的影响[6]。本研究将宫颈成熟度与破膜时间相结合,分析不同引产时机孕妇的围生期结局,希望为临床工作提供更合理、安全的引产方案。
1 对象与方法
1.1 研究对象选取青岛大学附属医院和临沂市中心医院2015年1月—2017年12月足月胎膜早破的孕妇共1 474例。纳入标准:①符合胎膜早破的诊断标准:无诱因少量阴道流液,用窥器检查见液体自宫颈流出,阴道后穹窿有液池,用pH试纸检测试纸变蓝。②孕周≥37周。③单胎头位,且无明显的合并症及经阴道分娩的禁忌证,排除精神系统疾病、剖宫产手术史、胎位异常、明显头盆不称及其他产科并发症不适合经阴道分娩者。④未发生宫内感染和胎儿窘迫。
1.2 方法孕妇入院后立即完善化验检查,行胎心监护,监测脉搏、体温。破膜时间超过12 h应用抗菌药物预防感染。根据宫颈评分及引产开始时间将孕妇分为4组,A组,Bishop评分≥6分,破膜2 h未临产缩宫素引产;B组,Bishop评分≥6分,破膜12 h未临产缩宫素引产;C组,Bishop评分<6分,破膜2 h未临产缩宫素引产;D组Bishop评分<6分,破膜12 h未临产缩宫素引产。缩宫素引产方法为:500 mL乳酸钠林格注射液加入2.5 U的缩宫素注射液,摇匀后静脉滴注,根据宫缩情况调整滴速,直至诱发有效宫缩。若发生不良反应则停药[4]。回顾性分析不同组别的妊娠结局。4组孕妇的年龄、孕周、羊水指数、新生儿体质量、初产妇和经产妇所占比例差异均无统计学意义(P>0.05),具有可比性。见表1和表2。
表1 孕妇一般情况比较 (±s)
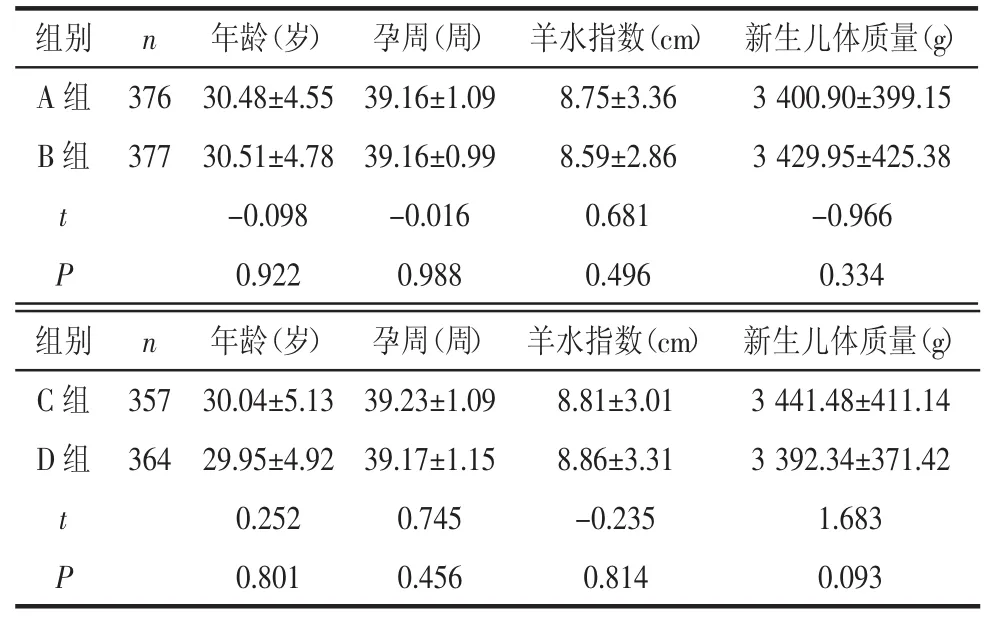
表1 孕妇一般情况比较 (±s)
组别 n 年龄(岁) 孕周(周) 羊水指数(cm)A 组 376 30.48±4.55 39.16±1.09 8.75±3.36 B 组 377 30.51±4.78 39.16±0.99 8.59±2.86 t -0.098 -0.016 0.681 P 0.922 0.988 0.496新生儿体质量(g)3 400.90±399.15 3 429.95±425.38-0.966 0.334组别 n C组 357 D组 364 t P年龄(岁) 孕周(周) 羊水指数(cm) 新生儿体质量(g)30.04±5.13 39.23±1.09 8.81±3.01 3 441.48±411.14 29.95±4.92 39.17±1.15 8.86±3.31 3 392.34±371.42 0.252 0.745 -0.235 1.683 0.801 0.456 0.814 0.093
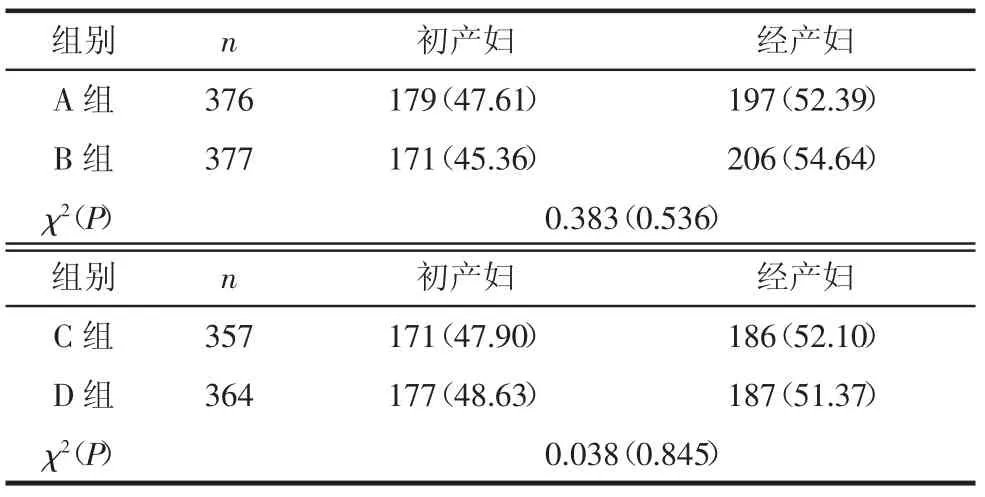
表2 各组初产妇和经产妇所占比例 例(%)
1.3 统计学方法采用SPSS17.0软件进行统计分析,定量资料用均数±标准差(±s)表示,A、B组间和C、D组间比较采用t检验;定性资料用率表示,组间比较采用卡方检验或确切概率法。P<0.05为差异有统计学意义。
2 结果
2.1 孕妇分娩方式比较A、B组间的阴道分娩率差异无统计学意义(P>0.05),而D组阴道分娩率高于C组,差异有统计学意义(P<0.05),见表3。
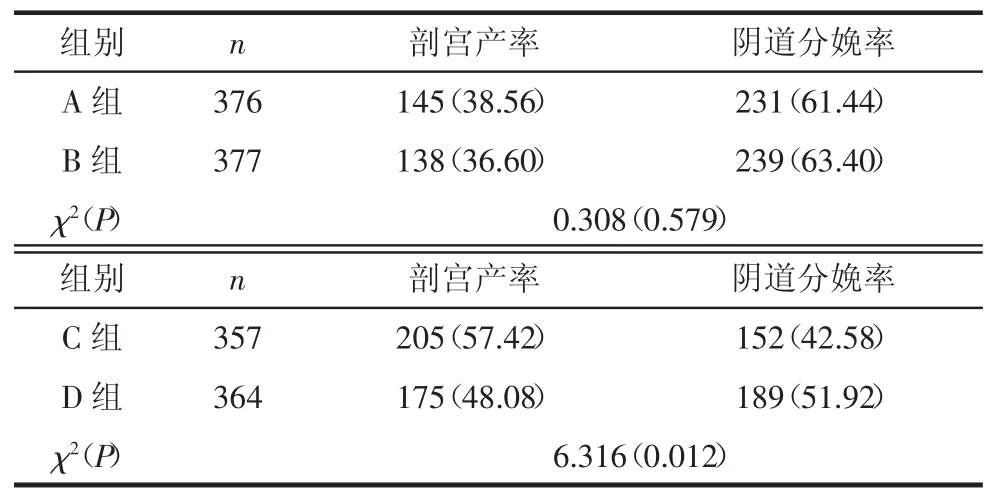
表3 孕妇分娩方式的比较 例(%)
2.2 孕妇产程时间比较A组和B组孕妇的第一产程、第二产程、第三产程及总产程时间比较差异无统计学意义(P>0.05),C组和D组孕妇的第一产程、第二产程、第三产程及总产程时间比较差异无统计学意义(P>0.05),见表 4。
表4 孕妇产程时间比较 (±s)
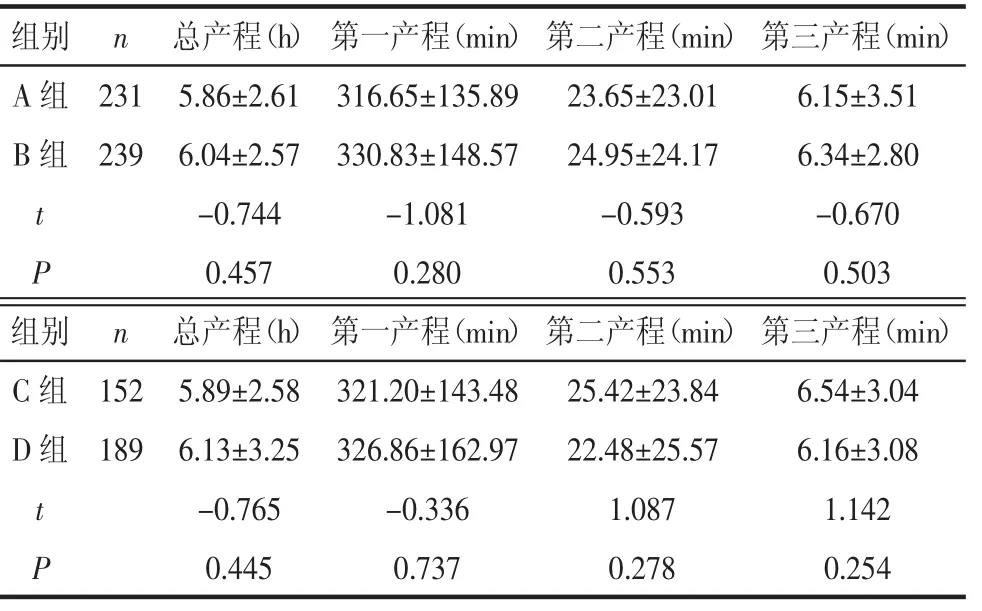
表4 孕妇产程时间比较 (±s)
组别 n 总产程(h) 第一产程(min) 第二产程(min) 第三产程(min)A 组 231 5.86±2.61 316.65±135.89 23.65±23.01 6.15±3.51 B 组 239 6.04±2.57 330.83±148.57 24.95±24.17 6.34±2.80 t -0.744 -1.081 -0.593 -0.670 P 0.457 0.280 0.553 0.503组别 n 总产程(h) 第一产程(min) 第二产程(min) 第三产程(min)C 组 152 5.89±2.58 321.20±143.48 25.42±23.84 6.54±3.04 D 组 189 6.13±3.25 326.86±162.97 22.48±25.57 6.16±3.08 t -0.765 -0.336 1.087 1.142 P 0.445 0.737 0.278 0.254
2.3 孕妇自胎膜破裂至分娩的时间比较A组自胎膜破裂至分娩的时间与B组相比,时间较短,差异有统计学意义(P<0.01),C组与D组相比差异无统计学意义(P>0.05)。见表 5。
表5 孕妇自胎膜破裂至分娩的时间比较 (h,±s)
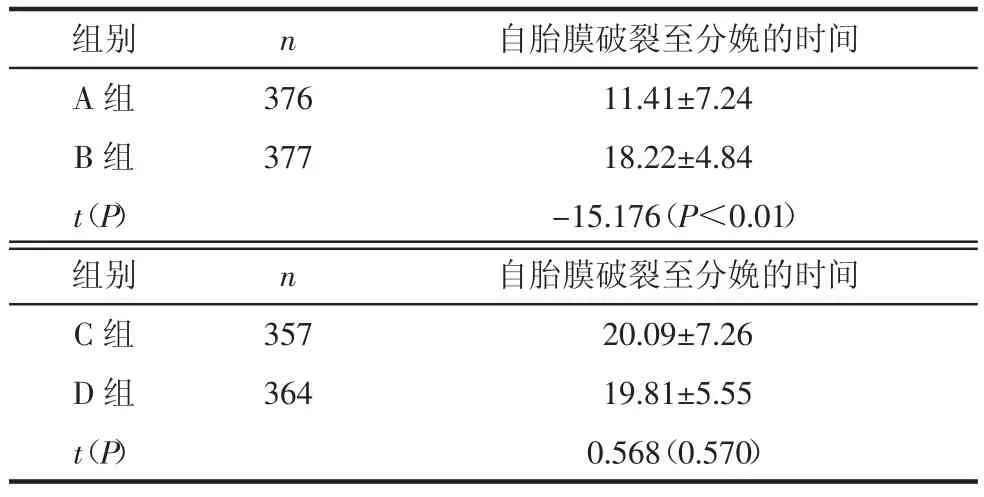
表5 孕妇自胎膜破裂至分娩的时间比较 (h,±s)
组别 n 自胎膜破裂至分娩的时间A 组 376 11.41±7.24 B 组 377 18.22±4.84 t(P)-15.176(P<0.01)组别 n 自胎膜破裂至分娩的时间C 组 357 20.09±7.26 D 组 364 19.81±5.55 t(P)0.568(0.570)
2.4 孕妇引产并发症比较A组产褥期感染率低于B组(P<0.05),C组和D组比较差异无统计学意义(P>0.05)。产后出血率、脐带脱垂发生率、缩宫素过敏发生率、羊水栓塞发生率、胎盘早剥发生率、先兆子宫破裂发生率A组与B组比较、C组与D组比较,差异无统计学意义(P>0.05)。孕妇引产并发症的总发生率A组低于B组(P<0.05),C组高于D组(P<0.05)。见表 6。

表6 孕妇引产并发症比较 例(%)
2.5 新生儿并发症比较A、B两组间胎儿窘迫率、新生儿转科率差异无统计学意义(P>0.05),C组的胎儿窘迫率、新生儿转科率高于D组,差异有统计学意义(P<0.05)。见表 7。
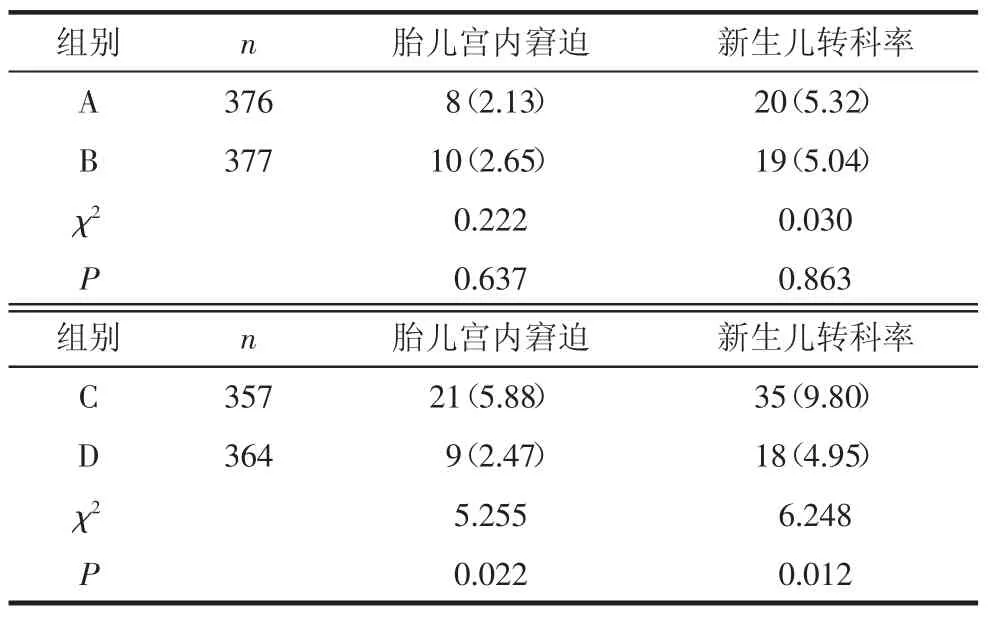
表7 新生儿并发症比较 例(%)
3 讨论
胎膜早破多由羊膜腔受力不均、头盆不称、胎位异常等原因所致,容易导致母婴感染、胎儿宫内窘迫、新生儿窒息,威胁母婴健康。应用缩宫素引产是足月胎膜早破孕妇引产的最常使用的方法[7]。目前临床关于足月胎膜早破引产时机尚缺乏一致结论。随着破膜时间的延长,宫内感染率、产褥期感染率增加[8],故有学者主张破膜后2 h未临产为避免感染发生应积极引产[2],最新版胎膜早破诊断与处理指南推荐足月胎膜早破2~12 h内积极引产[9],能显著降低绒毛膜羊膜炎及母体产褥感染的风险。也有学者主张破膜后12 h未临产行缩宫素引产[10]。
分娩的发动是多因素综合作用的结果,其中宫颈成熟度是能否成功经阴道分娩的重要因素。临床工作中多采用Bishop评分法评估宫颈成熟度,Bishop评分<6分为宫颈不成熟,Bishop评分≥6分为宫颈成熟。宫颈不成熟时,子宫缩宫素受体相对较少,加之内源性前列腺素分泌较少,常导致引产失败,而宫颈成熟时,引产成功率较高。所以有必要根据宫颈是否成熟,调整缩宫素的应用时机。本研究将引产开始时间结合宫颈成熟度分组,进行缩宫素引产的研究,结果显示宫颈评分≥6分的孕妇破膜后2 h引产较12 h引产其阴道分娩率无明显差异,但产褥期感染率及引产并发症发生率明显少于12 h引产者,表明对于宫颈成熟的足月胎膜早破孕妇,可破膜后2 h积极引产。
本研究显示对于宫颈评分<6分的孕妇,破膜后期待12 h较2 h缩宫素引产者的经阴道分娩率高,而引产并发症发生率低,胎儿宫内窘迫率及新生儿转科率低。同时对于宫颈评分<6分的孕妇,破膜后2 h引产者与12 h引产者比较,自胎膜破裂至分娩的时间无明显差异,不增加宫内感染率及产褥期感染率。相关研究也证实破膜后可适当延长期待处理的时间,支持本研究结论[11]。有研究指出由于足月妊娠孕妇胎膜破裂后,可刺激蜕膜和子宫肌细胞产生前列腺素,从而诱发宫缩和促进宫颈成熟,50%孕妇可在12 h内自然临产[9]。因此,对于宫颈不成熟的足月胎膜早破孕妇适当延后应用缩宫素引产的时机,不仅增加了孕妇期待自然临产的机会,同时减少了医疗干预,降低医疗成本,减轻了患者痛苦。
本研究显示对宫颈评分<6分的孕妇,破膜后2 h引产其引产并发症的发生率增加,且胎儿宫内窘迫发生率及新生儿转科率明显高于期待12 h引产者。有学者认为,应避免宫颈不成熟孕妇因为过早的行缩宫素引产所导致的子宫破裂等危险。同时过早干预、在引产过程中的操作、长时间的胎心监测以及缩宫素引起的过强宫缩所导致的不适感,降低了孕妇对经阴道分娩的依从性和信心,增加了剖宫产率[12]。因此临床医师在临床工作中,应该对足月胎膜早破孕妇行过早的缩宫素干预所导致的母儿不良结局引起足够的重视。本研究提示对于宫颈不成熟的孕妇,在保障母儿安全的前提下,应适当地期待自然临产,减少过早及不必要的缩宫素干预所导致的不良妊娠结局。
综上所述,足月胎膜早破孕妇,宫颈成熟者,破膜后期待2 h未临产应积极引产,可减少产褥期感染率及引产并发症发生率;宫颈不成熟者,期待至破膜后12 h未临产再行缩宫素引产,较2 h行缩宫素引产阴道分娩成功率更高,胎儿窘迫率及引产并发症的总发生率更低,同时并不增加产褥期感染率。

