食用明胶中微量铬含量测定的方法研究
(广西-东盟食品药品安全检验检测中心,广西南宁530021)
铬(chromium)广泛存在于自然界中,人体中微量铬对人的糖代谢、脂肪代谢、蛋白质及核酸的相互作用有着重要的影响,然而铬的过度摄入会对人体造成危害[1],国际癌症研究机构(international agency for researchoncancer,IARC)已将六价铬列为人类致癌物[2]。食用明胶(gelatin)是用新鲜动物皮骨提取的胶原蛋白质[3],为淡无色至淡黄色薄片状或粉粒状末,无臭、无味,应用于食品工业作赋形剂、增稠剂,是食品工业广泛应用的添加剂。人体如果摄入含铬明胶,其中的六价铬会引起细胞周期调控系统CDK6异常表达改变细胞周期和DNA相关修复过程从而引发肿瘤[4]。因此食用明胶铬含量检测已成为食品药品检测的一个重要指标。目前测定食用明胶中微量铬的前处理方式主要有微波消解、湿法消解、干法灰化[5];测定方法主要有原子荧光(atomic fluorescence spectrometry,AFS)法、原子吸收-石墨炉(graphite furnace atomic absorption apectrometry,GF-AAS)法和电感耦合等离子质谱(inductively coupled plasma mass spectrometry,ICP-MS)法[6-9]。目前国内相关标准如:GB 5009.123-2014《食品安全国家标准食品中铬的测定》[10]及GB 5009.268-2016《食品安全国家标准食品中多元素的测定》[11]中已有关于铬测定的方法,但由于食品基质的复杂性和铬元素的化学特性,按标准操作会出现某些基质的样品消解不彻底、仪器测定存在特殊干扰等情况,导致铬测定的精密度低、准确度差。本研究拟采用3种样品前处理方法及2种检测仪器进行综合全面的比较,以期确立一种快速、便捷、准确,适用于食用明胶中微量铬的测定方法。
1 材料与方法
1.1 仪器与设备
900T原子吸收光谱仪:PerkinElmer公司;Icap Q电感耦合等离子体质谱仪:Thermo公司;Mars6微波消解仪:CEM公司;P330马弗炉:Nabertherm公司;BHW-09C石墨电热消解仪:北京博通公司;ML204电子天平(感量0.1 mg和1 mg):Mettler Toledo公司;Milli-Q超纯水仪:Millipore公司。
1.2 材料与试剂
食用明胶质控样:编号T01530;铬标准值范围:380 μg/kg~719 μg/kg,中值:600 μg/kg,分析实验室能力验证 (food analysis performance assessment scheme,FAPAS)考核组织提供。
铬标准溶液、钪标准溶液:1 000 mg/L,介质为2%硝酸,美国O2SI公司;硝酸、氢氟酸:分析纯,德国Merck公司;30%过氧化氢:优级纯,广东光华科技股份有限公司;氩气:纯度99.999%,广西国信气体研究有限公司。
1.3 试验方法
1.3.1 标准溶液配制
1)铬标准使用液:将铬标准储备液用硝酸溶液(5+95)逐级稀释至浓度为100 ng/mL。
2)钪标准使用液:将钪标准储备液用硝酸溶液(5+95)逐级稀释至浓度为10 ng/mL。
3)标准系列溶液的配制:分别吸取铬标准使用液(100 ng/mL)0、0.5、1.00、2.00、3.00、4.00 mL 于 25 mL容量瓶中,用硝酸溶液(5+95)稀释至刻度,混匀。各容量瓶中每毫升分别含铬 0、2.00、4.00、8.00、16.0 ng。由GF-AAS和ICP-MS分别吸取标准系列溶液进行测定。
1.3.2 样品前处理方法
1.3.2.1 微波消解
准确称取试样约0.5 g(精确至0.001 g)于微波消解罐中,分别加入6 mL硝酸、4 mL硝酸和2 mL氢氟酸、4 mL硝酸和2 mL双氧水,按照微波消解的操作步骤消解试样(消解条件参见表1)。冷却后取出消解罐,在电热板上于140℃~160℃赶酸至0.5 mL~1.0 mL。消解罐放冷后,将消化液转移至10 mL容量瓶中,用少量水洗涤消解罐2次~3次,合并洗涤液,用水定容至刻度。同时做试剂空白试验、加标回收试验和平行性试验,微波消解程序见表1。

表1 微波消解仪工作条件Table 1 Working parameters of microwave digestion
1.3.2.2 湿法消解
准确称取试样约0.5 g(精确至0.001 g)于消化管中,分别加入6 mL硝酸、4 mL硝酸和2 mL氢氟酸、4 mL硝酸和2 mL双氧水,在可调式电热炉上消解(升温程序:120℃保持0.5 h、升温至180℃2 h、升温至200℃)。若消化液呈棕褐色,再加硝酸,消解至冒白烟,消化液呈无色透明或略带黄色,取出消化管,冷却后用水定容至10 mL。同时做试剂空白试验、加标回收试验和平行性试验。
1.3.2.3 干法灰化
准确称取试样约2 g(精确至0.001 g)于30 mL坩埚中,置于马弗炉中,于550℃恒温3 h~4 h,至试样呈白灰状,取出冷却,用硝酸溶液(1+1)溶解并用水定容至10 mL。同时做试剂空白试验、加标回收试验和平行性试验。
1.3.3 测定方法
1.3.3.1 原子吸收-石墨炉法(GF-AAS)
铬元素原子化温度高,经对比,食用明胶的测定即使不加基体改进剂,原子化过程中也不会出现干扰,因此选择不使用基体改进剂以获得更高的灵敏度。测定波长:357.87 nm;狭缝宽度:0.7 nm;灯电流:5 mA;进样体积:20 μL;背景扣除:塞曼扣背景;GFAAS工作参数见表2。

表2 GF-AAS主要工作参数Table 2 Main operating parameters of GF-AAS
1.3.3.2 电感耦合等离子体质谱法(ICP-MS)
铬同位素有50Cr、52Cr、53Cr、54Cr,其中52Cr天然丰度最高且干扰较低,选为待测同位素。52Cr主要的多原子离子干扰为40Ar12C+、36S16O+、38Ar14N+、36Ar16O+,使用动能歧视型碰撞池(kinetic energy discrimination,KED)模式,通入氦气作为碰撞气,能有效减少干扰。ICP-MS测量过程中,被测元素的信号受样品溶液中共存元素或基体元素的影响,引起被测物信号的增强或减弱的现象,称之为抑制或增敏效应[12]。抑制或增强效应可通过内标法进行校正,使用10 ng/mL的钪(Sc)作为内标元素可以减少这些干扰及仪器各种条件的波动带来的影响,ICP-MS工作参数见表3。
1.3.3.3 铬含量计算公式
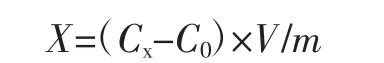
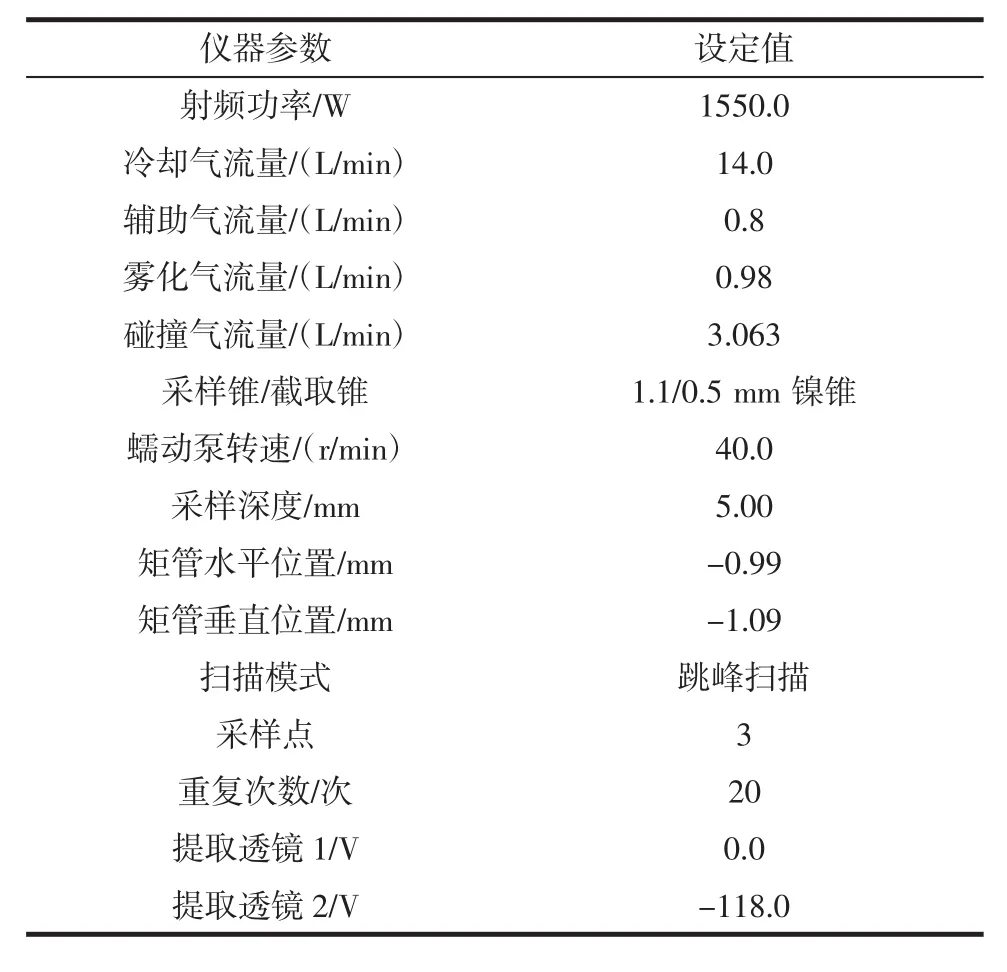
表3 KED模式ICP-MS主要工作参数Table 3 Main operating parameters of ICP-MS in KED mode
式中:X为样品中铬的含量,μg/kg;Cx为样品溶液中铬的质量浓度,ng/mL;C0为空白溶液中铬的质量浓度,ng/mL;V为样品溶液定容体积,mL;m为样品称样量,g。
2 结果与分析
2.1 不确定度分量来源的分析
GF-AAS法及ICP-MS法测定明胶铬含量的不确定度的主要来自:标准曲线拟合计算浓度过程;样品重复性测定次数;样品的处理过程;标准溶液的配制过程[13];分析仪器的相对不确定度。
2.2 样品测定结果分析
本文比较了3种不同的消解方式,结果见表4和表5。
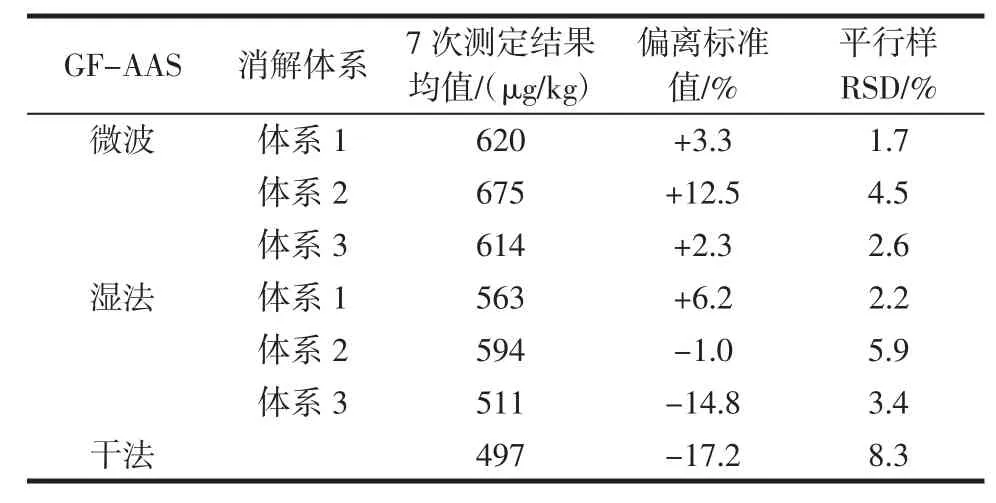
表4 GF-AAS测定铬结果Table 4 GF-AAS results of chromium
由表4和表5可知,干法灰化法在样品经马弗炉灰化后加酸溶解并转移的过程中,易造成铬元素损失;湿法消解耗时长且消解不够彻底;微波消解耗时短且消解效果好,平行样精密度高。研究了不同的酸体系的消解效果,结果表明,硝酸-过氧化氢体系消解效果最佳,过氧化氢能够使样品消解液更澄清透亮,起到氧化脱色作用,羟自由基同时也更利于有机物的分解,从结果来看该消解体系得到的样品溶液测定结果精密度最高,也接近质控样的标准值;而硝酸-氢氟酸体系消解过程中引入氟离子,在赶酸过程中即使加入高氯酸也较难将氟赶尽,在高氯酸赶F的操作中,时间不易控制,时间不够或过长均会导致铬测定结果的偏高或偏低[14],效果不理想。此外,还比较了不同的仪器,对同一消解方式的测定结果:铬是高温元素,在原子化温度(横向加热)高达2 300℃时,干扰极少,原子吸收-石墨炉测定的结果比较稳定,而电感耦合等离子体质谱测定铬时,铬易被同质荷比的多原子离子干扰,开启碰撞模式消除这类干扰则使灵敏度下降,导致测定结果稳定性较原子吸收-石墨炉法差。

表5 ICP-MS测定铬结果Table 5 ICP-MS results of chromium
2.3 标准曲线测定结果
铬标准曲线测定结果见图1,图2。

图1 GF-AAS标准曲线图Fig.1 GF-AAS calibration curve
2.4 检出限
GF-AAS和ICP-MS的仪器检出限均采用纯水连续11次测定铬信号值的3倍标准偏差所相当的铬浓度,再经过稀释倍数和取样质量及单位转换系数的换算,得到对应方法检出限GF-AAS法:0.01 mg/kg;ICPMS法:0.006 mg/kg,均能很好地满足试验灵敏度需求。
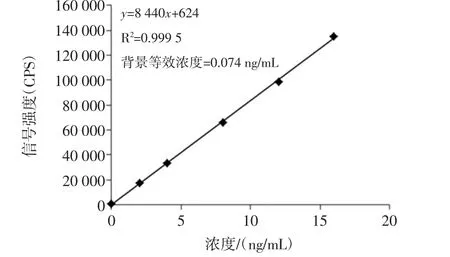
图2 ICP-MS标准曲线图Fig.2 ICP-MS calibration curve
2.5 回收率试验
按照不同前处理方法分别称取试样,向其中加入与称取试样铬含量接近的铬标准溶液,分别按照相应的前处理方法制备得到回收率试样待测液,供GFAAS及ICP-MS测定,得到不同前处理条件下的试样回收率,回收率见表6、表7。

表6 GF-AAS加标回收率Table 6 GF-AAS spike recovery
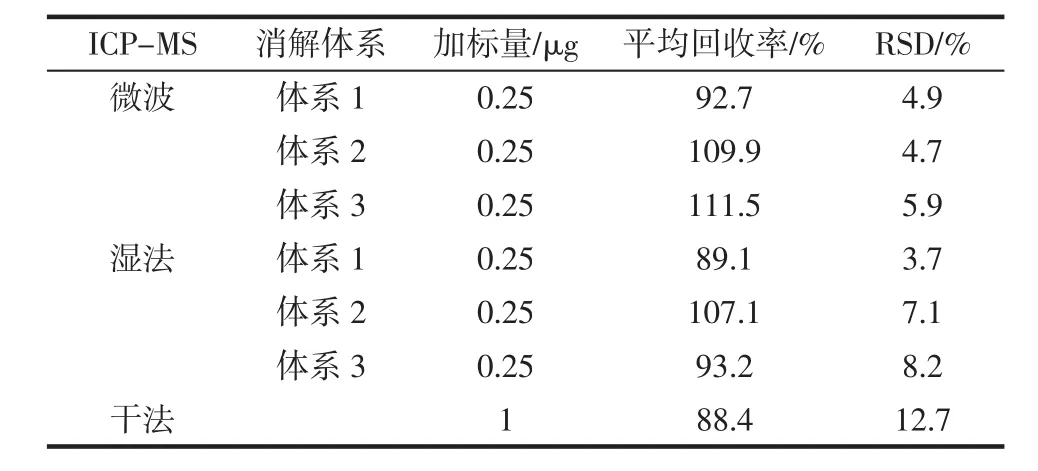
表7 ICP-MS加标回收率Table 7 ICP-MS spike recovery
综合比较表6、表7中回收率情况,可以看出干法回收率略低,各种酸体系的微波消解和湿法消解所得回收率测定液,在GF-AAS和ICP-MS中测得回收率结果均比较满意。
2.6 精密度试验
按照2.2中微波消解(体系1~体系3)、湿法消解(体系1~体系3)、干法灰化的7种前处理方式,各取7份平行样进行前处理,所得7组待测样品溶液分别在GF-AAS和ICP-MS上进行精密度测定,结果表明相比较于其他前处理方法,硝酸-过氧化氢体系—微波消解这一前处理方法所得的结果精密度最好,在GFAAS上测得RSD=1.7%,在ICP-MS上测得RSD=2.6%,试验数据详见表8、表9。
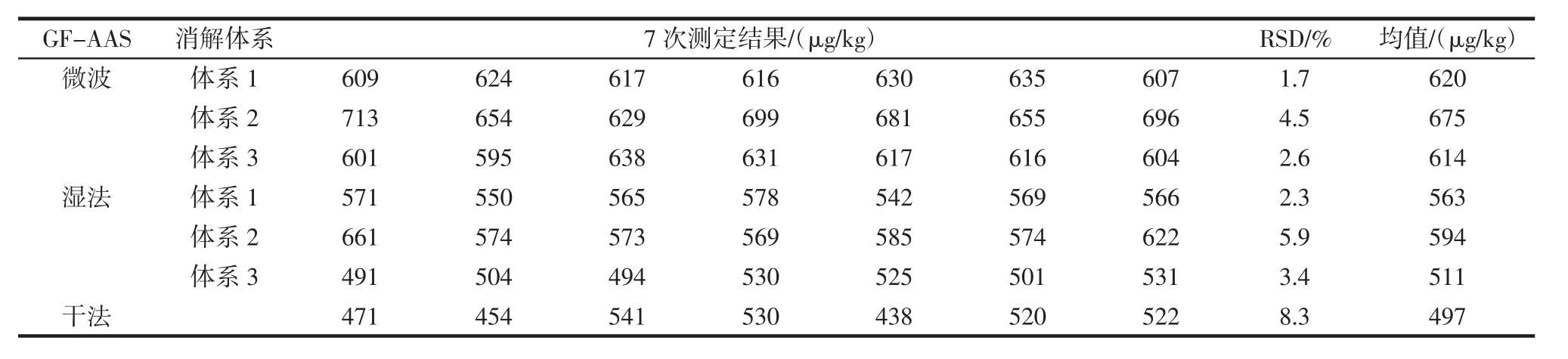
表8 GF-AAS精密度(n=7)Table 8 GF-AAS precision(n=7)
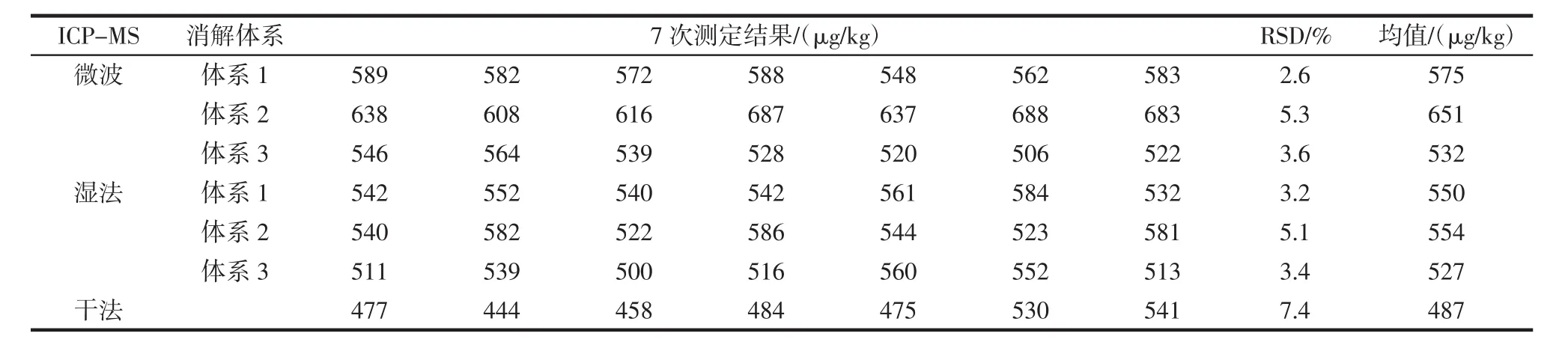
表9 ICP-MS精密度(n=7)Table 9 ICP-MS precision(n=7)
2.7 重现性
取同一食用明胶质控样,在不同的实验室设备条件下,由不同的人员按照同样的方法操作(试验2),得到的铬测定结果与原测定结果(试验1)对比见表10、表11。
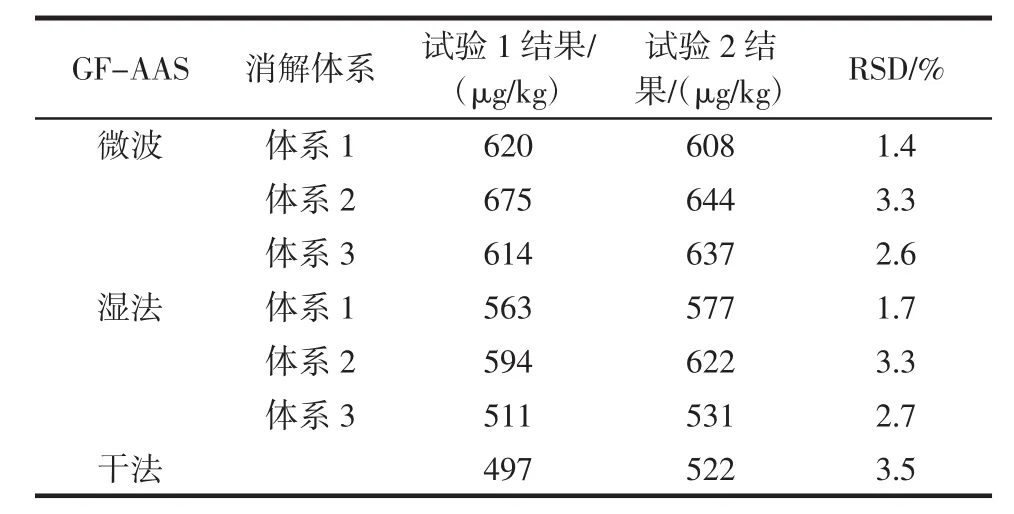
表10 GF-AAS测定铬结果Table 10 GF-AAS results of chromium
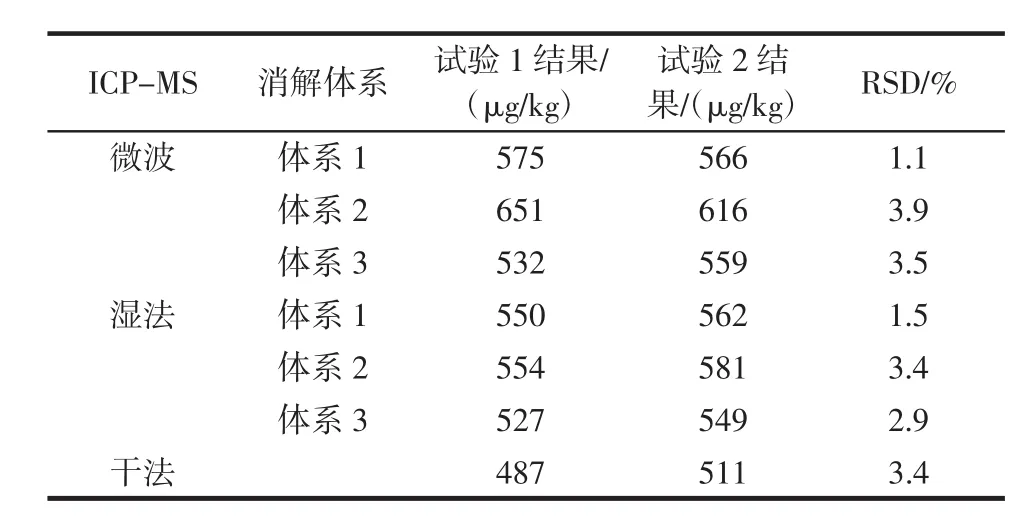
表11 ICP-MS测定铬结果Table 11 ICP-MS results of chromium
3 结论与讨论
硝酸-过氧化氢体系-微波消解-原子吸收-石墨炉这一测定方法,样品消解效果最好,平行样测定结果精密度最高,所得结果较接近标准物质铬含量的标准值,加标回收测定结果最为满意。如不加过氧化氢溶液,从湿法消解结果及ICP-MS测定结果看来,精密度、偏离标准值、加标回收率等方面结果较差。
本研究经过多方面对比,样品使用硝酸-双氧水消解体系进行微波密闭消解并采用原子吸收-石墨炉法测定食用明胶中微量铬,灵敏度高、精密度高、准确度好、重现性好、回收率高,质控样测定结果接近其中值,是适合用于明胶中微量铬测定的较好的方法。