经皮经肝胆囊穿刺引流术在复杂胆道外科中的应用
张金梁,翟 博,陈雪健,王 伟,徐力善
(哈尔滨医科大学附属第四医院,黑龙江 哈尔滨,150001)
经皮经肝胆囊穿刺引流术(percutaneous transhepatic gallbladder drainage,PTGBD)是近年广泛开展的微创外科新技术,因具有创伤小、操作简便、床旁可行等诸多特点,临床上主要用于不能耐受手术或麻醉的危重急性胆囊炎的治疗。近年,笔者团队在常规开展PTGBD技术的基础上,逐渐将其应用范围扩展至合并胆道梗阻的多种复杂胆道疾病,收到较好的临床效果。现将2015年6月至2018年6月哈尔滨医科大学附属第四医院肝胆外科开展的50例PTGBD患者的临床资料报道如下。
1 资料与方法
1.1 纳入标准 PTGBD行胆道外引流的前提是:术前影像学判断胆道梗阻位于胆囊管汇合部以下的胆总管;胆囊输出道通畅,无狭窄及梗阻;胆囊胀大,以便于穿刺并作为判断引流效果的间接依据;恶性肿瘤,病灶应距胆囊管一定距离,避免短期内再梗阻;有手术、麻醉禁忌证或需胆道外引流,以减轻黄疸、控制病情。纳入疾病包括:(1)急性胆囊炎伴胆道梗阻;(2)急性化脓性胆管炎;(3)胆源性胰腺炎伴胆总管梗阻;(4)肿瘤引起的梗阻性黄疸;(5)肿大淋巴结或胆道炎性狭窄导致胆总管梗阻。
1.2 临床资料 本组50例患者中男32例,女18例;42~89岁。临床症状:均有不同程度的腹痛、黄疸,发热34例(占68%),右上腹部肿块18例(占36%),上消化道出血1例(占2%)。合并高血压病28例、糖尿病18例、心脏病11例、肺部疾病7例、脑血管病8例、甲亢1例、肾功能不全3例。按病因分组:(1)结石性胆囊炎导致梗阻性黄疸20例,合并胆总管结石16例(80%),是最主要的原因,其中1例为肝吸虫虫卵形成胆总管结石;Mirizzi综合征3例(15%),术后均经手术证实,并根据瘘口确定临床分型(Ⅱ型2例,Ⅲ型1例);胆囊出血并胆道梗阻1例(5%)。1例患者合并甲状腺功能亢进,基础代谢率+50%,为中度甲亢。(2)急性化脓性胆管炎伴胆囊胀大10例,均有Charcot三联征,其中2例出现五联征,8例患者体温超过39℃,5例白细胞计数>20×109/L,凝血酶原时间延长7例,合并胆总管结石8例。(3)胆源性胰腺炎伴胆总管梗阻6例,合并胆囊结石4例。(4)肿瘤引起的胆总管梗阻性黄疸9例,术前诊断为胰头癌4例、壶腹周围癌5例;其中3例患者经术前评估为肿瘤不可切除,6例为可根治性切除。9例患者中1例因肿瘤继发胆囊炎。(5)胆管周围淋巴结肿大致胆总管梗阻伴胆囊扩张2例。(6)胆道炎性狭窄导致胆总管梗阻伴胆囊扩张3例。IgG4相关性胆管炎1例,IgG4相关性胰腺炎2例,患者血清IgG4水平均升高。
1.3 方法
1.3.1 以猪尾管行PTGBD(一步法) 患者取平卧位,先行超声检查,肋间定位体表穿刺点,避开肝内明显血管结构,选择胆囊床与肝脏接触处为胆囊穿刺点。常规皮肤消毒、铺巾,以2%利多卡因局部麻醉后,做小切口。嘱患者屏住呼吸,超声引导下将18G穿刺针自下一肋骨上缘经肝沿胆囊床方向缓慢进入胆囊体部,退出中间针芯,使用20 mL注射器抽取胆汁送检。拔出外支撑针芯,同时将8Fr亲水性涂层猪尾巴导管送入胆囊;继续向前推送导管约5 cm,卡扣锁紧,使猪尾巴导管头端成猪尾状盘曲于胆囊内。用引流管固定装置固定导管于皮肤,用20 mL注射器缓慢抽吸胆汁,胆囊腔缩小后接无菌袋持续引流。见图1~图4。

图1 急性胆源性胰腺炎,胆囊内可见结石
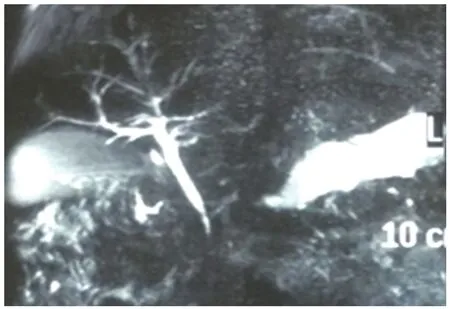
图2 MRCP示胆总管下段中断,锥形变窄

图3 超声下可见穿刺管进入胆囊

图4 导管头端成猪尾状盘曲于胆囊
1.3.2 以三腔管行PTGBD(二步法) 此法适于穿刺风险较高的患者,以深静脉穿刺包内三腔管进行替代。穿刺方法同上,但需置入导丝后撤出穿刺针,扩皮器沿导丝方向一直进针至胆囊床,扩皮器充分打开隧道后撤出,置入三腔管。待超声监测到三腔管进入胆囊腔后再撤出导丝。引流管固定装置固定导管于皮肤,用20 mL注射器缓慢抽吸胆汁,胆囊腔缩小后接无菌袋持续引流。
1.4 统计学处理 采用SPSS 13.0软件进行数据分析。计量资料以均数±标准差(±s)表示,比较采用配对t检验,检验水准α=0.05。
2 结 果
50例患者均成功完成PTGBD,穿刺成功率为100%。4例患者术后有局限性腹膜炎,腹痛较剧烈,考虑为少量胆汁漏,予以止疼抗炎治疗后第2天症状缓解;3例患者术后腹胀、食欲不佳;2例因引流管不耐受,术后第2~3天行肋间神经封闭;3例引流管护理不当,术后5~8周管腔堵塞,返院行通管处理后引流恢复通畅;余者无明显不适,住院3~27 d,平均(20.4±6.2)d;带管 2~21周,平均(5.6±3.8)周。非肿瘤患者(n=41)PTGBD术后72 h白细胞计数、中性粒细胞百分比、总胆红素、天门冬氨酸氨基转移酶、凝血酶原时间较术前均有好转。见表1。
急性化脓性胆管炎伴胆囊扩张10例患者中,1例因基础心脏疾病重,术后心衰转往ICU,余者均在病房完成治疗,术后患者生命体征平稳,炎症及胆道梗阻得到有效缓解,体温于穿刺后48~72 h内逐渐恢复正常,腹痛缓解,腹部体征减轻,行抗炎治疗复查白细胞正常后出院。胆源性胰腺炎伴胆总管梗阻6例患者,腹痛缓解时间3~5 d,住院15~25 d,出院前手术治疗4例,1例因肺部疾病转入ICU治疗,患者均康复出院。肿瘤引起的胆总管梗阻性黄疸患者9例,与术前相比,PTGBD术后3 d总胆红素、天门冬氨酸氨基转移酶均有好转,凝血酶原时间差异无统计学意义(P>0.05)。PTGBD减黄效率于术后1周内较为显著,随着时间的延长效率逐渐降低。见表2。胆管周围淋巴结肿大致胆总管梗阻伴胆囊扩张2例,行PTGBD穿刺后予以抗炎治疗,术后平均1周胆红素降至正常。IgG4相关性胆管炎1例,IgG4相关性胰腺炎2例,术前总胆红素为115.6 μmol/L,行PTGBD减黄的同时予以激素类药物治疗。
PTGBD术后2例患者因肿瘤进展,术后3个月加行经皮肝穿刺胆道引流术;4例患者未行其他手术治疗;44例患者行下一阶段手术前胆红素水平降至正常或术前理想水平。
表1 非肿瘤患者手术前后相关指标的比较(±s)

表1 非肿瘤患者手术前后相关指标的比较(±s)
时间 白细胞计数(×109/L)中性粒细胞百分比(%)总胆红素(μmol/L)天门冬氨酸氨基转移酶(U/L)凝血酶原时间(s)PTBGD 术前 15.4±3.6 86.6±3.2 69.4±9.8 63.2±6.4 13.9±2.5术后 72 h 9.6±253 78.2±2.5 40.8±5.5 51.2±3.7 12.1±2.3 t值 -28.48 -13.25 -16.29 -10.44 -3.39 P 值 <0.001 <0.001 <0.001 <0.001 <0.002
表2 肿瘤引起的胆总管梗阻性黄疸患者手术前后相关指标的比较(±s)

表2 肿瘤引起的胆总管梗阻性黄疸患者手术前后相关指标的比较(±s)
时间 总胆红素(μmol/L)天门冬氨酸氨基转移酶(U/L)凝血酶原时间(s)PTBGD 术前 363.3±24.5 104.4±10.5 13.2±1.5术后第 3天 230.8±13.6 90.2±8.2 12.4±1.3术后第 7天 154.2±18.1 87.5±9.4 12.1±2.2术后第 10天 110.4±14.7 84.6±7.3 11.9±1.7 F值 -14.19 -3.19 -1.209 P值 <0.001 <0.02 >0.05
3 讨 论
PTGBD是在超声引导下经皮经肝行胆囊穿刺置管引流,传统上主要应用于因高龄、合并严重系统性疾病不能耐受麻醉及手术的急性胆囊炎患者[1]。因PTGBD可于床旁操作、简便易行、引流确切、效果明显,从而得到广泛开展。我们在临床工作中体会,传统PTGBD的目的虽然在于胆囊引流,但对于胆囊与胆道间无梗阻的患者,PTGBD可将肝脏分泌的胆汁经胆道、胆囊管、胆囊持续引出体外。因此我们将PTGBD应用于合并胆道梗阻的胆囊炎、胆管炎、胆道良性狭窄或恶性肿瘤等病例中,获得了良好效果。
对于胆道梗阻需要引流减黄的患者,以往临床多采用经皮肝穿刺胆道引流术、经乳头插管留置鼻引流及胆道支架引流术[2-3]。但经皮肝穿刺胆道引流操作复杂,需要结合超声穿刺与放射线造影方能完成,胆道管径较细的患者失败率较高,且容易损伤肝内管道[4]。内镜逆行胰胆管造影经乳头插管留置鼻引流、胆道支架引流术及需要行逆行性胰胆管造影,甚至破坏括约肌功能、加重逆行感染或诱发相关性胰腺炎[5-6]。尤其本组中急性胰腺炎患者均处于胰腺炎急性期,内镜逆行胰胆管造影可能加剧病情;而胆源性胰腺炎患者一方面需择期行胆囊切除术或附加胆道探查取石术,另一方面患者胆囊多扩张,胆道压力大,治疗期间可能存在胆囊内结石再次脱落进入胆总管加剧病情的风险。因此,对于此类患者行PTGBD在实现胆胰分流、胆道减压、减黄的同时,有效降低胰腺炎复发风险,且并不额外损伤健康的器官。对于结石梗阻位于胆胰管汇合部以上的患者,可避免急诊于乳头区外科操作,延期手术治疗。文献报道[7],对于伴发多器官功能障碍综合征的重症患者,急诊手术及麻醉的风险更大,死亡率更高,且术后并发症发生率高达14%~30%。我们体会,PTGBD术前无需特殊准备,于患者床旁局麻下既可完成,尤其适合高危复杂的患者,避免了搬动患者及麻醉风险,以及因科室间协调沟通耗时从而延误治疗时机,且费用相对低廉,节约医疗成本。尤其胆囊相较胆管操作空间更大,难度低,安全性更高。因此,对于急性胆管炎患者,如果病情不甚严重,PTGBD也可发挥引流优势,控制感染。
PTGBD也存在潜在风险,术后并发症如堵管、出血、胆漏、穿刺点疼痛等也多见于报道[8]。本组50例患者,实际操作中遇此类问题经对症治疗后均得到有效缓解,患者满意度良好。PTGBD虽然技术难度小,但穿刺过程并非一帆风顺。对于胆囊床小,腹胀、肠道内积气的患者,可供穿刺的路径受限,穿刺过程相对困难。我们体会,对于穿刺困难的患者,采取“慢-快-慢”的步骤,“慢”:缓慢进针,避免进针速度过快,失去超声的监视,发生进针过深或方向偏离,穿透胆囊或损伤重要胆道、血管等结构,从而造成不必要的副损伤。“快”:一旦见到胆汁快速送管,引流管进入胆囊腔后快速吸净胆汁,以减少胆汁外溢引起的化学性腹膜炎。“慢”:超声下反复确认引流管位置,妥善固定引流管;放慢心理预期,由于PTGBD引流的原理限制,胆汁需要肝脏分泌再经胆囊管至胆囊内,引流初始较少,往往应间隔8~12 h才能逐渐增多。引流管拔除也不可操之过急,尤其穿刺过程不顺利的患者,引流时间应在三周以上,使窦道形成充分,避免胆漏发生。对于带管时间长的患者,需注意引流管护理,避免引流管移位、逆行感染,定期予以生理盐水冲管,穿刺点附近皮肤也应加以护理,减少带管不适。对于长期引流量较大的患者,需进行胆汁回喝,以减少离子及消化酶的丢失。
本组50例患者虽然病情不同、病种较多,但均获得了满意疗效,这与适应证的合理选择有重要关系。应强调术前精确评估,结合PTGBD的引流原理与患者病情,综合考量选择胆道引流方式。由于PTGBD需经胆囊管引流肝脏分泌的胆汁,具有一定延迟性,因此对于需要胆道迅速减压引流的患者不适宜;且胆囊管需要保持通畅,对于胆囊管有结石嵌顿或压迫阻塞的患者效果也不甚理想。同时对于肿瘤贴近胆囊管开口的患者,也应考虑肿瘤进展导致引流短期失效,从而选择其他引流方式。
综上所述,PTGBD可作为减黄、降低胆道压力、控制炎症的有效手段,操作简便、易行,合理选择适应证,可最大程度地发挥微创化的优势,适于在基层医院开展。

