锰掺杂对纯化磷酸铁制备磷酸铁锂电池正极材料的影响
李光明,刘小瑜,张家玮,吴敏昌,乔永民,王利军
(1.上海第二工业大学 环境与材料工程学院,上海201209;2.上海杉杉科技有限公司,上海201209)
0 引言
磷化渣是金属表面预处理时,磷化过程的必然产物,它是一种淡黄色固体废渣。根据磷化渣中主要组分的不同,可分为锰系和铁系磷化渣。磷化渣的主要成分为磷酸铁(FePO4)、磷酸锰[Mn3(PO4)2)]和磷酸锌[Zn3(PO4)2],可能还含有少量Ca、Ni等金属离子[1-2]。磷化渣属于HW17类型危险固体废物,被记录在《国家危险废物名录》之中,对其处置需要经过严格的管控和处理[3]。目前的主要处理方式以填埋为主,但会对周围的土壤、水体和大气造成严重污染。如果能将FePO4或Mn3(PO4)2从磷化渣中提取出来,用作制备磷酸亚铁锂和磷酸锰锂正极材料的主要原料,既可以实现磷化渣的资源化综合利用,又可以降低磷酸亚铁锂正极材料的原料成本[4]。
现代经济的发展使得人们越来越重视锂离子电池应用,锂离子电池具有能量密度高、充放电电流大和循环寿命长等优点,使其成为本世纪最有竞争力和发展前景的动力源[5]。磷酸铁锂(LiFePO4)具有安全性能好、理论容量高和良好的倍率性能等优点,被认为是最有应用前景的锂离子电池正极材料之一[6-8],吸引了越来越多研究者的关注。LiFePO4电池可应用于储能设备、军事领域等,尤其在轻小型电子产品及电动车领域具有广阔的市场前景[9-11]。但LiFePO4电子电导率较低、锂离子扩散系数较小,导致其倍率性能较差,从而影响了LiFePO4在动力型锂离子电池中的发展和应用[12-14]。目前采用碳包覆、减小颗粒粒径、金属元素掺杂等比较成熟的方法来改善LiFePO4电子电导率低和锂离子扩散系数较小等问题[15]。其中金属元素掺杂可以明显提高LiFePO4正极材料的倍率性能,被认为是最有效的方法[16]。LiFePO4与其他锂离子电池正极材料(如LiMn2O4)相比,其工作电位平台偏低,而同为橄榄石型正极材料磷酸锰锂则具有较高的工作电位平台,具有更高的能量密度,被认为是最有希望取代LiFePO4的锂离子电池正极材料。Yuan[17]等利用固相反应法制备出了LiNi0.02Mn0.03Fe0.95PO4/C材料,其首次放电比容量为164.3 mA·h/g;PADHI[18]等发现,铁和锰共同占据橄榄石结构的八面体的4C位置,得到的Li(MnyFe1-y)PO4复合材料,具有较高的放电比容量。
本文利用酸洗水热过滤法对磷化渣提纯,在提纯后的FePO4中添加醋酸锰,并将其与碳源、锂源等混合,通过高温煅烧法制备得到LiFePO4/C复合材料[19-20]。主要研究了掺杂锰元素对LiFePO4电池的影响,对比了FePO4水合物与提纯后的FePO4分别作为原料制备LiFePO4/C正极材料对其电化学性能的影响。
1 实验部分
1.1 仪器和试剂
主要仪器:上海实验室乾正仪器SHB-95B循环水式多用真空泵,南京南大天尊仪器ND7-2L行星式球磨机,上海意丰电炉有限公司YFK40X440/120K-GC管式高温炉。前驱体材料的结晶度利用X射线衍射仪(XRD)测定,测试条件为:Cu/Ka射线(λ=0.154 18 nm),管电流40 mA,管电压40 kV,扫描范围10°~80°。使用日本HITACHI S-4800型扫描电子显微镜(SEM),观察材料的表面结构和元素成分变化。使用日本岛津720型能量色散X射线光谱仪(EDX)分析磷化渣中各物质的含量。使用武汉LAND CT-2001C测试仪测试扣式电池的电化学性能。
主要试剂:废弃磷化渣[主要成分为FePO4和Mn3(PO4)2,浙江省海盐某公司],醋酸锰(分析纯,质量分数为99.0%,国药集团化学试剂有限公司),无水葡萄糖(分析纯,质量分数为99.0%,国药集团化学试剂有限公司),浓磷酸(分析纯,质量分数为85.0%,上海凌峰化学试剂有限公司),碳酸锂(分析纯,质量分数为99.0%,国药集团化学试剂有限公司),磷酸二氢铵(分析纯,质量分数为99.0%,国药集团化学试剂有限公司)。FePO4·xH2O(分析纯,质量分数为99.0%,国药集团化学试剂有限公司)。
1.2 材料的制备
1.2.1 磷化渣提纯FePO4
磷化渣提纯制备FePO4是物理化学反应过程,主要反应包括:(1)大颗粒磷化渣不断变小和重结晶的重组过程;(2)在酸性环境下难溶的磷酸锌转化为微溶磷酸氢锌的提纯过程;(3)在强酸条件下可能生成可溶性的磷酸二氢锌。最后在酸性条件下,经过水热后,抽滤,可得到高纯度的FePO4。磷化渣反应过程中的主要反应式如下:

准确称取一定量的磷化渣,将磷化渣、水和浓磷酸按照质量比5:5:1的比例混合,搅拌均匀后于150°C的反应釜中恒温12 h,然后取出、过滤,将得到的滤料按上述步骤重复操作2~3次,最后将所得物料进行研磨、过筛后待用。
1.2.2 混料球磨
分别将 1.2.1得到的 FePO4·2H2O、自行购买的 FePO4·xH2O与碳酸锂,醋酸锰,磷酸二氢铵等原料以不同摩尔比混合,分别标 记 为 A、B、C。 A 为 nFePO4·2H2O:n碳酸锂=2:1.02,B 为 nFePO4·2H2O:n碳酸锂:n醋酸锰:n磷酸二氢铵=1.8:1.02:0.2:0.2,C 为 nFePO4·xH2O:n碳酸锂=2:1.02。分别在A、B、C中加入质量分数为15%的无水葡萄糖做为碳源和还原剂,利用无水乙醇作为分散剂,放入球磨罐中在600 r/min的转速下球磨4 h。将球磨后的混料放入80°C烘箱中恒温4 h,然后进行研磨,过200目筛后待用,样品标记为A1、B1、C1。
1.2.3 碳热还原
将得到的混料A1、B1、C1分别放入管式炉中,N2作保护气,从室温以6°C/min升温至730°C,恒温焙烧12 h,自然冷却至室温,取出样品,球磨粉碎,过200目筛,然后得到电池前驱体材料A2、B2、C2以制备电池。
1.3 电池组装
将A2、B2、C2分别与乙炔黑、聚偏四氟乙烯乳液以质量比为8:1:1混合,随后将混料在N-甲基吡咯烷酮溶剂中均匀混合,得到的混合物均匀涂布于铝箔上,完成3种电池正极制备。负极使用的是金属锂,隔膜为进口聚丙烯微孔膜,以1.0 mol/L的LiPF6为电解液(碳酸乙烯酯和碳酸二甲酯体积比为1:1,作为溶剂),在充满氩气的手套箱中组装成扣式电池A3、B3、C3。
1.4 电池测试
在常温下以不同的充放电倍率(0.1、1、2、4、6、8、10 C)在 2.5~ 4.2 V 电压范围内分别对A3、B3、C3进行首次充放比容量和容量保持率测试。
2 结果和讨论
2.1 EDX分析
通过EDX分析,对比磷化渣经过加酸水热过滤法提纯前后各物质纯度的变化,如表1 所示。从表中可以看出,提纯后 FePO4相对含量明显上升,从提纯前的81.6%提高到99.1%。Zn3(PO4)2相对含量明显下降,其除去率达到94.5%。Mn3(PO4)2、Ca3(PO4)2和其他杂质基本被去除,实际上由于该提纯方法对杂质离子的去除率较高,提纯后的磷化渣中Mn3(PO4)2、Ca3(PO4)2残留量极低,未被EDX检测出。磷化渣提纯前后的EDX测试结果表明,磷化渣经过加酸水热过滤法可除去磷化渣中的大部分杂质,得到高纯度的FePO4。
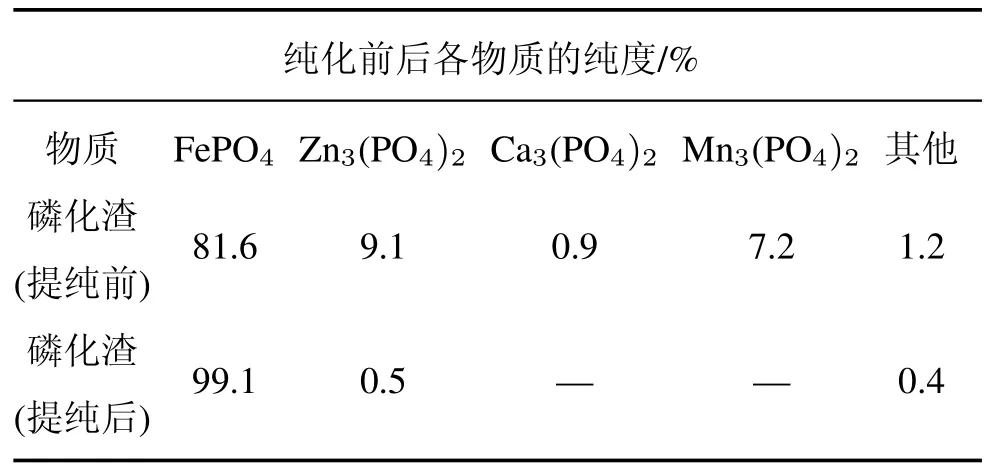
表1 磷化渣提纯前后各物质的纯度Tab.1 Purity of each substance before and after purif i cation of phosphating slag
2.2 XRD分析
图1所示为A2、B2、C2的XRD图。由图中可见,A2、B2、C2衍射峰的位置基本一致,表明制备的材料是正交晶系的橄榄石型结构。各样品的衍射峰均比较尖锐,且峰的强度较高,说明材料的结晶性能良好。其中,B2并未出现杂质峰,说明掺杂锰元素并未改变LiFePO4/C的晶体结构,可能是Mn取代了部分Fe位形成橄榄石形状的晶体结构。A2、B2、C2的XRD图中均未观察到锌及其化合物的衍射峰,说明锌元素没有在LiFePO4/C材料中形成杂相。根据表1分析,可能是由于Zn含量很低,低于XRD的检测最小浓度。

图1 A2、B2、C2的XRD衍射图Fig.1 XRD diffraction patterns of A2,B2and C2
2.3 SEM分析
A2、B2、C2的 SEM 如图 2所示,分别为图2(a)、(b)、(c)。磷化渣提纯得到FePO4与购买的FePO4所制成的LiFePO4/C(A2、C2)的微观形貌基本一致,说明可以大量地使用磷化渣提纯得到的高纯度FePO4来制备LiFePO4/C电池前驱体材料。B2和A2、C2的颗粒大小基本一致,且形状基本相似,有少量团聚,单颗粒排列更为紧密,其规则程度整体有所提高,说明B2中锰元素的掺杂使得晶体发生少量团聚,排列更为紧密和规则。

图2 A2、B2、C2的的SEM图Fig.2 SEM images of A2,B2and C2
2.4 电化学性能测试
2.4.1 首次充放电曲线及其效率
对A3、B3、C3电池进行恒倍率充放电测试,充放电倍率为0.1 C,首次充放电曲线如图3所示。由图3可见,A3、B3、C3的充电电压在3.4~3.6 V之间,而放电电压为3.4 V左右。A3与C3对比来看,可以发现使用提纯得到FePO4与购买的FePO4水合物制备的LiFePO4/C的首次充放电比容量和首次库伦效率基本相同,说明磷化渣提纯得到的FePO4可以作为制作LiFePO4正极的前驱体,这对于磷化渣的资源化利用具有重要意义。
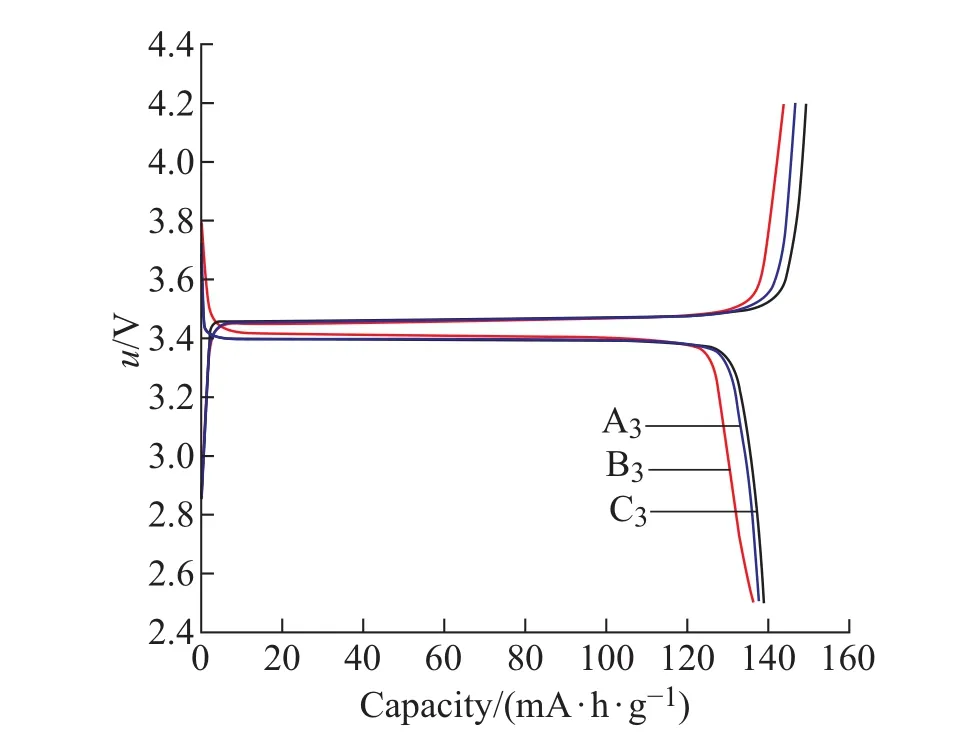
图3 A3、B3、C3的首次充放电曲线Fig.3 The initial charge-discharge curves of A3,B3and C3
A3、B3、C3的首次充放电及其效率如表2所示。可以看出,B3比A3、C3的充放电比容量稍低但相差不大,且首次库伦效率也很高。说明在低倍率下锰元素对LiFePO4/C的充放电比容量基本没有影响。B3的首次充电比容量为143.8 mA·h/g,首次放电比容量为136.3 mA·h/g,库伦效率高达94.78%。就充放电比容量来说,锰元素对于LiFePO4正极材料影响不大,因此磷化渣中含有的锰元素不用去除,可直接用于正极电池材料制作。
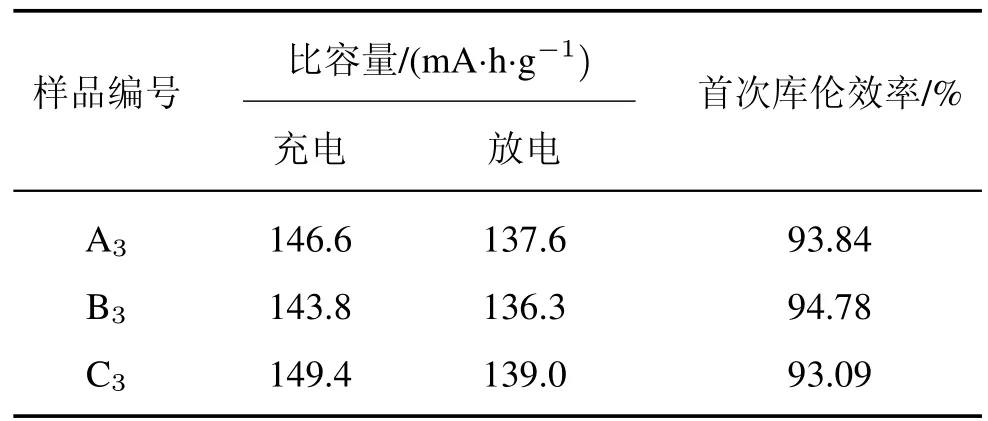
表2 A3、B3、C3的首次充放电及其效率Tab.2 The initial charge-discharge eff i ciency of A3,B3and C3
2.4.2 倍率性能分析
图4所示为A3、B3、C3的倍率性能曲线。由表2可见,A3、B3、C3在0.1 C较低倍率下,其首次放电比容量分别为137.6、136.3、139 mA·h/g,首次库伦效率分别为93.84%、94.78%、93.09%。而在0.1、2、4、6、8、10 C倍率下,B3的容量保持率均高于样品A3和C3的容量保持率,表明即使在高倍率下B3依然能够保持较高的容量保持率,具有较好的倍率性能。这可能是由于添加的锰元素可以增强橄榄石形LiFePO4/C结构的稳定性,有利于Li+在脱嵌过程中的界面迁移反应,有效地降低了电极反应动力学的限制,因此表现出了较好的倍率性能,也说明掺杂锰元素对于保持高倍率循环起到了很好的作用。

图4 A3、B3、C3的倍率性能曲线Fig.4 Rate capacity curves of A3,B3and C3
3 结 论
利用加酸水热过滤法对固废磷化渣提纯,以提纯得到的FePO4为主要原料,通过高温还原法制得LiFePO4/C正极材料。制得的3种电池中,添加锰元素的电池容量保持率最高,放电比容量衰减不明显,显示出了较好的倍率性能。通过实验得到如下结论:
(1)在橄榄石型LiFePO4中,锰元素取代了铁元素的位置,增强了其高倍率下电池循环效率,说明制备LiFePO4时少量锰离子掺杂对于电池循环过程中的容量保持率起到了积极作用
(2)利用固废磷化渣提纯的FePO4代替FePO4化学试剂所制备的LiFePO4/C正极材料与之具有相似的电化学性能,可实现磷化渣的资源化利用。

