开放手术与脊柱内镜下行椎板减压治疗退变性腰椎管狭窄症的临床对照研究
孙凤龙李军梁庆晨王宏庆刘祖耀李富董婕刁文博闫明
(1.首都医科大学附属北京康复医院骨二科,北京100043;2.周口协和骨科医院骨科,河南周口466000;3.吉林大学白求恩第一医院脊柱外科,长春130021)
腰椎管狭窄症(lumbar spinal stenosis,LSS)是临床常见的一种腰椎退行性疾病,根据2011年北美脊柱协会指南[1]和2014年中国专家组共识[2],LSS是由于先天或后天等各种不同因素所引起的椎管内部有效空间的减小,从而导致其内容物包括神经组织及血液循环受到不同程度的压迫,进而产生各种相应的临床症状。LSS尤其好发生于40岁以上的中老年[3],据报道该病的发病率为1.7%~10%[4,5]。LSS经保守治疗后症状改善率为15%~43%[6,7],但保守治疗无法解决局部的增生和压迫,随着病程的延长症状频繁发作甚至加重恶化,多数患者会选择手术治疗。手术治疗在缓解症状方面比保守治疗有更好的效果[8]。传统的椎板切除减压术一直以来被作为标准手术方法,并作为临床住院医师标准的培训术式[9]。近十年来随着脊柱内镜技术和脊柱微创理念的逐渐发展[10],以腰椎间孔内镜技术为典型代表的脊柱微创内镜技术逐渐得到了广泛的应用和普及。本研究探讨脊柱内镜下进行半椎板切除减压手术对单节段退变性中央型LSS患者的治疗效果。
1 资料与方法
1.1 临床资料
纳入标准:①通过影像学检查、体格检查和临床体征,最终确诊为退变性单节段中央型LSS;②有明显的腰背部或下肢症状,经诊断明确,病程6个月以上;③经保守治疗无效需进行开放手术或脊柱内镜手术。排除标准:①合并腰椎间盘脱垂、椎间盘突出伴严重钙化、重度腰椎滑脱、腰椎不稳者;②明显脊柱侧弯及其他类型LSS者;③既往有腰椎手术史患者;④无法耐受手术及恶性肿瘤等疾病患者;⑤合并严重创伤、精神疾患、具有吸毒史患者;⑥术前及术后临床资料不全、失访者。
根据上述纳入和排除标准,选择2016年1月至2017年7月收治的单节段退变性腰椎椎管狭窄症患者78例,其中行传统半椎板切除减压手术的32例为开放组,行脊柱内镜下椎板减压手术的46例为内镜组。两组患者的临床资料具有可比性(P>0.05,表1)。

表1 两组患者的临床资料比较
1.2 治疗方法
1.2.1 开放组:行半椎板切除减压术,患者取俯卧位,全身麻醉后进行手术,C型臂X线机定位病变节段,选择腰部后正中入路切开皮肤,逐层切开,沿患椎棘突逐层切开皮下组织、筋膜及肌肉,充分暴露后将棘上韧带纵形切开,充分暴露患侧椎板后显露患侧节段棘突和关节突,牵开患侧周围的骶棘肌,局部止血清理术区,术区显露清楚后进行半椎板切开减压。患侧切开减压的范围向内侧至棘突根部,向外侧至外侧关节突,清除增生的黄韧带和骨质。暴露硬膜和神经根,操作时注意保护神经和血管,咬除椎间盘黄韧带,凿除小关节内侧增厚的骨皮质,以期有效地扩大椎管。可以根据病情将手术床向对侧倾斜,对椎管进行更彻底的减压,对棘突根部甚至对侧椎板下的黄韧带进行切除,以进一步扩大椎管。探查患侧的神经根管和侧隐窝,充分减压患侧神经根。减压彻底后,观察无明显出血后留置负压引流管,缝合切口,术毕。术后1 d引流量低于50 ml时可拔除引流管,拔除引流管后可在助行器的保护下适度下地活动,术后14 d拆线,患者术后腰围支具保护3个月。
1.2.2 内镜组:采用脊柱内镜操作系统,进行脊柱内镜可视化下减压手术,患者取俯卧位,体表定位后,术区消毒铺单。局部麻醉后在C型臂X线机引导下定位,定位点选在关节突上1/3的位置(图1A、B),以导针为中心做1~2 cm切口,置入工作通道及内镜系统。内镜直视下使用可视环锯,第1锯在上关节突1/3的位置,去除患椎的部分上下关节突及部分上椎板,内侧切除至棘突根部,外侧最大范围可至关节突,根据压迫范围可酌情调整切开减压范围(图1C-F)。除第1锯外每锯要环取大半个骨质,一般占据环锯70%以上,以便于取出,直到骨块同环锯共同旋转表示骨块已环取成功(图1G、H)。将增生的黄韧带切除减压,显露硬膜及神经根。必要时可给予腹侧及后纵韧带减压,可使用射频止血,同时也可使用髓核钳修整神经根周围组织,以达到减压的目的。内镜下见术区局部无出血,检查神经根搏动好,缝合穿刺部位切口,术毕。术后1 d可适度使用助行器下地活动,1周左右逐渐开始腰背肌锻炼,患者术后腰围佩戴3个月。
1.3 随访计划及评价指标
手术临床指标评价:手术时间(min)、出血量(ml)、切口长度(cm)、卧床时间(h)及住院时间(d),选择两种术式手术中常规指标进行对比。
术后1、3、6、12个月以及之后每年进行随访,进行腰椎功能评价(JOA评分及ODI评分)、减压效果评价及腰椎稳定性评价。腰椎功能评价:手术前后功能评价采用腰椎JOA评分(Japanese Orthopaedic Association Scores,JOA)[11]和Oswestry功能障碍指数(oswestry disability index,ODI)[12]。
1.4 统计学方法
采用SPSS 17.0软件进行统计学分析,计量资料以均数±标准差表示,计量资料比较采用t检验;计数资料比较采用χ2检验,以P<0.05为有统计学差异。
2 结果
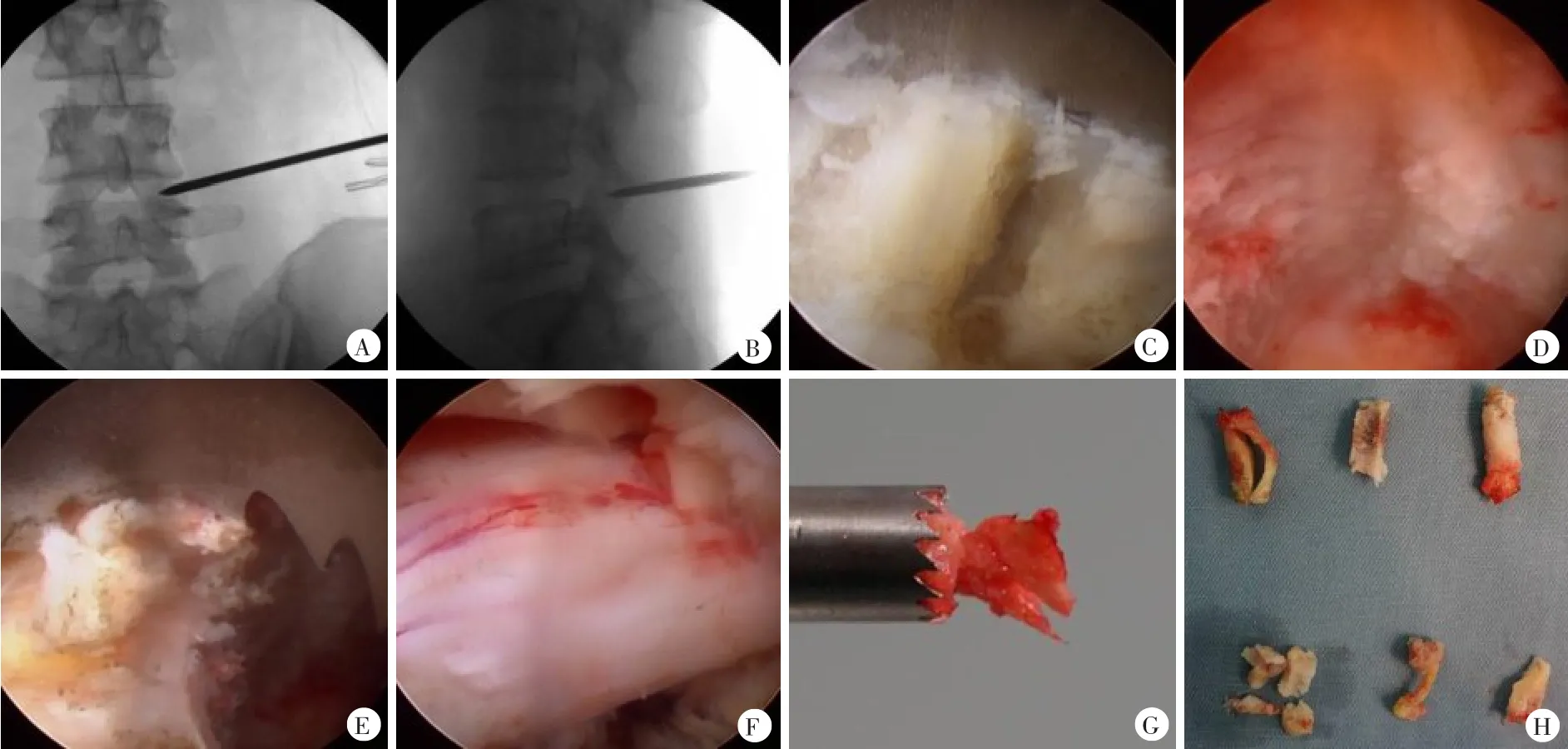
图1 典型病例,女,63岁,以L4-L5左侧为著,行脊柱内镜下减压手术
全部患者均获得随访,随访时间为12~24个月,其中开放组随访时间平均为(16.2±3.2)个月,内镜组的随访时间平均为(16.6±3.0)个月。内镜组典型病例见图2。
2.1 手术临床指标评价
两组患者在手术时间、出血量、切口长度、卧床时间和住院时间方面,具有统计学差异(P<0.05,表2)

表2 两组患者的手术临床指标的比较
2.2 JOA评分及ODI评分比较
术前、术后3个月、术后6个月、术后1年及末次随访的JOA评分和ODI评分,两组均未见统计学差异(P>0.05,表3);而术后1个月的JOA评分和ODI评分,两组比较有统计学差异(P<0.05,表3)。
3 讨论
3.1 LSS的传统手术治疗
退变性LSS主要是由于日常活动中腰椎反复活动、长期劳损,导致局部退变所致。LSS主要包括腰椎中央管、侧隐窝狭窄以及椎间孔通道距离缩小等常见类型,其发病机制主要是由于随着年龄的增长和椎间盘的退变,导致椎体间的韧带松弛、椎间隙的高度丢失、局部力学结构发生改变,进而引起椎间小关节间的应力增加、重叠和摩擦增大,导致小关节、关节囊和黄韧带的肥大、增生和钙化,严重者导致纤维环的钙化、椎体后缘骨赘形成。多种因素作用下致椎管容积的变小,最终形成LSS。
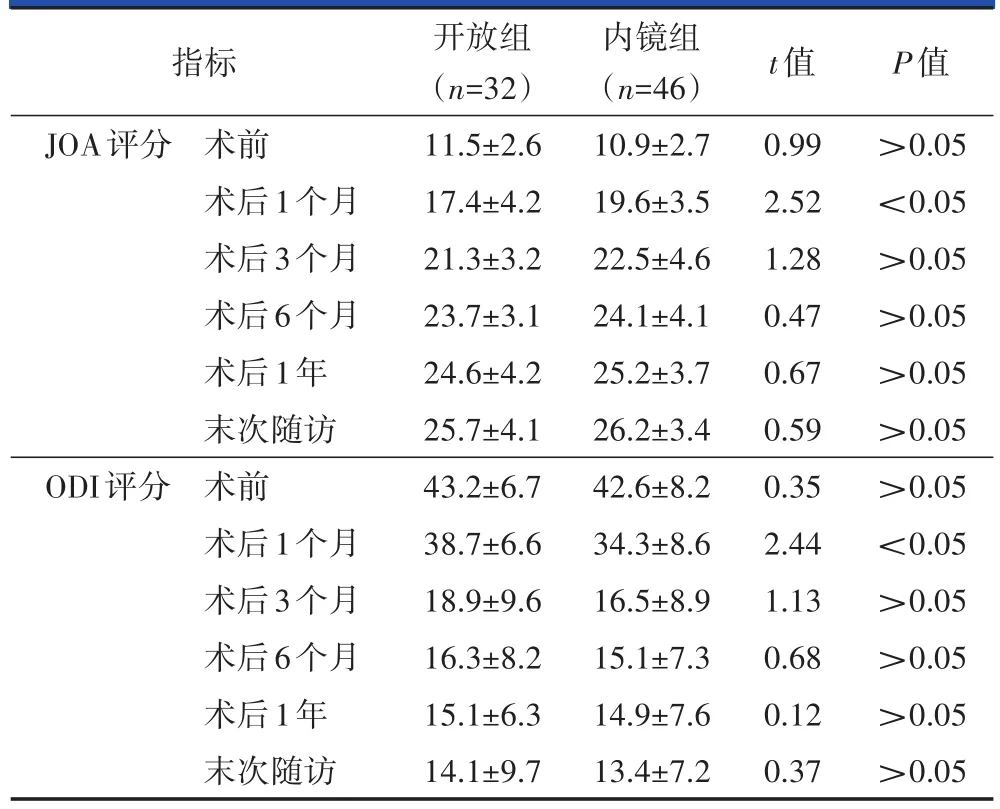
表3 两组患者的手术前后JOA评分及ODI临床指标的比较

图2 典型病例,男,65岁,L3-L4椎管狭窄症,行脊柱内镜下减压手术
尽管LSS在手术时机和方案的选择上存在争议,但手术治疗的效果和地位获得了广泛的认可[13-18]。传统开放手术治疗主要包括椎板切除减压术、椎板切除减压术+植骨融合内固定术等。其中椎板切除减压手术是治疗LSS最基本的术式,主要又分为椎板间开窗术、全椎板切除减压术和半椎板切除减压术等。各种类型的椎板切除减压手术虽能达到彻底的减压效果,但开放减压术式对椎旁软组织进行损伤性操作,会引起周围肌肉失神经支配和局部萎缩,术后可能导致持续性腰背部疼痛甚至腰椎不稳等缺点。此外,LSS患者在行椎板切开减压术时,是否联合融合术目前仍存有争议[19,20]。有研究指出,附加融合手术对于远期临床疗效并无明显改善,并且可能导致邻近节段发生退变,术后可导致较高的翻修率[15,21-23]。目前开放手术治疗LSS的方法较多,但尚未形成较为一致的共识。
LSS的手术治疗目的主要还是解除椎管内致压因素,达到椎管和神经根的彻底减压,恢复椎管有效容积。全椎板减压手术的手术创伤较大,术后有形成较大血肿和死腔的风险,导致硬膜外瘢痕组织的形成,由于切除棘突、棘间和棘上韧带等脊柱后方结构,可导致力学结构的破坏,术后往往会出现腰痛症状[24],最终导致腰椎手术失败综合征的发生[25]。半椎板切除减压术在有效满足椎管容积效应的基础上,由于创伤较小,能够有效保留棘上、棘突韧带,并且对脊柱后方骨性结构破坏较小,保证了脊柱术后的稳定性,相比全椎板切除减压手术可降低术中及术后的并发症发生率[26]。半椎板切除减压术能够有效治疗LSS,特别是针对术前无明显脊椎滑脱的患者,其术后功能改善效果与全椎板切除手术相似,而且再手术率低于全椎板切除手术,所以此类患者行半椎板切除减压手术可以替代全椎板切除减压手术[27]。
3.2 LSS的脊柱内镜手术治疗
近年来随着脊柱生物力学理论的发展、手术器械和技术的进步,脊柱内镜手术因其手术创伤出血少、住院时间较短及术后恢复较快等优势[28],逐渐在腰椎疾病的治疗中取得了重要地位,尤其在治疗腰椎间盘突出症方面已逐渐被接受[1,2,10]。然而在LSS的治疗上依然存在适应证把握不准确、并发症发生率高等问题,并未形成统一的共识。
目前临床中常用的脊柱内镜技术包括后路椎间盘镜技术和经皮椎间孔镜技术,两种脊柱内镜技术进行腰椎管减压手术有着不同的手术入路和手术适应证选择。后路椎间盘镜技术在操作中手术视野较小、减压的操作范围有限、处理增生的骨性组织比较困难,只能进行LSS的有限减压。经皮椎间孔镜技术是目前临床上常用的脊柱内镜技术,该技术基于经皮穿刺技术和脊柱内镜技术,能够结合射频或激光等技术的优势,被广泛应用于各种腰椎疾病的治疗。目前较为常用的两种经皮椎间孔镜技术为YESS和TESSYS技术:YESS技术进入点选择椎间孔内Kambin安全三角区进入椎间盘;TESSYS技术则选择椎间孔下方作为进入点,能够远离出行神经根和背根神经节。这两种技术均为腰椎后外侧经椎间孔入路,进入椎管后进行松解减压,由于椎间孔局部解剖结构所限,对于LSS需要行椎间孔扩大成形术治疗,但无法有效松解减压背侧。鉴于椎间孔镜技术治疗的局限性,虽然可用于有根性症状的侧隐窝或神经根管狭窄的患者,但并不适于中央管狭窄的患者。此外,椎间孔镜技术学习曲线较为陡峭[29,30],与治疗腰椎间盘突出症相比,治疗LSS的手术操作更困难、手术时间更长[31]。
3.3 脊柱内镜下减压治疗LSS
3.3.1 开放手术思路下脊柱内镜的椎板减压:传统介入技术基于穿刺针,先进入靶点,由内到外进行操作,是一种穿刺思路下进行的盲视技术。目前临床中常见的椎间孔镜操作也是基于“穿刺进椎间孔-穿刺进椎管”穿刺思路下进行的可视技术,由于椎间孔的限制,其可视也是一种有限的可视,无法达到硬膜囊背侧的减压,操作者对于精准穿刺的掌握需要丰富的经验,也具有一定难度和风险。传统椎间孔镜技术和开放手术的博弈就在于是否全程可视和逐层切开,在熟练进行脊柱内镜操作和传统开放椎板减压手术的基础上,将两者的优势结合,使用脊柱内镜进行椎板减压的操作,能够达到减压过程的全程可视,实现开放手术思路下的逐层入路、逐层切开,并最终达到椎板减压的目的。
开放手术思路下的脊柱内镜操作是一种非穿刺思路,操作上遵循由外而内、逐层入路的开放手术思路。患侧小关节背侧作为脊柱内镜减压操作的起点,在内镜可视下直接看到小关节背侧骨质,相对安全性更高,第一视野为浅层软组织和椎板或关节突的骨性结构,而非椎间孔,使用可视环锯经由“骨-韧带-神经-减压”逐层入路。内镜镜头相当于术者的双眼,而内镜器械取代了传统开放手术器械,有效避免了盲视穿刺入路的各种风险。找到和显露出骨性标志物也是骨科医师最擅长和习惯的操作步骤,在开放手术思路指导下的脊柱内镜操作能够达到术野的有效显露。
3.3.2 脊柱内镜下的椎板减压的手术操作:可根据患者情况选择局部麻醉和全身麻醉。局部麻醉中患者基本全程耐受,疼痛感不明显。全身麻醉的风险也较小,手术全程在可视化下进行,镜下高分辨率,手术视野被放大数十倍,可基本达到直接减压、精准减压。并且水介质较空气介质出血明显减少,视野更加清晰,特别是对于精细手术,能够有效避免对神经的损伤。如果患者条件允许则选择局部麻醉下操作,患者可随时和医护进行沟通,毕竟患者清醒状态下的局部麻醉手术是最好的监护。
该术式在定位过程中对定位范围不求精准,定位点选在关节突上1/3的位置,该位置1 cm2范围内均可,对术者的要求不高,能够有效减少透视次数,熟练操作者于术前进行C型臂X线机的正侧位透视,只需2次透视便可确定位置,可达到按需减压、自由减压的目的。有研究指出,腰椎一侧关节突手术切除范围<1/2时,对于腰椎生物力学稳定性无显著改变;而切除范围>1/2时,腰椎的局部力学稳定性会遭到破坏,腰椎旋转及侧屈活动度明显增加,生物力学稳定性明显降低[32]。该术式操作中只对关节突上1/3做切除,关节的下2/3则予以保留。
在使用可视环锯开窗时,第1锯很关键,位置一般选择在上关节突1/3位置,选择后外侧骨性入路,第1、2锯相对较难开窗,第2锯根据具体情况可选择第1锯的同侧或对侧,第3、4锯相对好操作,可根据肥厚的黄韧带变换环锯开窗减压的范围。4锯后达到类方形的开窗是最理想的减压操作,相当于脊柱内镜下的半椎板切开减压术,实际操作中可根据具体需要来增加锯数。每锯要环取大半个骨质,一般占据环锯70%以上,以便于取出,直视下环取时,直到骨块同环锯共同旋转表示骨块已环取成功。实际操作中,环锯在环取过程中,骨性物质后面是黄韧带,在骨性结构即将通透时,会有特殊的手感,如同矿泉水瓶盖拧开一刹那的“开瓶盖感”,内镜直视下此时骨块会与环锯共同旋转。黄韧带起到了保护作用,取出的骨块背后可见附带黄韧带。术者轻旋几圈后取出环锯,骨块会因摩擦力而随着环锯带出。在熟练掌握内镜操作技术的基础上,结合开放外科彻底减压理念,用可视环锯做患侧椎板开窗,开窗后清除黄韧带、神经内膜及硬膜边缘,进入硬膜腹侧,去除腹侧致压因素。减压范围头侧可至上位椎弓根下缘,外侧可到椎间孔外口,尾侧可到下位椎弓根上缘,对侧可至棘突中线位置甚至超越棘突中线位置。实现对目标狭窄的椎管背侧腹侧及侧隐窝的全程松解减压。适当扩大减压范围使神经充分减压对于椎体失稳和滑脱的影响不大[33]。
3.3.3 脊柱内镜下椎板减压的临床效果:根据侧后入路脊柱内镜下椎板减压技术,在最大限度保护脊柱生理结构完整性的基础上建立骨性通道,达到可视化减压的目的。研究显示该术式在切口长度、出血量方面要优于传统半椎板切开减压手术(P<0.05),体现了该术式创伤小、破坏小的优点。该术式能够有效保留前柱、中柱完整性。使用逐层入路技术,术中能够按照所需调整内镜操作范围进行开窗减压。脊柱内镜下开窗减压手术视野放大数十倍,视野更清晰,从而降低了神经损伤的风险,能够对目标硬膜囊和神经根精准减压。调整镜头能够观察到开放手术无法达到的视野盲区。脊柱内镜减压与传统开放手术减压范围均在2个椎弓根之间,能够在有效减压的同时,有效避免因为操作区狭小而导致过度牵拉神经,减少对神经根造成伤害[34]。此外,该术式使用局部麻醉,不仅降低了围术期风险,在进行开窗减压同时观察患者的下肢反应,较以往开放手术使用全身麻醉能够保证治疗安全和有效。该术式在卧床时间和住院时间方面要优于传统的半椎板切开减压手术(P<0.05),也体现了内镜手术更安全、恢复快等特点。所以该术式是一种行之有效、易于掌握的微创手术方式,以期最终达到手术方法可重复性和治疗效果标准化的目的。
本研究显示,该术式在手术时间方面要长于传统半椎板切开减压手术,主要因其术中需要定位,操作比传统开放手术更为复杂,并且作为一种新术式,也受到术者熟练程度和学习曲线的影响。不过在研究的后期阶段,随着解剖结构和手术操作的熟练,能够有效避免不必要的操作,手术时间呈现出下降趋势,内镜手术操作时间能够保持在30~50 min。腰筋膜通过本体感觉及痛觉两者支配,分布疼痛相关的神经组织,能够导致腰背痛[35]。术后早期腰椎功能内镜组优于开放手术,可能由于内镜手术切口小、损伤部位只局限内镜通道,对周围组织损伤降到很低程度;而开放手术切口大,对局部组织进行分离,并且器械牵拉撑开,对椎旁肌和周围软组织造成损伤,局部组织需要重新愈合重建,也不利于术后腰部功能的康复训练,所以术后早期的腰椎功能评价方面,术后1月JOA评分及ODI评分,内镜组要优于开放组(P<0.05),表现出该技术创伤小、术后恢复快等优点。在术后3月直至末次随访中,随着术后腰部功能的恢复和康复练习,开放组在术后3个月后,术区韧带和肌肉已重建和恢复,腰部力量和稳定性也渐恢复,两组JOA评分及ODI评分趋于一致(P>0.05)。也体现出在术后中长期疗效方面,该技术能够达到和开放手术的一样临床效果。由此可见,脊柱内镜下椎板减压术式的各项临床手术指标令人满意。
在平时手术过程中,对于常见的腰椎椎管狭窄症合并腰椎间盘突出患者,以及其他类型椎管狭窄患者,该术式同样取得良好的效果。对于腰椎椎管狭窄症合并椎间盘突出钙化、椎间隙高度丢失、完全性椎管狭窄等病例,该技术作为一种微创技术也取得较为不错的治疗效果,但由于病例数量相对较少少目前未纳入系统研究。此外对于合并腰椎不稳的疗效方面也尚存争议[36]。考虑到一致性和可比性,本研究选择单节段中央型腰椎管狭窄症患者进行对比研究,并且得到了较为满意的治疗效果。随着手术例数和手术类型的增多,会逐渐纳入其他类型腰椎管狭窄进行研究,使得内镜下可视化减压这项技术的研究更加深入和系统化。
相信随着操作技术和器械的不断改进,在脊柱内镜椎板下减压技术治疗腰椎管狭窄症的技术会越来越得到改进和完善。

