PFNAⅡ与LCP DHS Blade治疗股骨转子间骨折的生物力学研究*
周天健,黄文俊,姜 未,邹回春,胡新佳(深圳市人民医院/暨南大学第二临床医学院骨关节科,广东518020)
髋部骨折是全世界面临的重大公共健康问题之一。据估计,2000年全世界大约有160万例髋部骨折。随着人口预期寿命延长,到2050年,预计髋部骨折的数量可达630万例[1]。股骨转子间区连接股骨头颈和股骨干,生理应力集中而复杂,骨折后常出现显著移位,这些解剖特点决定了转子间骨折患者不良结局发生率较高,通过外科手术复位并使用内植入物固定转子间骨折是骨科界普遍的共识[2]。用于转子间骨折的内植入物总体分为2类,以滑动髋螺钉为代表的髓外固定系统和以头髓钉为代表的髓内固定系统[3]。然而,术后手术侧肢体是否能即刻完全负重行走仍然存在争议。临床实践中,由于存在个体差异,加上人体结构的复杂性、人体运动的多样性、测量仪器的局限性及伦理问题,临床很难直接测量人体行走运动的力学参数。因此,这个问题需要通过生物力学研究来解答。本研究选择了2种具有代表性的植入物:股骨近端抗旋髓内钉(PFNA⁃Ⅱ)和带螺旋刀片的锁定加压钢板与动力髋螺钉(LCP DHS Blade),分别建立手术固定稳定型转子间骨折(AO分型31⁃A1型)的三维几何模型,在计算机仿真人体动力学条件下进行有限元分析,了解骨折与内固定物复合体的生物力学分布情况,从而为临床术后康复提供理论依据。
1 资料与方法
1.1 资料
1.1.1 一般资料 选取2017年4月本院女性患者1例,年龄82岁,身高150 cm,体重50 kg,既往身体健康,无骨关节疾病及重大创伤史,因摔伤致左股骨转子间骨折入院。患者知情并签署知情同意书。
1.1.2 实验设备及系统 PFNAⅡ系统和LCP DHS Blade系统(包含4枚直径4.5 mm锁定头螺钉)各1套(DePuy Synthes公司,美国)、16排螺旋电子计算机断层扫描(CT)机(Simens公司,德国)、3.40 GHz CPU 及16 GB内存计算机(Asus公司,中国),Geomagic Studio系统(Geomagic公司,美国)、Simpleware6.0系统(Simpleware公司,英国)、Anybody5.3系统(AnyBody Technology公司,丹麦)、Abaqus6.12系统(Dassault Systems公司,法国)。
1.2 方法
1.2.1 股骨和植入物几何模型生成 使用CT扫描机对志愿者双侧股骨全长进行水平扫描,层距0.4 mm,扫描范围为髋臼至胫骨平台,最终得到521幅断层扫描图像,以Dicom格式保存;再使用CT扫描机分别对PFNAⅡ系统和LCP DHS Blade系统进行水平扫描,条件同前,扫描图像以Dicom格式保存;将CT扫描图像导入Simpleware,分割图像并对图像进行优化;在Geomagic Studio系统中进行装配,共形成2个股骨⁃植入物复合几何模型。见图1、2。
1.2.2 模型装配 将股骨模型分为皮质骨部分和松质骨部分,按照转子间骨折AO分型31⁃A1亚型分割股骨近端,并对图像进行优化,建立股骨⁃PFNAⅡ固定模型和股骨⁃LCP DHS Blade固定模型,并输出为stl格式文件。见图 3、4。
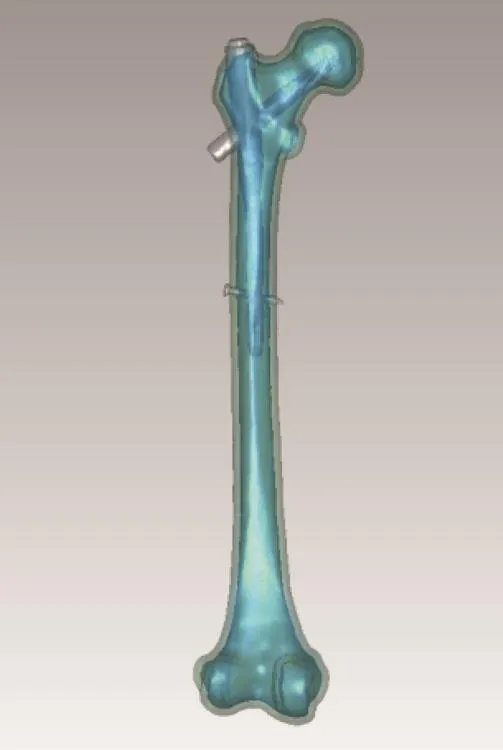
图1 股骨-PFNAⅡ固定模型示意图
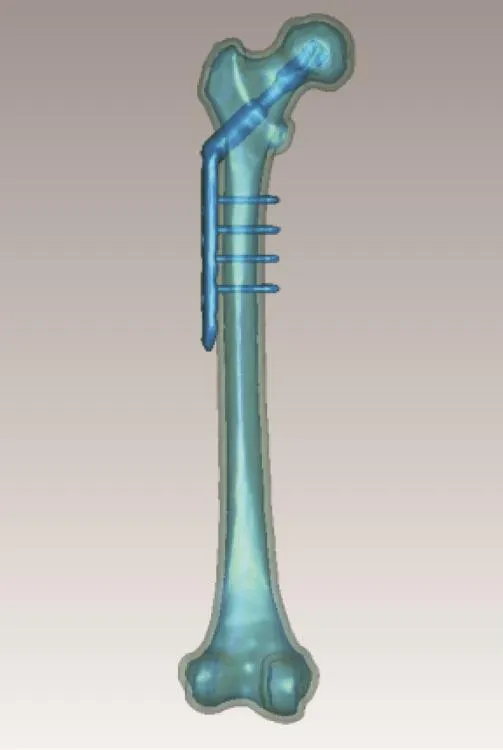
图2 股骨-LCP DHS Blade固定模型示意图

图3 AO 31⁃A1型骨折⁃PFNAII固定模型示意图

图4 AO 31⁃A1型骨折⁃LCP DHS Blade固定模型示意图
1.2.3 网格划分 将上述stl格式文件分别导入Simpleware的FE模块中,进行网格划分,并输出inp格式的文件,完成后的三维网格模型如图5所示,三维网格模型节点及单元数如表1所示。

图5 AO 31⁃A1型骨折⁃PFNAII固定三维网格模型
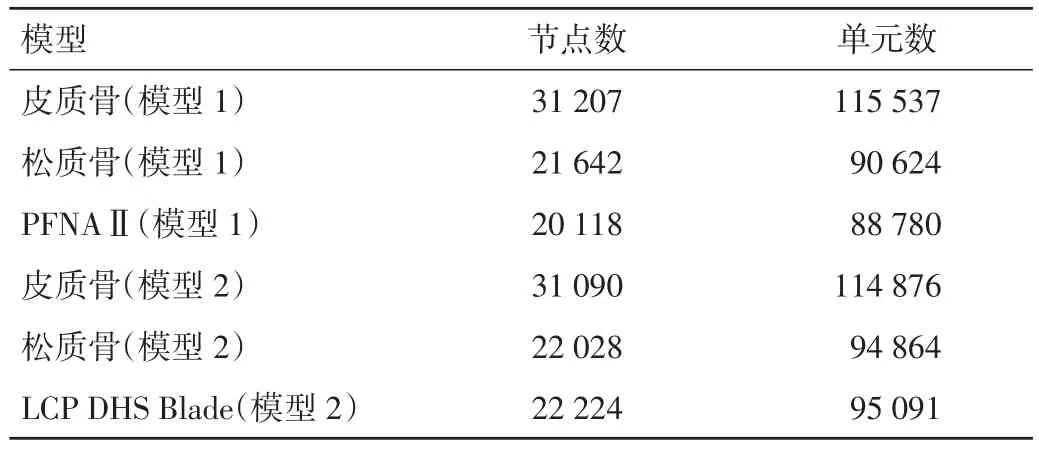
表1 三维网格模型节点及单元数(n)
1.2.4 股骨⁃植入物复合几何模型配准 从Anybody系统中选择与研究对象匹配的正常人体股骨模型,并与股骨⁃PFNAⅡ固定模型、股骨⁃LCP DHS Blade固定模型一同导入Geomagic Studio系统中,将2组模型进行比对配准,使得股骨⁃植入物复合几何模型与Anybody正常人体股骨模型的位置一致。见图6。
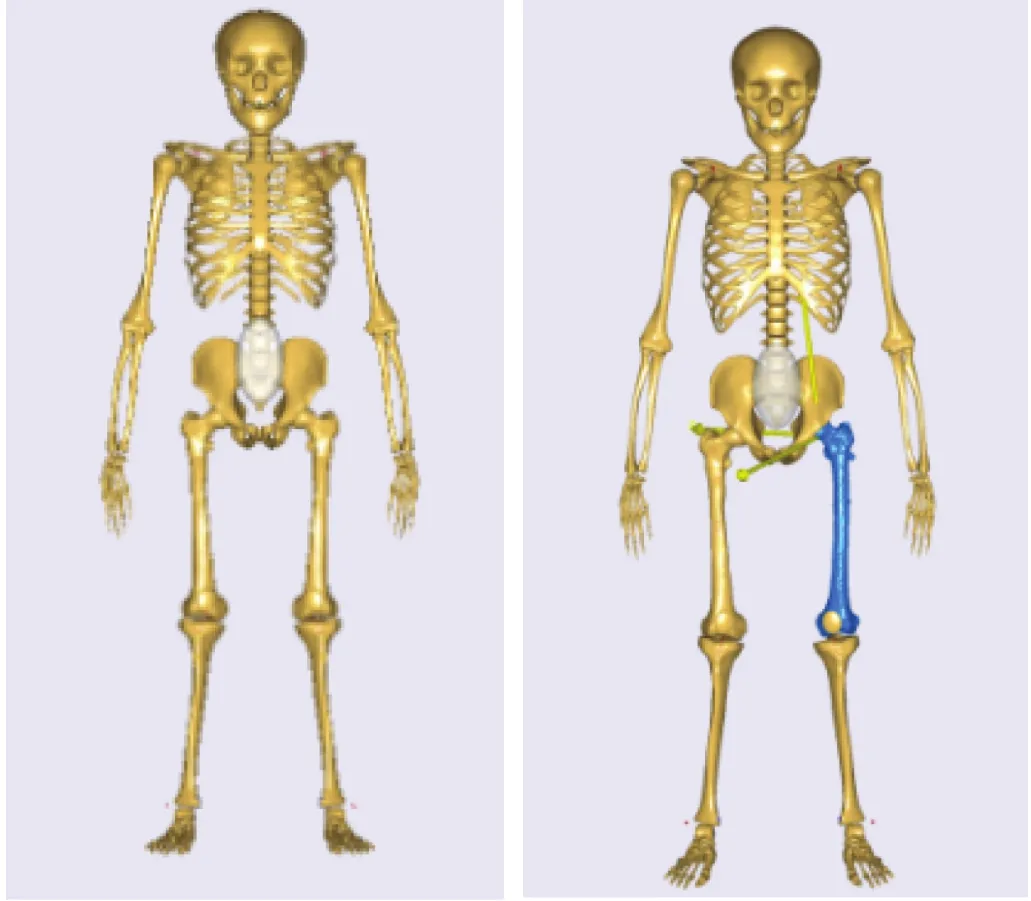
图6 在Anybody软件中用AO 31⁃A1型骨折⁃PFNAII固定模型替换正常股骨模型
1.2.5 步态仿真 将配准好的股骨⁃PFNAⅡ固定模型、股骨⁃LCP DHS Blade固定模型分别导入Anybody系统中,进行步态仿真分析,计算人体在正常步态情况下股骨周围肌肉力的大小。仿真过程如下:将左脚跟着地到下一次左脚跟着地前定义为一个步态周期,将步态周期分成20个分帧动作,从中选取5个典型姿态,代表了右下肢站立相初期、右下肢站立相中期、右下肢站立相末期、右下肢摆动前期的分割点,依次为左足跟着地(第3帧)、左足趾离地(第6帧)、右全足底着地(第11帧)、左足跟着地(第15帧)、右足趾离地(第18帧)。见图 7。
1.2.6 载荷和边界条件 将在Anybody中得到的随时间变化的肌肉力导入Abaqus中,约束股骨远端表面上的有节点,将其自由度全部固定。本次仿真总共对股骨施加了360个不同载荷,其中包括3个膝关节关节力和357个肌肉力,这些载荷均通过AnyBody所输出的边界调节进行施加。见图8。
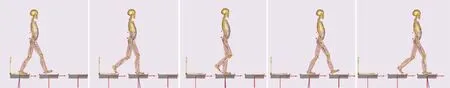
图7 步态仿真过程中的5个典型姿态

图8 载荷和边界条件
1.2.7 设置接触关系及材料属性 (1)接触关系:骨折断面间设置面与面互相接触,接触面间的摩擦系数为0.2;在设置器械与股骨的接触关系时,首先通过布尔运算,用股骨模型减去器械模型,在股骨中形成放置器械的孔洞,然后在Abaqus中设置器械与股骨之间通过绑定进行交互。(2)材料属性设置:股骨由皮质骨和松质骨构成,其中皮质骨弹性模量为16800 MPa,泊松比0.3,松质骨弹性模量为620 MPa,泊松比0.29;PFNAⅡ和LCP DHS Blade的弹性模量均设置为110000 MPa,泊松比为0.3。
1.2.8 有限元分析 采用Abaqus系统进行有限元分析。
2 结 果
采用PFNAⅡ固定的稳定型股骨转子间骨折复合模型在步态周期中5个典型姿态下的应力云图,见图9。使用LCP DHS Blade固定的稳定型股骨转子间骨折复合模型在步态周期中5个典型姿态下的应力云图,见图10。PFNAⅡ系统和LCP DHS Blade系统在步态周期中5个典型姿态下的Von Mises等效应力峰值曲线,见图11。PFNAⅡ系统和LCP DHS Blade系统在步态周期中右足跟着地(姿态4)时的应力达到最大值,见图12。
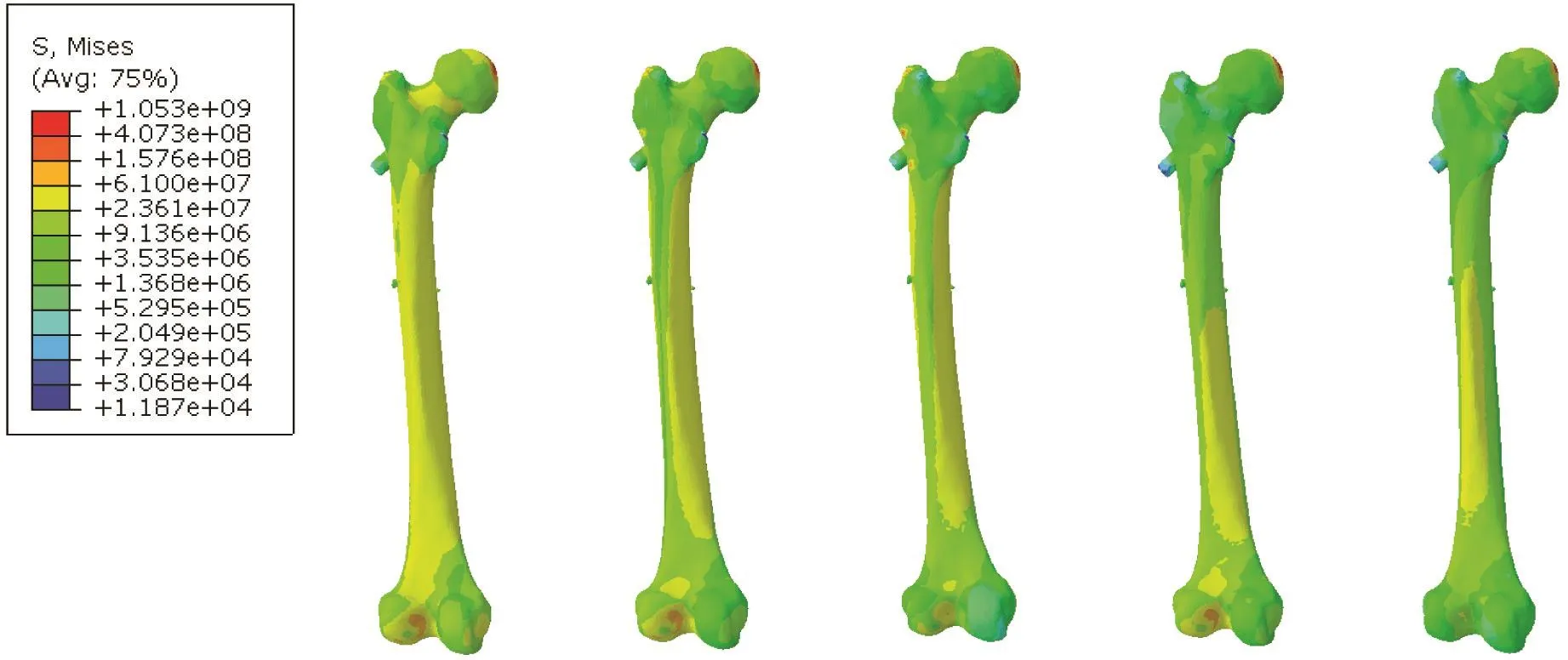
图9 PFNA⁃II固定模型在典型步态下的应力云图
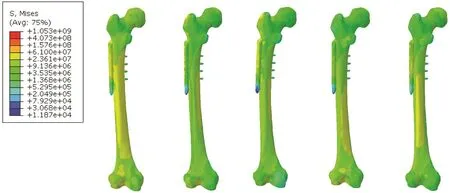
图10 LCP DHS Blade固定模型在典型步态下的应力云图
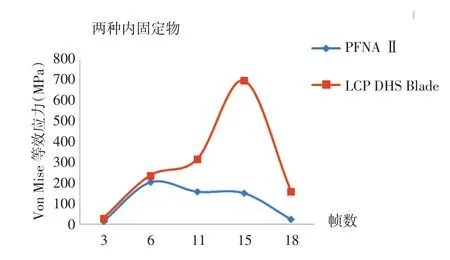
图11 PFNAⅡ和LCP DHS Blade在5个典型姿态中的Von Mises应力曲线
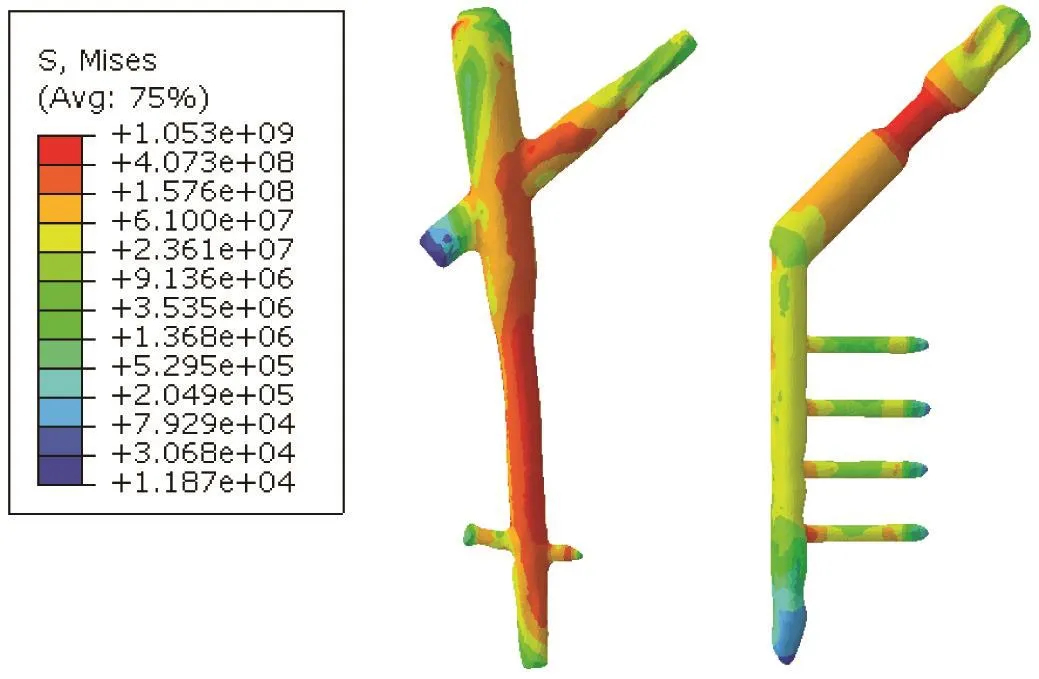
图12 PFNAⅡ和LCP DHS Blade在步态周期中姿态4时的应力云图
3 讨 论
骨科生物力学是以骨骼肌肉系统为对象,利用生物力学的方法将工程原理,尤其是机械力学原理应用于临床医学,解决骨科问题,是生物力学领域中相当重要的分支学科[4]。标本试验是传统的骨科生物力学研究方法,针对不同临床问题构建不同的人体骨骼与关节标本模型,通过材料力学试验机或其他加载设备,驱动标本模型模拟人体活动,然后通过二维或三维影像、传感器等手段对模型的结构稳定性、材料强度、力传导等指标进行观测和分析[5]。这些方法存在以下缺陷:(1)样本量偏小;(2)样本之间骨质量难以做到一致;(3)骨折不能精确模拟自然骨折类型;(4)无法全面揭示样本内在应力的变化。随着计算机三维图像重建和有限元分析方法的发展,有限元虚拟仿真实验可以弥补标本实验的不足。将计算机仿真技术与有限元数值计算相结合,针对临床研究对象建立骨科三维有限元模型进行虚拟仿真实验,已成为骨科生物力学研究的重要手段[5]。骨科有限元分析的效果(即分析结果与真实的相似程度)很大程度上依赖于边界条件的设置。在人体正常行走过程中,股骨近端的受力环境相当复杂,许多生物力学研究的不足之处在于仅将股骨承受的主要外力简化为集中力,并没有考虑肌肉对股骨的应力[6⁃7]。
AnyBody是一款新颖的计算机辅助人机工程学和生物力学分析软件系统,可以通过计算机语言的编辑来模拟人体不同的动作,如行走、奔跑、上下阶梯、抬举重物等。通过逆向动力学原理,将完成动作过程中所感兴趣的肌肉力、关节力、位移等感兴趣数据进行计算并导出,在第三方软件上使用。该系统包含目前最为完整的骨肌系统数据库,能真实地模拟人体的生物力学环境,达到最大限度的仿真效果[8]。本研究采用AnyBody系统,在股骨三维有限元模型上加载了357个肌肉力和3个关节力,随着身体姿态的不同,这些力的大小、方向都会改变,因此可以在有限元分析软件上获得不同步态情况下应力结果,更接近人体行走时的真实情况。在材料属性方面,本研究采用了骨科有限元研究的常规设置方法。董双鹏等[9]认为,在准静态载荷状态下可以将皮质骨与松质骨都看成为具有线弹性、各向同性的材质。本研究建模时假设股骨由连续、均质、各向同性的线弹性皮质骨和松质骨构成,其中皮质骨弹性模量为16800 MPa,泊松比0.3,松质骨弹性模量为620 MPa,泊松比 0.29;PFNAⅡ和 LCP DHS Blade 亦假设为连续、均质、各向同性的线弹性Ti⁃6AI⁃4V材料,弹性模量均设置为 110000 MPa,泊松比为 0.3[10⁃11]。
从最终的应力分析结果来看,在正常步态周期各个典型姿态载荷条件下,使用PFNAⅡ和LCP DHS Blade固定的稳定型股骨转子间模型均没有出现明显应力集中的区域。这说明对于稳定型股骨转子间骨折(AO分型 31⁃A1),不论采用 PFNAⅡ还是 LCP DHS Blade固定,在正常行走情况下,股骨都不容易出现骨折移位或内固定穿出的情况。单独观察内固定物的应力分布情况,在一个步态周期中,2种植入物的应力均呈现双波峰分布,第一个波峰出现在右下肢支撑相中期,第二个波峰出现在右下肢支撑相末期,PFNAⅡ的最高峰值出现右下肢支撑相中期,为230.6Mpa,LCP DHS Blade的最高峰值出现在右下肢支撑相末期,为697.9 Mpa。而 Ti⁃6AI⁃4V 材料的屈服强度为 811~904 MPa[12],二者应力峰值都没有达到材料的屈服强度,说明内固定失效的风险不大。以上结果说明对于稳定型股骨转子间骨折(AO分型31⁃A1),不论采用PFNAⅡ还是LCP DHS Blade固定,术后手术侧肢体都可以完全负重行走。
对比2种内固定物⁃股骨复合模型的应力分布情况:(1)在PFNAⅡ固定的股骨模型中,PFNAⅡ的最大应力范围分布在主钉的纵轴,力量分布均匀,股骨部分最大应力范围分布于股骨内、外侧,分布均匀。(2)在LCP DHS Blade固定的股骨模型中,LCP DHS Blade固定最大应力分布主要位于主钉的头螺旋刀片的螺杆部分和4孔钢板远端第4枚螺钉的基底段,且出现应力集中现象,其中股骨上的最大应力分布也分布于内、外侧,但是分布不均匀,分布限于局部。2组在左足站立相初期至中期过程中,PFNAⅡ最大应力变化不明显,LCP DHS Blade最大应力增加明显,PFNAⅡ最大应力均小于LCP DHS Blade;在对侧承重期过程中,2组中器械和股骨的应力均较整个站立相明显降低,2组中股骨的应力分布类似,PFNAⅡ的最大应力分布主要位于主钉的纵轴,力量分布均匀,LCP DHS Blade的最大应力分布主要位于螺旋刀片的螺杆部分和锁定加压接骨板远端第4枚螺钉的螺杆基底段,其中LCP DHS Blade的最大应力明显大于PFNAⅡ的最大应力。这是因为PFNAⅡ的主钉位于股骨干髓腔内,与偏心固定的LCP DHS Blade比较,PFNA的防旋刀片力臂短,所产生的力矩也较小,从应力分布云图上可以看出,防旋刀片上所承受的应力可以迅速被传递并分解至髓内钉和股骨干皮质,以及通过髓内钉远端的横锁螺钉传递至股骨干上。同时,主钉受股骨干的牵拉和挤压影响很小,从而减少了由于主钉弯曲所引起的应力和应变。LCP DHS Blade为髓外固定,力臂较长,因而应力集中在螺旋刀片纤细的杆部和LCP最远端螺钉基底部,由于LCP DHS Blade的张力带作用,使螺钉基底部受到较大的剪切应力及向外侧的拉应力,可能出现内固定失效。
综上所述,相对于LCP DHS Blade,采用PFNAⅡ固定稳定型的股骨转子间骨折(AO 31⁃A1)仍具有一定的生物力学优势。股骨转子间骨折后,如何重建股骨近端的力学稳定性是治疗的核心问题。KAUFER等[13]提出,股骨转子间骨折内固定术后稳定性取决于以下5个因素:骨质量、骨折类型、复位程度、植入物类型、植入物在骨中位置。本研究假定在相同骨质量、稳定型骨折类型、复位良好、植入物位置良好的情况下,将不同类型的植入物作为主要观察指标,在新型计算机软件辅助下进行仿真有限元分析,为术后早期康复提供了较为确切的生物力学依据。下一步将对影响转子间骨折稳定型的其他因素进行研究和评价。

