葛根素对脑缺血再灌注大鼠神经功能与大脑皮质突触形态结构及参数的影响*
李晓伟, 王 跃, 韩 硕, 孙永奇, 李玲玲, 刘 壮, 张晓晟, 刘 月, 赵淑敏, 纪海茹
(承德医学院, 河北 承德 067000)
突触作为神经元与其它细胞传递信息的特殊结构,对维持大脑神经的正常功能具有重要作用。脑缺血会导致神经元脱失、变性及结构和功能的改变,进而改变突触的形态与结构,影响神经信息传递和神经功能恢复[1-3]。治疗由缺血引起的脑卒中时可以通过修复突触,提高突触可塑性,进而促进神经功能恢复。葛根素(puerarin,Pue)有抗衰老、抗炎、改善微循环、保护神经细胞及改善学习记忆等作用,在心脑血管疾病的治疗中取得了良好的疗效[4-5],但目前关于葛根素对缺血再灌注(ischemia-reperfusion,IR)大鼠神经功能与大脑皮质突触形态结构及参数影响的报道较少。本实验通过观察葛根素干预后脑缺血再灌注大鼠大脑皮质突触形态结构及参数的变化,探讨其对神经损伤的作用及机制。
材 料 和 方 法
1 材料
1.1动物 69只雄性SD大鼠购自北京维通利华实验动物技术有限公司,体质量260~280 g,许可证号为SCXK(京)2016-0001。
1.2药品及仪器 葛根素注射剂(2 mL:0.1 g;国药准字H20034082)购自哈尔滨松鹤制药有限公司;尼莫地平(nimodipine,NIM)注射剂购自拜尔医药保健有限公司。透射电镜(Hitachi,H-7650);超薄切片机(Leica,EMUC6)。
2 方法
2.1分组与造模 将69只SD大鼠随机分为假手术组(sham组)、模型组(IR组)、Pue组和尼莫地平阳性对照组(NIM组),假手术组15只,其余3组每组18只。大鼠参照线栓法制备右侧大脑中动脉局灶性缺血再灌注模型,假手术组仅分离血管,不插入线栓。缺血2 h后,再灌注24 h。大鼠清醒后,参照Longa 5级4分制评分标准[6]进行神经功能缺损评分,剔除造模评分0分及4分和不符合实验标准的大鼠,并及时补遗。术后大鼠单笼饲养,给予8×104U青霉素腹腔注射抗感染。
2.2给药 Pue组和NIM组大鼠于脑缺血再灌注后分别立即腹腔内注射Pue (8 mg·kg-1·d-1)和NIM (1 mg·kg-1·d-1);sham组及IR组相同时点给予等体积的生理盐水,直至相应时点。
2.3神经功能缺损评分 术后第3、7和14天采取改良的神经功能缺损评分(modified neurological severity score,mNSS)评价大鼠神经功能缺损状况。mNSS主要包括提尾反射、行走测试、感觉测试、平衡测试、反射缺失和反常运动,各项目总和记为最终评分:1~6分为轻度损伤,7~12分为中度损伤,13~18分为严重损伤[7-8]。
2.4电镜检测突触超微结构的变化 各实验组大鼠腹腔内麻醉后,经左心室灌注4%多聚甲醛和2%戊二醛混合固定液固定。取缺血区大脑皮质,常规电镜样品制备,H-7650透射电镜观察并采集照片。电镜下图片放大5万倍,每只大鼠取不同部位10张,采用Quantiment-520 图像分析仪测量突触活性区长度、突触间隙宽度、突触后膜弦长和弧长及突触后致密物(postsynaptic density,PSD)厚度。测量活性区长度与PSD厚度参考Guldner法,计算突触界面曲率参照Jones法,多点平均法测定突触间隙宽度,取其均数。
3 统计学处理
用SPSS 17.0软件进行统计学分析。实验数据以均数±标准差(mean±SD)表示,析因设计的方差分析检验突触形态结构参数,两组间比较采用q检验,以P<0.05为差异有统计学意义。
结 果
1 神经功能缺损评分
与IR组相比,用药组各时点神经功能缺损评分均降低(P<0.05),Pue组和NIM组2组间评分的差异无统计学显著性。用药3、7和14 d后各组大鼠神经功能缺损评分逐次降低,且用药7 d和14 d时行为学评分明显优于3 d(P<0.05),但用药7 d与14 d的差异无统计学显著性,见表1。

表1 各组大鼠改良神经功能缺损评分的变化
*P<0.05,**P<0.01vssham group;△P<0.05vsIR group;#P<0.05vs3 d.
2 电镜检测突触超微结构变化
电镜下观察sham组突触数目较多,轮廓清晰,前后膜完整,突触前成分内突触囊泡呈均等、密集的圆形清亮小泡,突触后致密带较宽、高密度,厚度均匀,突触间隙清晰;IR组各时点较相应时点sham组突触数目明显减少,前后膜及间隙模糊,突触囊泡数目显著减少、密度不均,突触后细胞终末胞质严重破坏,呈空泡变性,突触后致密带密度降低,突触界面曲率明显减小;Pue组和NIM组各时点较IR组突触密集,突触形态接近sham组,突触囊泡数量较IR组增多,凹形突触增加,常见两个活性点,突触后细胞终末胞质变性溶解显著减轻,致密物增厚,间隙减小,突触界面曲率增加。用药组各时点均呈逐渐好转趋势,且7 d和14 d明显优于3 d,但用药7 d与14 d无明显差异,见图1。
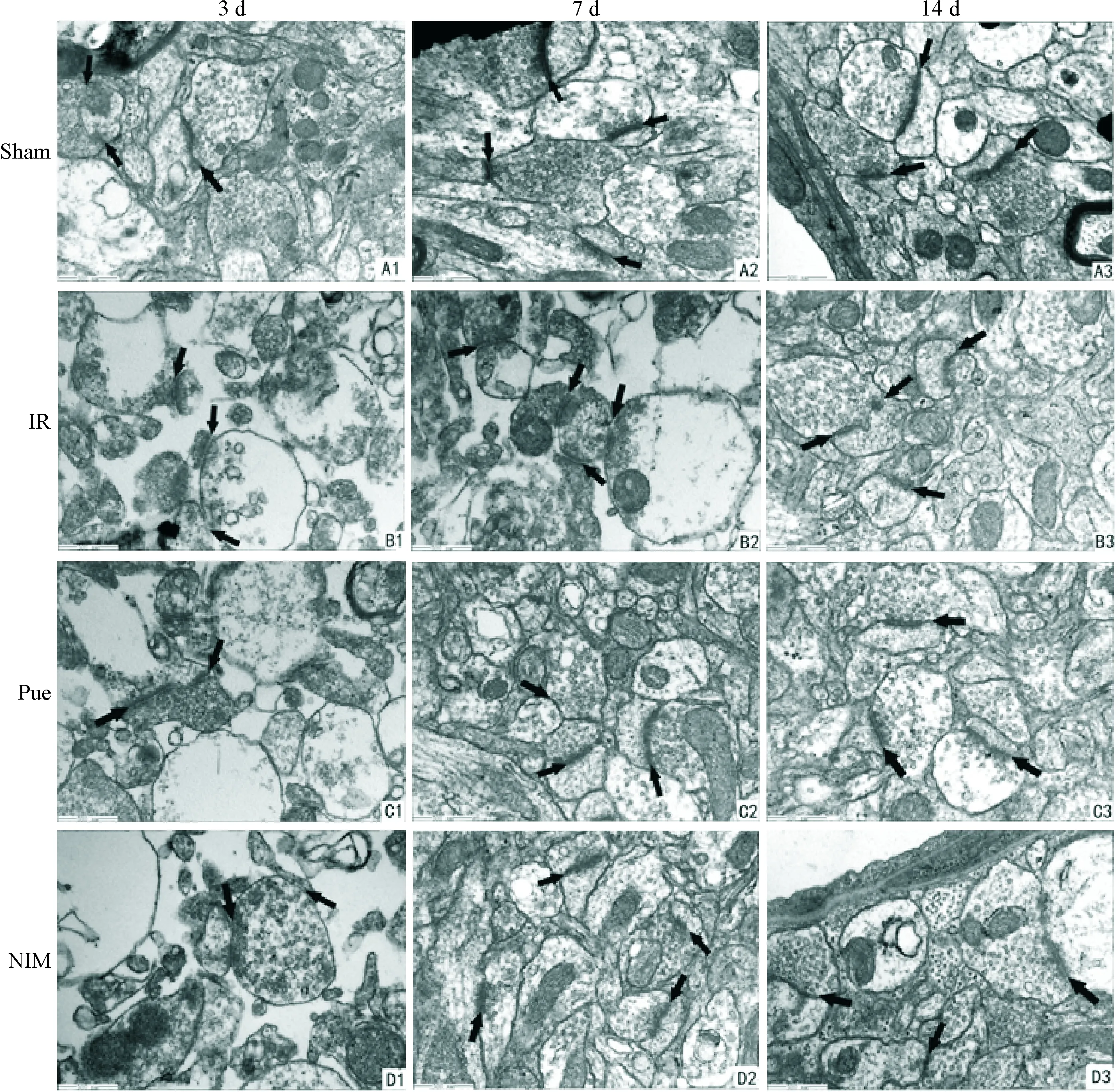
Figure 1. The ultrastructural alterations in cerebral cortex of rats in each group at different time points (×50 000, bar=500 nm).
IR组各时点突触界面曲率均呈下降趋势,与sham组比较差异有统计学意义(P<0.05);与IR组相比,用药组各时点突触界面曲率均明显增加(P<0.05),但Pue组和NIM组突触界面曲率的差异无统计学显著性。用药组各时点突触界面曲率逐渐增加;用药7 d和14 d明显大于3 d(P<0.05);且用药7 d与14 d的差异无统计学显著性,见表2。
IR组各时点PSD厚度均呈下降趋势,与sham组比较差异有统计学意义(P<0.05);与IR组相比,用药组各时点PSD厚度均明显增加(P<0.05),Pue组和NIM组PSD厚度的差异无统计学显著性。用药组各时点PSD厚度逐渐增加;用药7 d和14 d,PSD的厚度明显大于3 d(P<0.05);且用药7 d与14 d的差异无统计学显著性,见表3。

表2 各组大鼠大脑皮质突触界面曲率变化的比较
*P<0.05vssham group;△P<0.05vsIR group;#P<0.05vs3 d.

表3 各组大鼠大脑皮质PSD厚度变化的比较
*P<0.05,**P<0.01vssham group;△P<0.05vsIR group;#P<0.05vs3 d.
IR组各时点突触间隙均呈上升趋势,与sham组比较差异有统计学意义(P<0.05);与IR组相比,用药组各时点突触间隙宽度均明显下降(P<0.05),Pue组和NIM组突触间隙宽度的差异无统计学显著性。用药组各时点突触间隙宽度逐渐下降;用药7 d和14 d,突触间隙宽度明显大于3 d(P<0.05);且用药7 d与14 d的差异无统计学显著性,见表4。

表4 各组大鼠大脑皮质突触间隙宽度变化的比较
*P<0.05,**P<0.01vssham group;△P<0.05vsIR group;#P<0.05vs3 d.
讨 论
随着世界老龄化进程的加快,缺血性脑卒中发病率越来越高,日益成为致死致残主要因素[9],常伴发不同程度的感觉、运动和认知等功能障碍,其高致残和致死率严重影响人民的生活[10-11]。葛根素对缺血性脑损伤的恢复起着积极的作用,对于抑制神经元损伤,减轻神经功能缺损也有一定作用[12]。突触是神经元与其它神经元或效应细胞之间相互接触并借以传导冲动的结构,是信息传递的结构基础。突触结构的数量与完整对保证神经元获得、加工、贮存及传递信息起着至关重要的作用[13]。突触具有较大的可塑性,在环境变化或受损时,其结构与功能会发生相应变化,从而改善学习记忆与肢体运动能力[14]。
突触可塑性是神经功能重建的重要机制[15],在缺血后神经功能的恢复中起关键作用[10]。缺血性脑损伤发生后,脑实质缺血所引起的坏死及再灌注后所引起的凋亡常可引发感觉、运动障碍等一系列神经功能缺损,因此临床上常通过神经功能缺损评分对神经受损情况进行有效评价。动物行为学实验不仅可以评价缺血性脑损伤后残存神经功能,而且可以用来评估治疗手段对神经功能的保护效果[16]。在本课题的mNSS检测中,发现脑缺血再灌注大鼠均迅速呈现明显的运动障碍,用药后运动障碍均有好转,但未回归正常运动,用药7 d、14 d较3 d行为学评分有明显降低,用药7 d与14 d的差异无统计学显著性,表明葛根素明显改善了脑缺血再灌注后的神经功能。
突触界面曲率的转变是突触可塑性的潜在特征,曲型突触比直型突触拥有更多可产生能量的线粒体,可提供更多的能量,使突触处于兴奋状态。曲型突触较直型突触更能扩大接触面积[8],同时限制释放的神经递质扩散,保证更多的神经递质到达突触后膜,有利于神经递质与后膜受体更充分的结合及神经递质作用受体后被重新摄取,从而提升信息传导的有效性与迅速性,由此推断突触界面曲率增大可能是一种代偿作用。本研究用电镜观测Pue和NIM组的突触界面曲率明显大于IR组,用药7 d、14 d较3 d的突触界面曲率有明显增大,但用药7 d与14 d的差异无统计学意义,说明应用葛根素7 d可促进突触功能代偿。
PSD是突触后膜的一层均质致密物,由突触后膜分化物组成。PSD 厚度与突触机能变化密切相关,是反映突触可塑性的形态学参数[17]。PSD 含有多种酶与蛋白质, 在酶的催化下蛋白质分子构象的可逆性改变能引起其亚微结构的转变(厚度增大或减小)。PSD形态变化可能与突触后膜上受体及离子通道的变化密切相关,PSD 增厚和增长可能是突触功效增强的物质基础[8]。本研究显示与IR组相比,Pue和NIM组脑缺血侧皮质PSD厚度显著增加。用药7 d、14 d较3 d时PSD厚度明显增加,用药7 d与14 d的差异无统计学显著性,证明葛根素可增强突触功效。
突触间隙宽度可改变神经递质的有效率。间隙宽度减小,可减少神经递质的扩散,增高利用度,实验中,Pue、NIM组脑缺血皮质区较IR组均变窄,与IR组比较差异有统计学意义,用药7 d、14 d较3 d行为学评分明显降低,用药7 d与14 d的差异无统计学显著性。
本实验通过Pue与现阶段临床用药尼莫地平的比较,证实Pue与NIM所达到的治疗效果相似,均能有效修复脑缺血再灌注大鼠大脑皮质突触结构,提高突触可塑性,改善大鼠神经功能,且其价格低廉,具有明显的经济优势,预测葛根素有可能成为新型治疗临床缺血性脑卒中的药物。

