CLAG方案和FLAG方案治疗难治或复发性急性髓系白血病对比观察
罗文丰,余惠兰,邹兴立,倪勋,魏锦
(川北医学院附属医院,四川南充637000)
随着分子遗传学的发展,对于急性髓系白血病(AML)[1,2]病理有了更好的认识,并且更多的个体化治疗方案被应用在AML患者的治疗中,然而仍有20%~40%的患者对诱导治疗不响应,且50%~70%的患者在获得完全缓解(CR)后出现复发,这些情况被定义为难治或复发AML(R/R AML)[3,4]。R/R AML患者中广泛使用的治疗方案是以阿糖胞苷(Ara-C)为基础,联合使用其他化疗药物和细胞因子。大量研究表明,作为一种能够抑制核糖核苷酸还原酶的细胞毒性药物,嘌呤类似物在R/R AML的治疗发挥了重要作用[5, 6]。其中,氟达拉滨的应用较早,常与Ara-C和粒细胞集落刺激因子(G-CSF)联合使用(FLAG方案)治疗R/R AML[6,7],CR率为46%~63%[8]。克拉屈滨为新一代嘌呤类似物,被认为可以替代氟达拉滨,可与Ara-C和G-CSF合用(CLAG方案)治疗R/R AML[9,10]。据波兰成人白血病工作组(PALG)的一项多中心研究报道,CLAG方案在R/R AML患者中获得的CR率为50%,1年总体生存率为42%[11]。尽管CLAG或FLAG方案在R/R AML患者中均有良好的有效性,但直接对比这两种治疗方法疗效的研究并不多见。本研究旨在比较CLAG和FLAG两种不同治疗方案在R/R AML患者中的疗效及预后,并且分析影响其疗效及预后的因素。
1 资料与方法
1.1 临床资料 本研究为前瞻性队列研究,连续纳入73例2013年3月~2016年6月在川北医学院附属医院血液内科将接受CLAG或FLAG方案治疗的R/R AML患者。难治性AML定义:标准方案诱导化疗2个疗程未获得CR;首次诱导获得CR后在6个月内复发;首次获得CR后的6个月后复发,经原方案再诱导化疗失败;2次或2次以上复发者;髓外白血病持续存在。复发性AML定义:CR后外周血重新出现白血病细胞或骨髓原始细胞>10%。入选标准:根据形态学、免疫学、细胞遗传学和分子生物学确诊为AML;属于R/R AML;骨髓原始细胞>10%;将要进行嘌呤类似物为基础的诱导治疗(CLAG或FLAG方案);能够定期接受随访。排除标准:既往使用过含嘌呤类似物的诱导治疗(如果多次接受过以嘌呤类似物为基础诱导治疗的患者,只纳入第一次治疗信息,避免患者重复纳入);严重心脏功能不全,心律失常,肺功能不全,肝功能不全或肾功能不全;有实体肿瘤病史;已知对于CLAG或者FLAG方案中相关药物过敏或药物抵抗;妊娠、准备妊娠或哺乳期女性。收集记录患者的综合基线期信息,具体包括:人口统计学信息(年龄、性别);临床病理信息[疾病情况、原发或继发疾病、危险度分级(根据NCCN指南列举的细胞遗传学和分子异常进行判定)、ECOG评分、骨髓原始细胞、首次诱导CR、既往异基因造血干细胞移植(allo-HSCT)和挽救治疗次数]。队列研究不干预患者的治疗,所有患者经过入选排除标准筛选入组研究后,根据其疾病情况和意愿接受CLAG或者FLAG方案治疗。CLAG方案治疗27例,男12例、女15例,年龄(50.19±20.74)岁,复发AML 17例、难治AML 10例,原发AML 21例、继发AML 6例,危险度分级:低危、中危、高危和未知分别为1、16、9和1例,ECOG评分为0、1、2分分别有9、17、1例,骨髓原始细胞比例中位值为38.8%(24.0%,65.8%),首次诱导获得CR为15例,既往接受过allo-HSCT为5例,一线挽救治疗20例、二线或更高挽救治疗7例。FLAG方案治疗46例,男24例、女22例,年龄(47.87±17.82)岁,复发AML 28例、难治AML 18例,原发AML 36例、继发AML 10例,危险度分级:低危、中危、高危和未知分别为8、23、14和1例,ECOG评分为0、1、2分分别为12、29、5例,骨髓原始细胞比例为43.2%(28.1%,63.0%),首次诱导获得CR为17例,既往接受过allo-HSCT为10例,一线挽救治疗37例、二线或更高挽救治疗9例。两者上述资料比较差异均无统计学意义。本研究经川北医学院附属医院伦理委员会批准,所有患者签署知情同意书。
1.2 治疗方法 CLAG方案为5 mg/(m2·d)克拉屈滨,静脉滴注,第1~5天;2 g/(m2·d)阿糖胞苷,静脉滴注,第1~5天;300 μg/d非格司亭,静脉滴注,第0~5天;联合或不联合10 mg/(m2·d)米托蒽醌3天治疗。FLAG方案为30 mg/(m2·d)氟达拉滨,静脉滴注,第1~5天;2 g/(m2·d)阿糖胞苷,静脉滴注,第1~5天;非格司亭,静脉滴注,第0~5天;联合或不联合10 mg/(m2·d)去甲柔红霉素3天治疗。
1.3 随访和疗效评估 中位随访时间为10.0个月,随访截至时间为2017年2月。记录接受两方案治疗患者CR例数,并计算总有效率(ORR),记录接受allo-HSCT患者例数。比较CLAG与FLAG治疗不同基线期特征患者CR。CR定义为治疗后骨髓原始细胞低于5%,处于稳定状态,并且无白血病细胞浸润、无额外输注需求,白细胞数目大于1×109/L,血小板数目大于100×109/L。部分缓解(PR)定义为骨髓原始细胞在5%~25%,或者骨髓原始细胞百分比有50%以上的下降,或者原始细胞<5%但可见Auer小体。ORR定义为实现CR或PR的合计患者比例。
1.4 预后判断 比较接受两方案治疗患者总生存期(OS),比较CLAG与FLAG治疗不同基线期特征患者OS。OS定义为从治疗起到由于任何原因死亡的生存时间。
2 结果
2.1 两种治疗方案疗效比较 本研究纳入的73例患者中共有62例进行了治疗应答评估,其中CLAG方案治疗23例、FLAG方案治疗39例,其余患者由于个人原因未接受评估。其中CLAG方案治疗和FLAG方案治疗患者分别有11、15例达CR,15、21例达ORR,两者比较P分别为0.470、0.381。CLAG、FLAG方案治疗患者中接受allo-HSCT分别为5、6例,两者相比P=0.528。
2.2 两种治疗方案OS比较 K-M曲线结果显示,CLAG、FLAG治疗患者中位OS分别为10.0(95%CI:3.4~16.6)、9.0(95%CI:6.6~11.4)个月,两者OS比较P=0.151。
2.3 两种治疗方案不同基线特征CR、OS比较 两种方案治疗在不同基线期特征患者中的CR率均无统计学差异(表1)。在复发AML患者中,接受CLAG治疗的患者相比于接受FLAG治疗的患者获得了更长的OS(P=0.049);对于危险度分级为高危(P=0.053)、首次诱导获得CR(P=0.063)和既往接受过allo-HSCT(P=0.063)的患者,接受CLAG治疗相对于接受FLAG治疗有更好OS的趋势,但无统计学差异;其他不同基线特征两种方案治疗患者OS比较差异无统计学意义。
3 讨论
CLAG和FLAG方案主要联合了Ara-C、G-CSF和嘌呤类似物药物。其中Ara-C经磷酸化可以形成有活性的代谢产物Ara-CTP,它是一种DNA聚合酶的抑制因子,可结合在DNA上从而终止DNA链的延长来引起细胞凋亡[12]。G-CSF是在血液疾病中常用的细胞因子,在R/R AML患者的治疗过程中,G-CSF可动员造血祖细胞,从而促进骨髓细胞的分化[13]。
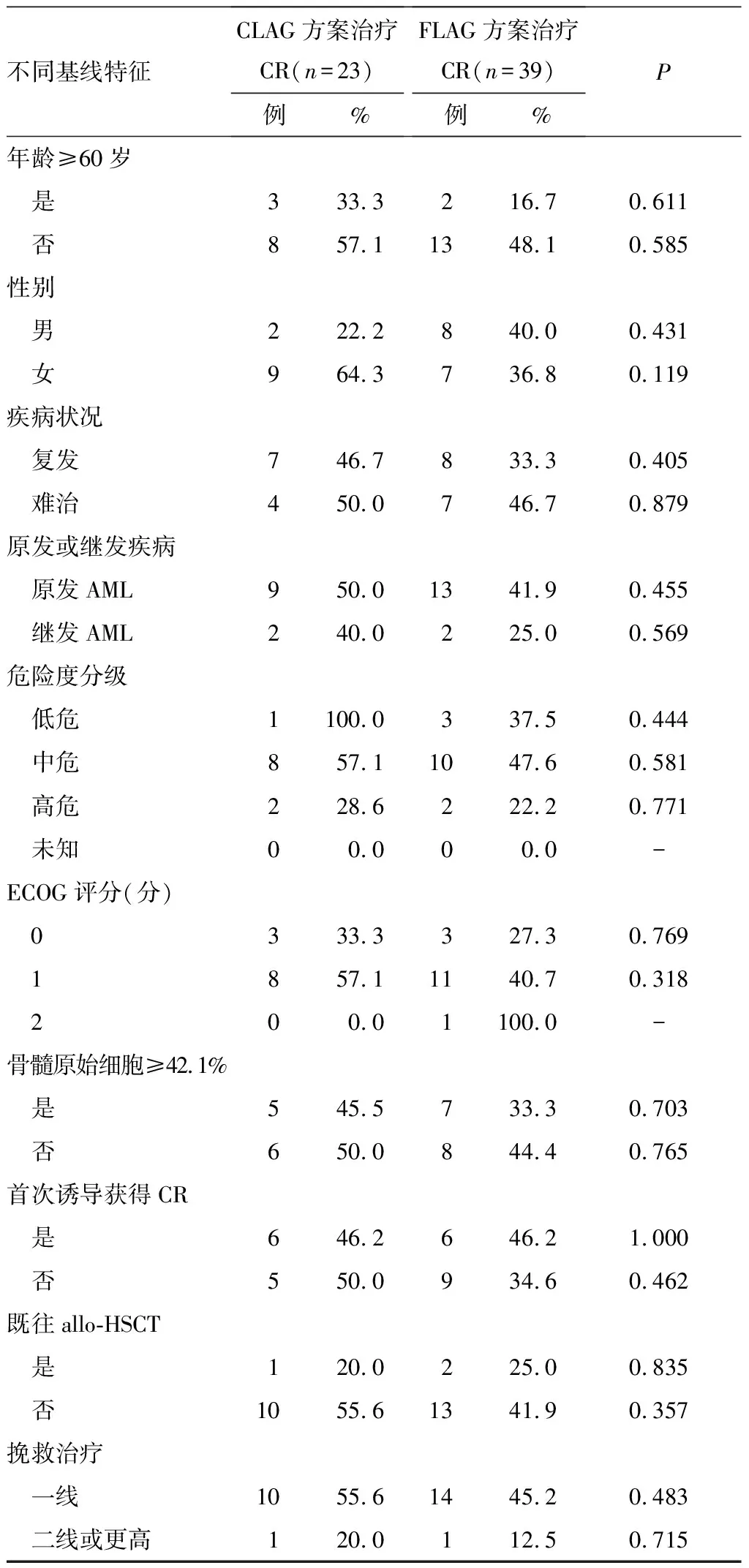
表1 CLAG与FLAG方案治疗不同基线特征CR比较
嘌呤类似物能够促进细胞对Ara-CTP的摄取及其在细胞内的累积,从而进一步提高对癌细胞的杀伤作用。除了共同的联合药物,CLAG和FLAG方案中的氟达拉滨和克拉屈滨对造血系统均发挥了重要作用。氟达拉滨可通过抑制核糖核苷酸还原酶进而影响细胞的增殖。克拉屈滨除了具有和氟达拉滨相似的作用机制外,还可通过改变线粒体的膜电位来诱导细胞色素C和凋亡诱导因子进入细胞质,从而促进细胞凋亡[14,15]。因此,使用克拉屈滨的CLAG方案日益受到关注。
近年来,已经有一些研究比较嘌呤类似物为主的化疗方案与其他药物化疗方案对于R/R AML患者的疗效。例如,一项回顾性研究对比了CLAG和一种由Ara-C、米托蒽醌和依托泊苷组成的化疗方法(MEC)治疗R/R AML患者的疗效,结果显示CLAG治疗组的患者相对于MEC治疗组的患者获得了更高的CR率[16]。另一项研究对比了由阿糖胞苷、阿克拉霉素和G-CSF组成的方案(CAG)与减低剂量的FLAG方案对61例R/R AML患者的疗效,结果显示接受减低剂量FLAG方案治疗的患者有较高CR率[17]。一项回顾性研究对比了以克拉屈滨为主的化疗方案和以氟达拉滨为主的化疗方案在R/R AML患者中的疗效,发现克拉屈滨治疗组得到CR率为62.7%,氟达拉滨组获得CR率为61.4%,其两组方法的疗效无显著差异[18]。上述研究的结果说明,在R/R AML患者中CLAG和FLAG取得了相似的疗效。与这一研究结果趋势一致,本研究发现对于R/R AML患者,CLAG方案治疗与FLAG方案治疗获得CR和ORR例数比较无显著差异。
此外,我们还研究了R/R AML患者在CLAG或FLAG方案治疗后生存期的对比,结果显示,接受这两种治疗的患者在OS上无统计学差异,与其他研究结果的趋势一致[18]。从这些结果来看,尽管克拉屈滨和氟达拉滨的作用特点略有不同,但影响患者OS的主要因素可能是CLAG和FLAG方案的共同联合药物以及嘌呤类似物的共同作用机制。嘌呤类似物与Ara-C的协同作用大大增强了细胞毒性,从而提高了抗白血病效应[19];G-CSF通过促进骨髓细胞的分化,改善了造血系统的活力,因此从长期来看,造血功能逐渐得到良好的恢复[13]。
据报道,CLAG方案在首次诱导获得CR、原发AML和危险度分级非高危的复发性的AML患者中获得了更好的OS,然而在继发AML患者中FLAG治疗后的OS更长[18]。我们的研究也进一步进行了CLAG和FLAG两种方案治疗在不同基线期特征中疗效的比较,发现在复发AML的患者中,经CLAG方案治疗的患者获得了更久的OS,危险度分级为高危、首次诱导CR和既往接受过allo-HSCT的患者,CLAG方案治疗后患者表现出更好的OS的趋势,这可能的原因是这几类患者可能存在更严重的耐药情况,而克拉屈滨有更强的促进细胞凋亡的作用,因此在这些患者中CLAG较FLAG方案治疗更有优势。我们得出的结果与上述报道结果不完全一致,可能的原因有:纳入患者的年龄不同,本研究患者平均年龄小于上述研究中的患者;治疗方法不全相同,我们的研究主要采用了CLAG方案和FLAG方案,而在Park等[18]的研究中,克拉屈滨治疗组包含了CLAG(n=31)、CLAG结合米托蒽醌(CLAG-M,n=34),且年长患者使用了修正的CLAG方案(mCLAG,n=13),这些治疗方案上的差异也可能导致了亚组分析结果的不同。
本研究仍有一些不足:本研究仅纳入R/R AML 患者73例,样本量相对较小,因此统计效能较低;随访时间较短(中位值为9个月),因此患者经CLAG和FLAG两种方案治疗后的长期疗效未能评估,然而R/R AML患者生存期本来就短且容易失访,因此如何提高患者的随访规范性是之后研究的重点;本研究为单中心队列研究,可能存在多种偏倚和混杂因素,从而影响研究结果,故需要大规模的、多中心的随机对照试验来进一步评估CLAG和FLAG方案在R/R AML患者中的疗效差异。
综上所述,CLAG和FLAG方案治疗R/R AML患者有相似的疗效,但对于复发AML、高危危险度分级、首次诱导治疗获得CR和既往接受过allo-HSCT的患者,CLAG方案可能是更优的选择。

