腹部平滑肌肉瘤的MSCT表现与病理比照
朱晓红 吴礼明 刘 斌 余永强
腹部平滑肌肉瘤发病率低,腹部含平滑肌脏器及组织均可发生。本病患者出现症状常较晚,发现时肿瘤体积常较大,关于原发性平滑肌肉瘤的报道较少,本文回顾性分析过去5年经手术证实的平滑肌肉瘤患者的病例资料,结合病理分析其CT征象,以期提高对该病的认识。
1 资料及方法
1.1 一般资料 回顾性分析2013年10月至2018年2月安徽医科大学第一附属医院手术并经病理证实的腹部平滑肌肉瘤10例患者临床资料,其中男性5例,女性5例,年龄28~77岁,平均(51.9±14.0)岁。临床主要症状:5例患者无意中发现腹部肿块,其中2例近期感觉有增大;3例患者自述腹部不适、腹痛;2例患者出现血尿。
1.2 仪器与方法 10例患者术前均行三期动态增强扫描,仪器GE lightspeed 64排CT或GE discovery宝石能谱CT。扫描层厚5 mm,层间距5 mm,120 kV,250 mA,CT增强扫描采用肘前静脉内团注非离子型对比剂,对比剂剂量为1.0~1.5 mL/kg,流率2.5~3.5 mL/s。由2名有10年以上工作经验的高年资医生对影像表现(包括大小、形态、密度、增强程度及坏死程度)进行分析,并结合术后病理与CT图像对照分析。
1.3 病理学检查 10例患者均接受手术治疗,术后标本经10%中性福尔马林固定,石蜡包埋,4 μm厚连续切片,进行常规HE染色及免疫组化染色检查。免疫组化主要观察平滑肌肌动蛋白(smooth muscle actin,SMA),肌源性特异标志物结合蛋白(desmin,Des),核增殖抗原表达基因Ki-67、CD34、CD117等。
2 结果
2.1 CT表现 10例腹部平滑肌肉瘤患者中,5例位于腹膜后,其中2例位于左侧腹膜后, 3例位于右侧腹膜后(见图1);2例位于胰周;1例位于脾门;还有2例为左肾占位(见图2)。4例呈分叶状,6例呈类圆形。肿瘤最大径3~23 cm,平均(11.6±6.4)cm。8例与周围结构分界不清,2例边缘清晰。仅1例平扫密度均匀,增强扫描呈轻度较均匀强化,坏死囊变不明显(见图3);另9例平扫密度不均,增强扫描可见不同程度的坏死囊变区(见图1、2);10例病灶平扫时CT值为(41.8±14.6)Hu,动脉期CT值为(64.4±21.0)Hu,门脉期CT均为(80.5±27.4)Hu,延迟期CT值为(84.0±23.8)Hu,实性部分呈持续强化;动脉期强化程度不等,4例动脉期呈轻度强化,6例动脉期强化较明显,较大病灶可见线状强化的滋养动脉(见图1)。1例病灶同时发生肝脏转移。
2.2 病理表现 镜下肿瘤细胞多呈梭形,有不同程度的核分裂像,免疫组化SMA均为阳性,9例DES(+,或部分+),1例DES(-),Ki-67阳性率5%~70%,7例CD34(-),3例CD34部分(+),9例CD117(-),1例CD117少数细胞(+)。
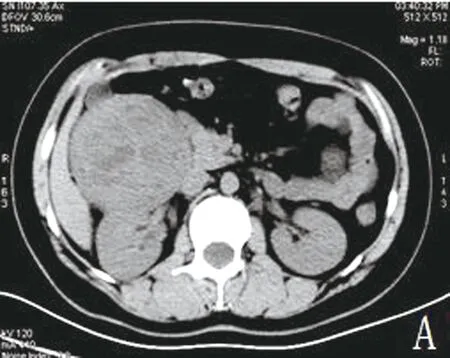
图1 右侧腹膜后平滑肌肉瘤
注:A为平扫病灶密度不均,可见低密度坏死;B为动脉期病灶明显不均匀强化,其内可见线状强化血管

注:A为平扫示左肾见分叶状巨大肿块,其内密度不均;B为增强扫描,病灶呈不均匀强化,坏死区未见明显强化

注:A为平扫呈等密度,病灶边缘清晰,与下腔静脉关系密切;B为动脉期病灶呈轻度强化
3 讨论
平滑肌肉瘤是一种梭形细胞恶性肿瘤,具有平滑肌分化倾向,多见于子宫及消化系统肠壁的平滑肌层,也可来源于任何含有平滑肌的组织,包括腹膜后、肠系膜及大网膜,发病率低,病因不明[1]。2例发生于肾脏,可能来源于肾被膜、肾盂、肾盏及肾血管平滑肌组织[2];2例位于左侧腹膜后,病灶与该侧肾上腺分界不清,可能来源于腹膜后间隙血管壁上的平滑肌细胞;3例位于腹腔,来源于肠系膜可能性大。发生于腹膜后的平滑肌肉瘤,当肿瘤较小时,可埋藏在腹膜后间隙中隐匿生长,患者常无明显的临床症状及体征,肿瘤较大时,腹痛及腹部包块常常是最早出现的症状及体征。7例发生于腹膜后的患者中有4例瘤体直径>10 cm。手术切除是平滑肌肉瘤的主要治疗方法,但由于病灶较大且与临近组织关系密切,病灶很难切除干净,术后容易复发,术前应尽可能通过多种影像方法显示肿瘤边界、与周围脏器及血管的关系,尽可能做到根治性切除。
原发性平滑肌肉瘤好发于中老年,文献[3]报道女性更多,呈分叶状或类圆形,少数形态欠规则,组织病理学特征表现为梭形细胞呈束状排列构成,可见核分裂像,肿块呈浸润性生长,易累积周围组织及血管。免疫组化通常表现为Des(+)、SMA(+),而CD34(-),CD117(-),本组病例病理结果与其一致,同时Ki-67阳性率5%~70%。来源于子宫平滑肌肉瘤免疫组化标记物亦为Des(+)、SMA(+),Ki-67表达量为10%~40%[4]。有研究[5]表明,Ki-67的增殖指数越高,其危险度越高,可做为判断肿瘤危险度的辅助指标之一,本组病例中随着Ki-67阳性率的增加,平滑肌肉瘤的危险度亦呈上升趋势,但因病例数太少,两者之间的相关性还需大样本量的研究。也有研究[6]认为,肿瘤内的坏死囊变是平滑肌肉瘤发生转移的重要预测因素,坏死面积越大,恶性程度越高。本组10例病灶中有1例病灶坏死不明显,该病例为高分化平滑肌肉瘤,另9例病灶均有不同程度的坏死囊变。
腹部平滑肌肉瘤动态增强扫描根据肿瘤的供血程度不同,其强化程度不同,本组4例病灶动脉期呈轻度强化,另6例动脉期强化较明显,实性部分均呈持续强化,可能与肿瘤内富含纤维组织及肿瘤细胞多且体积大,细胞间隙宽大有关。Kim等[7]认为多数腹膜后平滑肌肉瘤为富血供肿瘤,少数平滑肌肉瘤强化显著,类似血管瘤。本组病例CT强化差异较大,轻度强化至明显强化均可见,但比较其CT均值,肿瘤实性部分呈延迟强化表现。
腹部平滑肌肉瘤瘤体较大,常为偏实性的软组织肿块,大片状或小灶状坏死均常见,肿瘤实性部分轻度至明显强化均可见,但动态三期呈渐进性延迟强化表现。根据肿瘤的发病部位不同需要与不同的肿瘤鉴别。发生于腹膜后、腹盆腔及腹股沟的平滑肌肉瘤需要与脂肪肉瘤、恶性纤维组织细胞瘤、淋巴瘤、神经鞘瘤、横纹肌肉瘤等鉴别。脂肪肉瘤一般瘤体内可以看到脂肪组织;恶性纤维组织细胞瘤老年患者多见,肿瘤边缘不清,瘤内常见坏死、出血及钙化是其特征性表现[8];横纹肌肉瘤发病年龄较小;恶性神经源性肿瘤一般位于脊柱旁或腰大肌前方,沿神经走行方向生长,表现为上下径大于前后径的特点[9],有报道认为平滑肌肉瘤瘤体常前后径大于上下径[10],但还需要大样本量验证;淋巴瘤内血管漂浮多为腹膜后正常解剖血管,再结合其他部位的淋巴结肿大有助于诊断。发生于肾脏的平滑肌肉瘤主要与肾癌、肾盂癌、肾母细胞瘤、肾平滑肌瘤等鉴别,动态增强渐进性延迟强化对其诊断有一定帮助。发生于腹腔的平滑肌肉瘤需要与来源于胃肠道的间质瘤相鉴别,间质瘤的强化程度比平滑肌肉瘤更明显,但确诊还是有赖于手术病理及免疫组化。

