宫颈癌三维后装治疗中两种优化方式的剂量及相关性分析
周解平,吴爱东,钱立庭,盛六四,徐 榭
高剂量率192Ir腔内后装治疗联合外照射是宫颈癌根治性放疗的标准方案。随着计算机、影像及放疗技术的发展,CT/MR等影像引导下的三维腔内后装治疗逐渐在临床上应用,其计划的优化方式主要有正向手动优化(manual optimization, MO)和基于模拟退火逆向优化(inversely optimization simulation anneal, IPSA)等[1]。该研究回顾性分析放疗科30例宫颈癌患者的MO治疗计划,基于原图像信息重新设计IPSA计划,比较两种优化方法的靶区和危及器官(organs at risk, OARs)的剂量分布差异。目前国内多数放疗中心仍采用基于A点的点剂量评估模式,该研究标记出ICRU38号报道推荐的A点和膀胱、直肠参考点,对A点剂量与高危CTV(high risk clinical target volume, HRCTV)的D90值、膀胱和直肠参考点剂量与OARs的D2 cm3剂量作相关性分析,为传统腔内治疗点剂量评估提供参考依据。
1 材料与方法
1.1病例资料随机数字表法选取安徽省肿瘤医院2015年10月~2016年10月于放疗科接受外照射联合三维腔内后装治疗的30例患者,患者均签署后装治疗同意书,年龄45~72岁,中位年龄61岁,病理分析均为鳞状细胞癌。根据2009年FIGO分期[2],其中ⅠB期3例、ⅡA10例、ⅡB14例、ⅢA3例。体外照射总剂量为46 Gy/23次,单次2 Gy,在体外照射36~40 Gy后开始CT图像引导下的高剂量率192Ir三维腔内后装治疗,1次/周,连续6次。
1.2施源器插入及CT扫描患者治疗前均排空膀胱,外阴消毒后插入Foley导尿管,导尿管球囊内注入5.0 ml的空气,膀胱灌注0.6%泛影葡胺的生理盐水200 ml,直肠内置入带有铅丝的导尿管,阴道窥具暴露术野后插入宫腔联合阴道卵圆体施源器,阴道填塞纱布以推开膀胱和直肠。在Siemens Spirit CT模拟机下进行CT扫描,扫描范围从L3椎体至外阴口下缘2 cm,层厚5 mm,重建成3 mm传至后装治疗计划系统(Varian Brachy)。
1.3治疗计划设计根据患者治疗前妇检情况和GEC-ESTRO[3]推荐标准,在Varian Brachy计划系统上逐层勾画出HRCTV及OARs直肠、膀胱、乙状结肠和小肠。直肠的下界从齿状线开始,上界到直肠和乙状结肠交界处。重建并勾画施源器,标记出左右A点、膀胱及直肠参考点,膀胱参考点为膀胱中心与施源器连线过膀胱后表面一点,直肠参考点为阴道施源器与阴道后壁交点后5 mm。原计划采用MO优化方式,即基于A点给定处方剂量,然后分别在矢状面、冠状面和横断面三个层面上手动拖动等剂量曲线直至达到优化目标。基于原图像信息,重新设计IPSA计划,初始优化剂量限值如下:A点剂量5.5~6 Gy,90.0%的HRCTV受照剂量(D90)≥6 Gy,直肠D2 cm3(2 cm3体积受到的最小照射剂量,下同)≤4 Gy、乙状结肠和小肠D2 cm3剂量≤4 Gy、膀胱D2 cm3剂量≤5 Gy。参照3个断面的等剂量曲线分布以及DVH参数,根据每位患者的实际解剖结构,调整优化目标函数,直至达到理想剂量分布。
1.4剂量参数统计及相关性分析分别统计比较两种治疗计划的左右A点剂量、HRCTV的D90、D100和V100剂量体积参数及靶区的适形性指数(conformity index, CI);膀胱、直肠、乙状结肠和小肠的D2 cm3和D1 cm3的受照剂量;两种计划的治疗时间参数;统计并分析IPSA计划中A点剂量和HRCTV的D90,膀胱、直肠参考点剂量与OARs的D2 cm3的相关性;CI的计算公式如下[4]:
其中VHRCTV,REF是处方剂量线包括的靶区体积,VHRCTV是指靶区的总体积,VREF是指处方剂量线包括的总体积。
1.5统计学处理采用SPSS 16.0软件进行分析,利用配对样本t检验的方法比较两种治疗计划参数;用Pearson方法作相关性分析,P<0.05为差异有统计学意义。
2 结果
2.1HRCTV剂量及A点剂量原MO计划和IPSA计划的靶区HRCTV的剂量体积参数D90、D100、V100及CI比较差异无统计学意义(P>0.05);但IPSA计划左右A点剂量均高于MO治疗计划(P<0.05),见表1。
2.2OARs剂量比较两种治疗计划膀胱、直肠、乙状结肠、小肠的D2 cm3和D1 cm3剂量见表2。相对MO计划,IPSA计划膀胱和直肠的D2 cm3、D1 cm3剂量明显降低(P<0.05);乙状结肠的D2 cm3和D1 cm3剂量也略微降低,但差异无统计学意义(P>0.05);而小肠的D2 cm3和D1 cm3剂量两种治疗计划相近(P>0.05)。图1所示是1例ⅡB宫颈癌两种治疗计划不同OARs的剂量体积直方图(DVH图)比较,也显示类似的结果。
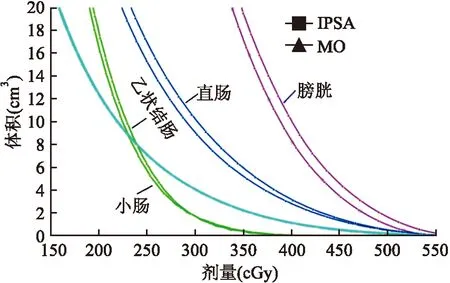
图1 1例ⅡB宫颈癌IPSA和MO治疗计划的OARs的DVH图比较
2.3IPSA计划相关性分析该研究中HRCTV体积为20.38~42.0 cm3,在此体积范围内,A点剂量与D90剂量呈正相关性(r=0.48,P=0.01),但D90值均稍大于A点剂量。IPSA计划膀胱参考点剂量为(2.75±0.54) Gy,约为其D2 cm3剂量的0.6倍;膀胱参考点剂量与小肠D2 cm3剂量呈正相关性(r=0.44,P=0.02);直肠参考点剂量与其D2 cm3剂量相近,与直肠、乙状结肠D2 cm3剂量均相关,但与乙状结肠相关性更大(r=0.42、0.62,P<0.05)。
2.4治疗时间IPSA和MO计划理论上所需的治
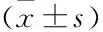
表1 IPSA和MO治疗计划靶区剂量参数比较
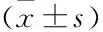
表2 直肠、乙状结肠、膀胱、小肠等OARs的剂量参数对比
疗时间分别为(324.27±44.65)s和(349.71±51.17)s,差异有统计学意义(t=-5.31,P<0.05),但两种治疗计划在具体病例驻留点的位置权重上,差别较大。图2所示为1例ⅡB宫颈癌的两种治疗计划的驻留位置和驻留时间的比较,IPSA计划驻留时间调节更精细,变化范围更广(0~30.1)s,而相应的MO治疗计划驻留时间变化相对较窄(9.4~21.5)s。
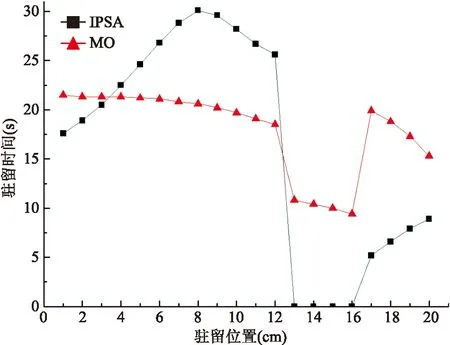
图2 1例ⅡB宫颈癌的IPSA和MO治疗计划的驻留位置和驻留时间的对比
3 讨论
基于CT/MR影像引导下的三维腔内后装治疗能清晰地显示肿瘤和OARs的大小、形状和位置关系,根据治疗计划的剂量体积直方图能精确地统计出靶区和OARs的剂量体积,可明显降低肠道和膀胱的并发症发生率[5-8]。目前三维后装治疗计划主要采用基于A点剂量的MO方式,但MO方式很大程度上依赖于物理师的经验和技巧,要得到临床满意的治疗计划常常耗费大量时间且治疗计划不可重复。逆向优化在外照射放疗中已广泛使用,实践证明其既提高靶区剂量的覆盖率、降低OARs照射剂量,又缩短了治疗计划优化时间且计划重复性好,但目前在后装治疗计划优化中使用较少。
该研究显示在HRCTV和OARs勾画不变的情况下,MO正向计划与IPSA逆向计划相比:HRCTV剂量体积参数D90、D100、V100和CI以及乙状结肠的剂量体积参数D2 cm3和D1 cm3差异均无统计学意义(P>0.05),但IPSA计划的乙状结肠D2 cm3和D1 cm3剂量略低;IPSA计划的膀胱、直肠的D2 cm3、D1 cm3照射剂量和照射时间分别降低了9%、8%、14%、11%和7.3%,差异有统计学意义(P<0.05)。Kannan et al[9]对基于CT的三维腔内后装治疗进行MO和IPSA计划对比研究表明IPSA计划可提高靶区HRCTV的V100和CI,而OARs剂量体积参数无显著性差异,与本研究结果相似,但可能该研究IPSA计划的目标函数限值更注重考虑靶区剂量。Hsu et al[10]对前列腺癌的三维插值后装治疗进行了IPSA研究,结果显示IPSA计划不仅提高了靶区HRCTV的覆盖指数V100和CI,而且降低了膀胱、直肠的D2 cm3剂量,与本研究结果略有不同,分析可能由于本研究中施源器仅为三管通道,其驻留位置和驻留时间调节有限,无法充分地发挥IPSA计划优势。因此,对宫颈癌肿瘤体积大、宫旁组织侵犯多的患者,采用腔内联合插值等通道较多的后装治疗时[11-12],可优化的空间较大,建议采用IPSA方式设计治疗计划。
基于曼彻斯特系统A点的二维后装治疗在临床上使用多年,积累了丰富的经验,但低估了膀胱、直肠等OARs的真实受量,结果易造成部分严重并发症的发生[13]。本研究开始于外照射36~40 Gy后,与外照射开始之初相比肿瘤HRCTV体积明显缩小,约为(20.38~42.0)cm3,在此体积范围内A点剂量与HRCTV的D90值呈正相关性,但D90值均略大于A点剂量,表明曼彻斯特系统确立A点处方剂量概念有一定的合理性,但略低估了肿瘤的实际受量。膀胱参考点剂量明显低于膀胱D2 cm3剂量,约为其0.6倍,据此利用膀胱参考点剂量可粗略地估算出传统二维腔内放疗膀胱的真实受量;膀胱参考点剂量与小肠D2 cm3剂量呈正相关性,提示可以通过控制膀胱体积来控制小肠最大受量;直肠参考点剂量与其D2 cm3剂量相近,直肠参考点剂量与直肠、乙状结肠D2 cm3均相关,但与乙状结肠相关性更大,可能与高剂量更容易落在乙状结肠而非直肠上有关,因此用直肠参考点剂量评估治疗计划可能会引起乙状结肠超量,导致肠道严重并发症的发生。

