恩替卡韦联合霉酚酸酯治疗乙型肝炎病毒相关性肾炎疗效研究
兰 静,曹彦丙
1.山西省运城市第二医院肝病五科 (运城 044000),2.山西省运城市第二医院肝胆外科(运城 044000)
主题词 肾炎 乙型肝炎病毒 @恩替卡韦 @霉酚酸酯
乙型肝炎病毒相关性肾炎(Hepatitis B virus-associated glomerulonephritis,HBV-GN)又称为乙肝相关性肾炎,是患者感染乙肝病毒后继发免疫复合物性肾小球疾病[1-2]。在我国,乙肝相关性肾炎的发病率大约为6.8%~20%,约占继发性肾炎病例总数的16.6%~32%。HBV-GN与在症状上与原发性肾病相似,而在病理类型中则存在多样化,疾病后期患者可出现肾功能衰竭,最终发展至终末期肾脏病(End-stage renal disease,ESRD),因此,通过临床治疗延缓HBV-GN的进展具有十分重要的意义。2014年1月至2016年12月我院收治的经肾脏活检,病理确诊为HBV-GN患者18例,给予恩替卡韦联合霉酚酸酯进行治疗,本文观察该组HBV-GN的近期疗效及安全性,探讨HBV-GN治疗的可行性方案。
对象与方法
1 研究对象 收集山西省运城市第二医院2014年1月至2016年12月在本科住院经肾脏活检,病理确诊为HBV-GN患者18例作为治疗组。其中男13例,女5例 ,年龄18~52岁,平均(28.12±3.14)岁;回顾我院2014年1月前收治的HBV-GN患者15例作为对照组,其中男11例,女4例 ,年龄19~55岁,平均(26.35±2.78)岁;临床诊断符合HBV-GN的诊断标准[3]:①血清中检测乙肝病毒抗原或抗体,提示阳性;②患有肾病或肾炎,但排除其他肾小球疾病;③病理检查提示肾小球中有HBV抗原沉积:常为HBsAg、HBcAg或HBeAg;④病理检查肾脏多为膜性肾炎,少数可表现为膜增生性肾炎和系膜增生性肾炎。诊断HBV-GN标准:患者表现为①、②和③;患者表现为①和②,但④中为膜性肾病;个别患者表现为②和③,血清中乙肝病毒抗原或抗体阴性也可确诊。
2 肾脏病理结果 所有患者肾脏标本均通过肾脏穿刺活检所得,标本常规做HE和PASM染色。通过光镜检查了解肾脏形态学变化,所有标本做免疫荧光检测IgG、IgA、IgM、C3、C4,并行电镜检查;肾脏标本中的HBsAg和HBcAg监测是通过在冰冻切片上行间接免疫荧光法。
3 治疗方法 患者一般治疗包括:改善肝功能、降血压、抗生素治疗、脱水利尿等。对照组是在一般治疗的同时联用恩替卡韦分散片(国药准字H20100019;生产批号20101031),给药方式为口服,每天一次,每次0.5 mg。治疗组在对照组治疗基础上加用霉酚酸酯胶囊(国药准字20031240;生产批号20101213),给药方式为口服,每天一次,每次1 g,可根据患者具体病情调整给药量,每天服药量不超过2 g。患者给药治疗时间为6个月。
4 观察指标 记录患者入院时的实验室指标:包括血清乙肝病毒标志物、HBV-DNA定量、丙氨酸转氨酶(ALT)、天门冬氨酸转氨酶(AST)、白蛋白(ALB)、血肌酐(Scr)、24 h尿蛋白(UPRO)。观察患者治疗有效情况。
5 治疗效果评定 完全缓解:尿蛋白多次监测为阴性,UPRO≤0.2 g/24h,ALB≥35 g/L,HBV-DNA滴度转阴,肝肾功能正常,临床症状和体征消失;显著缓解:UPRO <1.0 g/24h,血ALB显著改善,HBV-DNA滴度转阴,肝肾功能正常,临床症状和体征消失;部分缓解:尿蛋白定量较治疗前下降>50%,肾功能稳定,ALB较治疗前升高>30 g/L,ALT、HBV-DNA滴度较治疗前下降>50%,但均未降至正常范围,肝肾功能基本正常,临床症状和体征基本消失;无效:临床症状及实验室检查无明显改善。
结 果
1 两组患者治疗效果对比 见表1。治疗组总有效率88.9%显著高于对照组的53.3%,两组比较有统计学差异(χ2=5.215,P=0.022)。
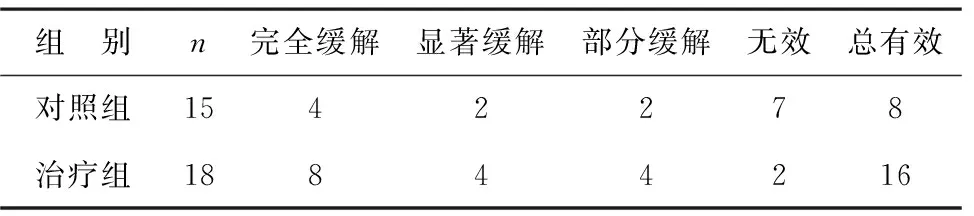
表1 两组患者治疗效果对比(例)
2 两组患者治疗前后ALB、UPRO、肝肾功能及HBV-DNA表达变化 见表2。治疗前两组间UPRO、Scr、ALT、AST、ALB及HBV-DNA对比无统计学差异(P>0.05);治疗后两组患者的UPRO、Scr、ALT和AST都有降低,ALB升高,但在治疗组患者中,各项临床治疗变化有统计学差异(P<0.05),而HBV-DNA治疗后两组之间表达变化,无统计学差异(P>0.05)。

表2 治疗前后ALB、24 h尿蛋白、肝肾功能及HBV-DNA表达变化
注:与同组治疗前相比,#P<0.05;与对照组治疗后相比,&P<0.05
3 不良反应 两组治疗期间均未发现明显的不良反应。
讨 论
乙型肝炎病毒(HBV)主要侵犯累及肝脏,但也可以造成肝外器官的病变与损害。HBV-GN是我国常见的继发性肾小球疾病之一,其发病机制尚不明确,可能为循环免疫复合物被动滞留;原位免疫复合物形成;自身免疫反应;HBV直接感染,这些结果可能是病毒、宿主和环境因素相互作用的产物。HBV-GN患者临床上以男性多见,常表现为肾病综合征,其次为无症状性尿检异常和肾炎综合征,该病导致的高血压发生率较低[4]。HBV-GN病理类型多样化,多数学者认为其病理类型以MN、MPGN为主,可表现为MN、MsPGN、MPGN、IgAN等,也有学者认为成人主要以IgAN为主,儿童以MN为主[5]。在临床治疗中,由于患者存在HBV感染与免疫介导的炎症共存而导致其治疗棘手,目前尚无规范化和有效的治疗方案。对于HBV-GN的临床治疗主要有:抗病毒、激素及免疫抑制剂、中西医结合治疗等[6]。近年来,联合或序贯使用两者或两种以上不同作用机制的药物进行治疗成为研究热点,但仍以抗病毒治疗为主,糖皮质激素及免疫抑制剂的应用与否及其应用的疗程和剂量尚存在争议。
作为鸟嘌呤核苷类似物,恩替卡韦可以通过抑制HBV-DNA反转录、复制和转录病毒复制,而抑制HBV-DNA的合成,是一种新的抗乙型肝炎病毒的一线药物。该药抗乙型肝炎病毒作用极强,在各个阶段都有作用例如:病毒DNA的复制、逆转录负链及正链的延长。恩替卡韦的半衰期大约为14~15 h,所以对于患者长期服用而反生的耐药率很低[7]。其临床治疗效果优于拉米夫定,5年以上的耐药突变率低,因此该药适合长期服用[8]。本组病例结果显示,两组患者治疗后患者HBV-DNA较治疗前均明显下降(P<0.05),表明恩替卡韦能够有效抑制HBV-DNA的复制。
在HBV-GN治疗中,针对免疫复合物沉积既往常用的药物包括:糖皮质激素或环磷酰胺、硫唑嘌呤等,但是收效甚微。激素治疗一方面抑制免疫复合物沉积,另一方面又降低了机体对HBV的清除。激素可导致病毒DNA复制增多,从而增加乙肝病毒再激活或复发的几率。而其他免疫抑制剂如环磷酰胺、硫唑嘌呤等又具有较强的肝毒性,使本已被乙肝病毒累及的肝脏功能进一步受损,患者常常不能耐受长期服用[9]。作为一种新研制的免疫抑制剂,霉酚酸酯在体内可被水解为麦考酚酸。麦考酚酸对鸟嘌呤核苷酸经典合成途径起到抑制作用,而不会改变其补救途径,所以该药只对淋巴细胞DNA和RNA的合成起到抑制作用,对其他细胞特别是肝细胞、骨髓细胞的影响很小。霉酚酸酯能够选择性抑制T、B淋巴细胞的复制和增殖,抑制粘附分子的糖基化,抑制机体特异性抗体的形成,减少或抑制细胞因子的产生[10]。霉酚酸酯的优点为即具有免疫抑制作用,又无明显的肝、肾毒性和骨髓抑制效果,没有高血压、骨质疏松、性腺抑制等不良反应,使用过程中继发性感染的发生率低,无明显的并发症。鉴于其在免疫介导性疾病中的作用及较少的不良反应,霉酚酸酯已被用于治疗免疫介导的肾脏疾病[11]。同时霉酚酸酯具有良好的口服利用度,疗效窗口宽,便于患者长期口服[12]。霉酚酸酯对比以往的免疫抑制剂,其特点在于:免疫抑制作用稍弱。但是这种较弱的免疫抑制作用,既能抑制免疫复合物沉积,又会降低乙肝病毒再激活或复发的几率,所以该药联合抗病毒药物对HBV-GN患者尤为合适。
本组病例结果显示,治疗组总有效率较高;治疗组患者24 h尿蛋白及Scr较前均明显下降(P<0.05),表明霉酚酸酯清除免疫复合物能力较佳,同时治疗组24 h尿蛋白及Scr较对照组下降更为明显,说明对HBV-GN患者同时给予免疫抑制剂更能有效改善肾脏功能。治疗组患者治疗后ALB显著增加,而ALT和AST下降明显(P<0.05),而治疗组改善更为明显,表明霉酚酸酯在清除免疫复合物能的同时对患者肝功能影响程度有限,安全性较好。
总之,我们的研究提示,在治疗HBV-GN中恩替卡韦联合霉酚酸酯疗效显著,且患者耐受性好,安全性高。所以恩替卡韦联合霉酚酸酯在治疗HBV-GN中值得推广,但尚需进一步研究药物间的联合作用。

