器质性与非器质性房性早博24小时心率变异性分析
陈芹 陈士金
1.三峡大学第二人民医院(宜昌市第二人民医院)心电图室;2.三峡大学第二人民医院(宜昌市第二人民医院)心内科,湖北宜昌 443000
房性心律失常包括房性期前收缩(房早)、房性心动过速、心房扑动、心房颤动等多种类型,其发生机制与折返激动、触发活动、异位起搏点兴奋性增高有关[1]。其中,非器质性房早患者临床症状一般不明显,通过去除诱因、心理干预、行为纠正等疗法,往往可得到明显改善;器质性房早患者发病时基础心脏疾病可明显加重,并伴有心悸、呼吸困难、胸痛等症状,预后质量一般[2]。大量研究显示,心律失常的发生与自主神经功能变化有关,而心率变异性能够为自主神经功能评估提供可靠参考[3-4]。因此,本文对比器质性与非器质性房早患者心率变异性特点。
1 资料与方法
1.1 一般资料
本研究已征得我院医学伦理委员会批准。将2014年7月至2017年10月收治的219例房早患者纳入此次研究,器质性组108例、非器质性组111例。患者均经心电图、动态心电图、超声心动图检查明确房早诊断[5],近2周内无抗心律失常药物使用史,对此次研究知情同意且自愿参与;排除合并室速、室颤、持续性房颤、起搏器植入者,以及合并其他内外科危急重症者。
1.2 检测方法
两组患者均接受24小时心率变异性检测,使用BMS Century 3000 24小时动态心电图分析系统(美国世纪公司),行24小时心电信号连续检测。导联选择[6]:V1:胸骨右缘第4肋间;V2:胸骨左缘第4肋间;V3:V2与V4连线中点;V4:左锁骨中线与第5肋间交叉处;V5:左腋前线与V4相同水平线;V6:腋中线V4相同水平线,以及左右锁骨下窝中1/3处及左右下胸壁各粘贴1个电极。向患者详细介绍动态心电图记录过程中注意事项,嘱患者详细记录工作、休息、活动、就餐、服药等日常活动情况,若期间出现房早相关症状,由患者详细记录症状发生时间、持续时间、症状感受,并于24小时后回院撤机。
1.3 分析统计方法
动态心电图仪撤机后,将数据导入分析软件,软件自动进行抗噪去干扰、去除异位节律等处理后,获取24小时心率变异性指标(时域指标),包括全部窦性R-R间期的总体标准差(SDNN)、均值标准差(SDANN)、SDNN指数(SDNNindex)、差值均方的平方根(RMSSD)及相邻NN间期相差>50 ms的个数占总心跳次数百分比(PNN50)[7]。按照患者房早类型,将其分别纳入偶发房早亚组、复杂房早亚组。偶发房早:动态心电图示房早<100次/24小时;复杂房早:动态心电图示房早>700次/24小时,伴多源房早、成对、呈联律或短阵房速[8]。对比各组患者24小时心率变异性指标差异,采用SAS 9.2进行分析,计量资料以()表示,并采用t检验,相关性分析采用Pearson法,计算上述指标与器质性、非器质性房早频率的关系,以P<0.05为差异有统计学意义。
2 结果
2.1 亚组分组结果
器质性组108例患者中,47例为偶发房早,61例为复杂房早;非器质性组111例患者中,51例为偶发房早,60例为复杂房早。
2.2 各组患者24小时心率变异性指标比较
器质性组复杂房早亚组SDNNindex、RMSSD、PNN50低于偶发房早亚组;非器质性组偶发房早亚组SDNN、SDNNindex、RMSSD、PNN50高于器质性组偶发房早、复杂房早亚组,其复杂房早亚组SDNN、PNN50均高于器质性组偶发房早、复杂房早亚组,其复杂房早亚组SDNNindex、RMSSD高于其他各组,差异有统计学意义(P<0.05)。见表1。
表1 各组患者24小时心率变异性指标比较()
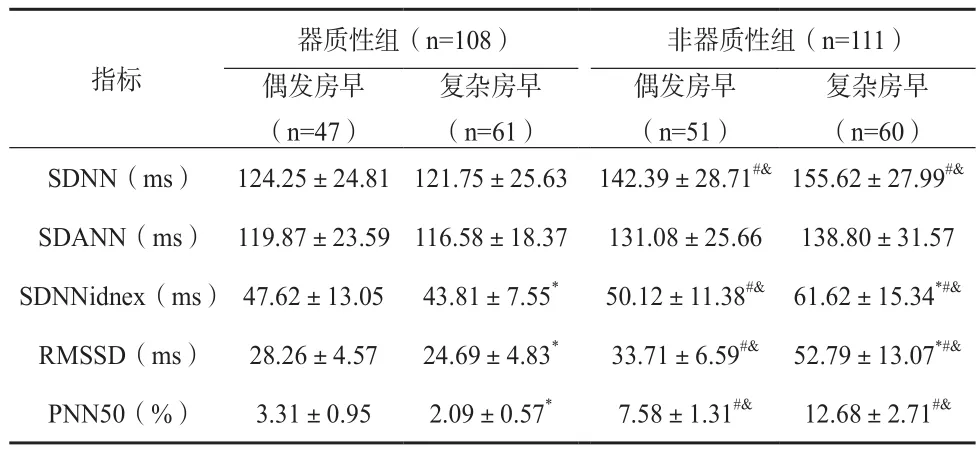
表1 各组患者24小时心率变异性指标比较()
注:与同组偶发房早亚组比较,*P<0.05;与器质性组偶发房早亚组比较,#P<0.05;与器质性组复杂房早亚组比较,&P<0.05
复杂房早(n=60)SDNN(ms) 124.25±24.81 121.75±25.63 142.39±28.71#&155.62±27.99#&SDANN(ms) 119.87±23.59 116.58±18.37 131.08±25.66 138.80±31.57 SDNNidnex(ms) 47.62±13.05 43.81±7.55* 50.12±11.38#& 61.62±15.34*#&RMSSD(ms) 28.26±4.57 24.69±4.83* 33.71±6.59#& 52.79±13.07*#&PNN50(%) 3.31±0.95 2.09±0.57* 7.58±1.31#& 12.68±2.71#&指标器质性组(n=108) 非器质性组(n=111)偶发房早(n=47)复杂房早(n=61)偶发房早(n=51)
2.3 24小时心率变异性指标与房早频率的相关性
Pearson相关性分析示,SDNN与器质性房早患者房早频率呈负相关,RMSSD、PNN50与非器质性房早患者房早频率呈正相关(P<0.05)。见表2。
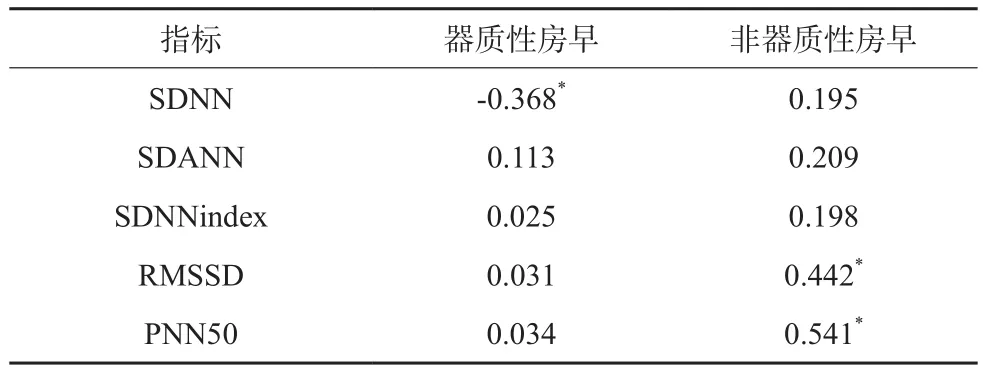
表2 24小时心率变异性指标与房早频率的相关性分析(r值)
3 讨论
房早当有明显症状或因房早触发室上性心动过速时,应给予治疗。因此,除早期诊断外,房性心律失常的危险分层评估与干预策略制定也至关重要[9]。心律失常与自主神经功能紊乱具有密切关联,而心率变异性能够为自主神经功能的无创定性、定量评估提供可靠参考[10]。心率变异性是指连续逐次窦性心搏RR间期之间的差异,可同时反映心脏交感神经及迷走神经功能状态,并体现出自主神经对心率调节的能力[11]。在心率变异性的时域分析指标中,SDNN能够反映自主神经功能的整体变化,SDANN与心率变化中长期变化成分有关,RMSSD常用于快变化成分大小的判断,而PNN50则可描述心动周期的逐搏变异特点[12]。在本次研究中,非器质性组复杂房早亚组SDNN、RMSSD、PNN50大幅升高,说明患者自主神经功能及迷走神经功能处于明显亢进状态,此时钾外流增多、钙内流减少,是造成心房不应期缩短、异位激动点兴奋阈值降低的主要原因,而上述变化可造成房室传导减慢、促进房早发生[13-14]。对于该类患者,β受体阻滞剂往往难以取得理想的治疗效果,应考虑自主神经调节药物[15]。
器质性心脏病伴偶发房早时,患者心率变异性呈下降状态,考虑与器质性心脏病所致迷走神经功能损伤有关,同时,患者往往伴有交感神经功能相对亢进,此时心房肌细胞兴奋性上升,但血浆高儿茶酚胺水平使得心肌对窦性心律的调节作用受限,故即便存在较大的张力波动,患者心率变化幅度仍较低[16-17]。在去除诱因、治疗基础疾病的前提下,β受体阻滞剂对该类房早的治疗效果值得肯定。器质性心脏病伴复杂房早时,患者心率变异性进一步下降,说明患者迷走神经功能损伤及交感神经功能均较为严重,而该类患者有着致命性快速性心律失常发生风险[18],各类基础疾病、抗心律失常药物的使用尤为必要。
综上所述,不同病因、不同类型房早患者心率变异性存在明显差异,器质性心脏病伴房早者心率变异性下降,且复杂房早往往伴有心率变异性的进一步下降,而非器质性心脏病伴房早患者心率变异性有所上升,且复杂房早者心率变异性上升更为明显,其原因可能与迷走神经、交感神经功能变化有关。

