甲氨蝶呤联合艾拉莫德治疗活动性类风湿关节炎的随机对照试验
莫美丽, 唐东兴, 张 筠, 刘 阳, 谢立虎
类风湿关节炎(rheumatoid arthritis,RA)是一种全身性自身免疫性疾病,其关节病理表现为滑膜炎而关节外主要表现为血管炎,可导致关节破坏、畸形和残疾,早期诊断及规范治疗是改善RA预后的关键。甲氨蝶呤(methotrexate,MTX)是治疗RA的基础用药,被广泛用于与其他抗风湿药联合用药,如柳氮磺胺吡啶、来氟米特、雷公藤多苷片、硫酸羟氯喹等。近年来,文献报道MTX与生物制剂,如依那西普、英夫利昔单抗、阿达木单抗等联合用药治疗RA也取得显著疗效[1]。艾拉莫德是一种新型小分子抗风湿药物,由于患者对可用药物的疗效、毒性和费用等方面的需求存在差别,因此使用艾拉莫德等新型小分子抗风湿药物与MTX联合治疗为RA患者提供了更多的选择,特别是在变更药物和减少治疗费用方面。艾拉莫德有独特作用机制,能够有效降低疾病的活动性[2]。研究发现,在培养的人滑膜细胞和急性单核细胞中,艾拉莫德可抑制转录因子kappaB的活化,进而抑制肿瘤坏死因子-α(tumor necrosis factor,TNF-α)诱导的炎症因子[如白细胞介素(interleukin, IL)-1,IL-6,IL-17,单核细胞趋化因子]的表达[3-5]。Tanaka等发现,艾拉莫德还通过直接作用于B细胞而不影响其增殖来降低免疫球蛋白(immunoglobulin, Ig)的表达[6]。本研究观察活动期RA患者治疗12周后的临床疗效,报告如下。
1 对象与方法
1.1对象 选取2015年11月—2017年4月在南华大学附属第二医院就诊的门诊和住院 RA 患者60例,按数字随机方法分为治疗组和对照组,每组30例。治疗组男性8例,女性22例;年龄(45±11.56)岁(33~57岁);病程(9.05±7.00)月(6~36月)。对照组男性6例,女性24例;年龄(43.30±10.25)岁(31~53岁);病程(9.8±6.5)月(7~38月)。研究期间治疗组及对照组均无脱漏及失访。2组患者在年龄、性别、病程及疾病活动性评分(disease activity score,DAS)28 方面比较,差别均无统计学意义(P均>0.05)。本研究通过南华大学附属第二医院伦理委员会批准,并获取患者签字同意。
1.2入组标准 病程≥6月,符合1987年美国风湿病学会(American college of rheumatology,ACR)RA分类标准或ACR/欧洲抗风湿联盟2009年RA分类标准,且ACR功能状态分类为Ⅰ~Ⅲ级活动性RA患者:(1)晨僵持续时间≥1 h;(2)关节压痛≥5个;(3)关节肿胀≥3个;(4)血沉(erythrocyte sedimentation rate, ESR,魏氏法)≥28 mm/h。
1.3排除标准 (1)对药物过敏或过敏体质者;(2)有重要脏器疾病或严重感染,肿瘤患者;(3)孕妇,哺乳期妇女;(4)胃、十二指肠活动性溃疡患者;(5)有乙肝或丙肝患者;(6)1年内未使用过生物制剂或未按规定用药或中断治疗者。
1.4治疗方法 治疗组予以 MTX 片(批号:H31020644,上海信谊药厂有限公司),每周10 mg,每周1次;同时联用艾拉莫德(批号:H20110084,先声药业有限公司),每天50 mg,分早晚各25 mg服用。对照组给予MTX,剂量及服用方法同治疗组;同时联用雷公藤多苷片(批号:243020138,湖南协力药业有限公司)20 mg/次,每天3次口服。12周内各药剂量保持不变,2组疗程均为12周。患者在第1次用药前及用药第4,8,12周到医院接受随访。记录患者的不良反应、症状、体征及相关实验室检查。
1.5伴随治疗 2组患者早期均服用剂量稳定的甲泼尼龙(每天8 mg),并辅以补充叶酸、维生素D、钙剂等对症治疗。在研究过程禁止合并使用其他改变病情的抗风湿药、生物制剂等影响本病疗效的药物。
1.6观察指标 评估治疗第0,4,8,12周时患者的临床症状,包括:晨僵时间、关节压痛数(28 个关节计)、关节肿胀数(28个关节计);医生对病情总体评价(采用VAS 评价,0~100 mm);患者对病情总体评价(采用VAS 评价,0~100 mm);关节疼痛评分(采用VAS 评价,0~100 mm);健康问卷(health assessment questionnaire, HAQ)评分。另外检测相关实验室指标,如ESR,C-反应蛋白(C-reactive protein, CRP),抗环瓜氨酸抗体(anti-cyclic citrullinated peptide antibodies,A-CCP),类风湿因子(rheumatoid factors,RF)和免疫球蛋白(IgG,IgM,IgA)。

2 结 果
2.1DAS28评分比较 在治疗第0,4周时,2组患者的DAS28评分比较,差别无统计学意义(P>0.05);治疗第8周时,治疗组的DAS28评分较对照组明显下降,差别有统计学意义(P<0.05)。治疗第12周时,治疗组的DSA28评分与对照组比较,差别无统计学意义(P>0.05,表1)。
2.2实验室指标变化比较 2组患者在治疗12周后,ESR及CRP等指标与治疗前比较明显下降,差别有统计学意义(P<0.05);治疗12周后,治疗组的RF,IgG及IgM与治疗前、对照组比较,差别均有统计学意义(P<0.05,表2)。

表1 2组患者治疗后DSA28评分的比较
与对照组比较,△:P<0.05.
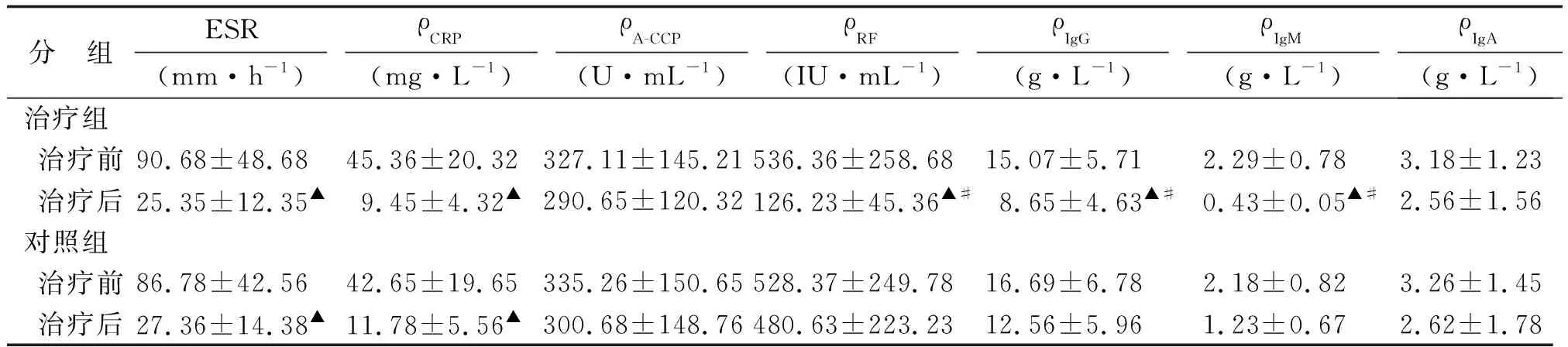
表2 2组治疗前、治疗12周后各实验室检查指标比较
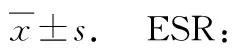
2.3不良反应 2组患者均未出现严重不良反应。治疗组有1例患者转氨酶轻度升高,对照组有2例转氨酶轻度升高,予以护肝药治疗后转氨酶均恢复正常。2组各有1例患者出现食欲下降、恶心,经对症治疗后好转。
3 讨 论
RA是一个以累及周围关节为主的系统性炎症性自身免疫疾病,其病因及发病机制仍不完全清楚。研究显示,TNF-α,IL-1,IL-6及IL-17等细胞因子在RA的发病和炎症过程中至关重要[7],同时还伴有T,B淋巴细胞的浸润。RA是最常见的风湿性疾病之一,早期诊断及规范治疗是提高RA预后的关键。近年来,随着研究的深入及医患重视的不断提高,早期使用改变病情的抗风湿药使RA的疗效有了显著提高。
本研究显示,MTX联合艾拉莫德在治疗第8周时RA患者的症状及体征显著改善,DSA28评分较对照组明显降低。但2组方案在治疗12周时临床疗效无明显差别,提示MTX联合艾拉莫德在用药8周即起效,较对照组快,与孟德钎等报道的结果相似[8],进一步说明MTX联合艾拉莫德治疗活动性RA的远期疗效与MTX联合雷公藤多苷片相当,但患者症状改善更快。笔者推测可能与艾拉莫德抗炎、镇痛有关。目前已有众多动物实验表明,艾拉莫德能有效抑制体外成纤维细胞释放前列腺素及缓激肽生成。本研究还显示,MTX联合艾拉莫德能显著降低RF,IgG及IgM水平,与Hara等报道的结果相似,该研究还发现此作用可至少维持至52周[9]。因此,MTX联合艾拉莫德具有独特免疫作用机制,且MTX联合艾拉莫德的安全性与对照组相似,2组主要不良反应为消化道症状,如恶心、呕吐及轻度转氨酶升高,均较轻且少见,予护肝及对症治疗后症状改善,无骨髓抑制、月经量减少及紊乱等。
在一项随机双盲实验中,活动性 RA 患者单用MTX,ACR的改善率为30.7%;加用艾拉莫德治疗24周后,改善率提高至69.5%(P<0.001),而ACR50、ACR70、健康评估问卷、DSA28评分及RF也显著改善;其不良反应表现为白细胞减少、贫血、鼻咽炎等,均相当轻微,未出现严重的不良事件[10]。同样Hara等对艾拉莫德的疗效与安全性的试验中,其疗效及安全性与柳氮磺胺吡啶相同,且对其他改变病情的抗风湿药无效的难治性RA患者有效[9]。
在一项艾拉莫德治疗RA的研究显示,艾拉莫德的总有效率较MTX高(95.24%vs80.54%,P<0.05)[11]。邵德宏报道,MTX联合艾拉莫德治疗难治性RA患者与单用MTX的总有效率比较,差别有统计学意义(96.25%vs66.25%,P<0.05),2组不良反应的差别无统计学意义[12]。因此,进一步说明MTX联合艾拉莫德治疗RA疗效肯定且安全。
艾拉莫德是一种细胞因子抑制剂,对TNF-α刺激下的体外培养的滑膜细胞有抑制增殖的作用,且明显降低趋化因子IL-8分泌水平[13];它可减少Ig的产生,其机制是通过直接作用于B细胞而不影响其增殖[6];改善骨代谢,促进骨形成,抑制骨破坏[14];通过降低金属蛋白酶-1、金属蛋白酶-3的蛋白和mRNA水平,进而抑制RA滑膜成纤维细胞对骨质侵袭[15];另外,艾拉莫德有一定抑制环氧化酶-2的作用,可减少炎症反应中缓激肽的增加及前列腺素释放[16]。
综上所述,MTX联合艾拉莫德治疗活动性RA疗效确切,并且起效快,安全性高,但其对RA的远期疗效有待进一步研究。

