壳聚糖基创伤敷料在伤口处理过程中的作用机制与应用
周亚平,刘吉伟,李学明
(南京工业大学药学院,江苏南京211800)
早期人们用植物的叶子、动物的皮肤等覆盖在伤口表面保护伤口,这是最早的创伤敷料形式。随着研究的深入,研究者们开发了复合敷料,将具有愈合作用的各种药材相互混合,但是愈合缓慢[1]。值得关注的是,新材料开发使得创伤敷料类型及功能多样化,主要包括天然生物材料类敷料、人工合成材料类敷料和矿物质类敷料等,其中天然生物材料具有良好的研究和应用前景。天然生物材料类创伤愈合敷料具有良好的生物相容性、生物可降解性、止血、加速愈合及抗菌杀菌等优良性能,而价格低廉、原料易得、不易引起过敏、易于移除等特性的天然生物材料类创伤愈合敷料更是得到研究者的特别关注[2]。
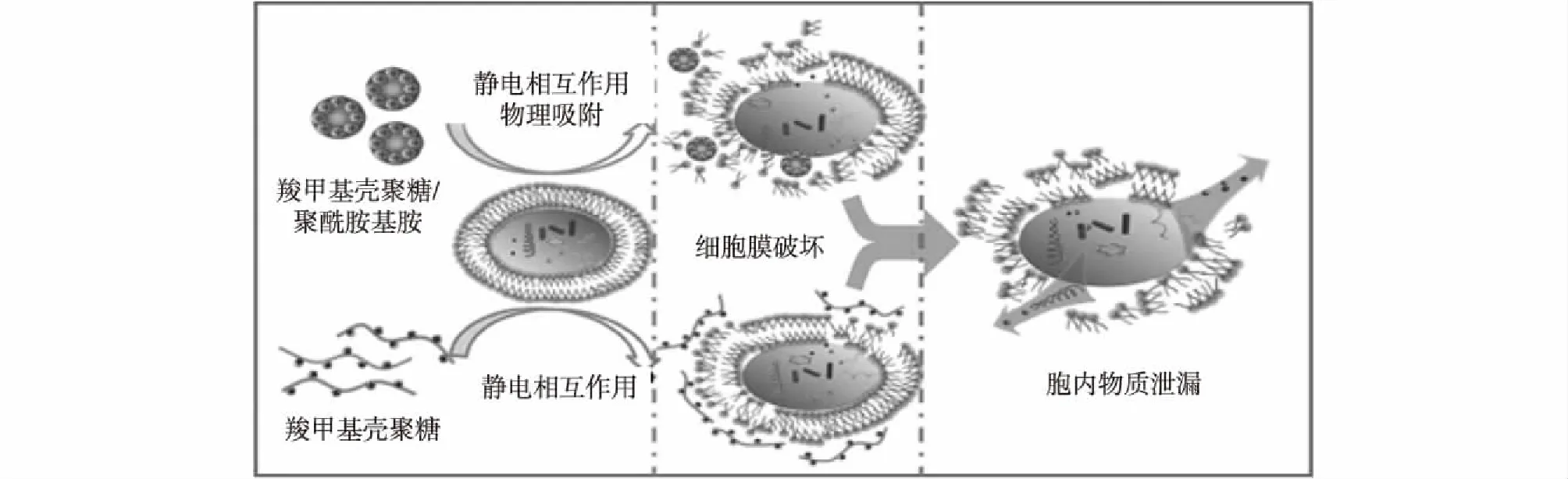
图2 壳聚糖抗菌机制Fig.2 Antibacterial mechanism diagram of chitosan
壳聚糖又称脱乙酰甲壳素,是带正电的碱性多糖,由自然界广泛存在的几丁质经脱乙酰反应得到的,化学名称为β-(1→4)-2-氨基-2-脱氧-D-葡萄糖。1859年法国人Rouget首先将甲壳素置于NaOH溶液中加热得到易溶于有机酸的壳聚糖[3]。壳聚糖具有良好的生物相容性、生物可降解性、止血、抑菌杀菌、促进伤口愈合等多种优良性能[2],因此被广泛应用于医药、生物工程和食品加工等研究领域。甲壳素来源广泛,尤其是甲壳类动物,如虾壳、蟹壳等,每年从不同来源生产的甲壳素达1 000亿t。因此,由甲壳素提取得到的壳聚糖在生物医药领域获得了广泛应用,主要用作止血剂、抗菌剂、伤口敷料和支架等。市售壳聚糖基止血材料HemCon©止血绷带和Celox©止血粉,已经获得FDA批准,目前这2种材料已经成为美军人手必备的急救物品。

图1 壳聚糖结构式制Fig.1 Structural formula of chitosan
1 壳聚糖在伤口处理过程中的抗菌作用
当机体出现伤口时,如果不作任何处理将会引起伤口感染,从而引发很多炎症反应,所以,理想的创伤敷料应该具备有效的抗菌活性。近年来,壳聚糖用作抗菌剂备受关注,壳聚糖及其衍生物对细菌、真菌、病原菌等微生物都具有显著的抑菌杀菌功能,在伤口处理的过程中可以作为良好的抗菌剂,保护伤口免受感染[4]。壳聚糖发挥抗菌作用有2个主要的抗菌机制:第1种机制是细菌细胞表面带有阴离子基团,壳聚糖是阳离子聚合物,两种带相反电荷的物质之间产生静电相互作用,在细菌细胞周围形成了不透水层,抑制重要的物质转运,从而产生抑菌功效,如图2所示[5];第2种机制是壳聚糖能够侵入细菌细胞核,抑制了细菌RNA及蛋白质合成,研究表明低分子量的壳聚糖或壳寡糖抑制作用更加明显[6]。
壳聚糖抗菌活性受多种因素影响,内在因素包括分子量、浓度及脱乙酰度等,外在因素包括微生物种类、细菌细胞的胞龄、壳聚糖衍生物和壳聚糖敷料形态等。壳聚糖侧链基团的存在,影响壳聚糖抗菌活性,壳聚糖衍生物的开发能够提高壳聚糖的抗菌活性。杂环或芳香族部分取代基的引入可以增加抗真菌活性,研究表明脂肪族侧链可以增加壳聚糖抗真菌活性,如Rabea等[7]通过还原胺化反应制备不同的N-苄基壳聚糖衍生物对德巴利腐霉和尖孢镰刀菌具有显著的抗真菌活性;Jia等[8]合成N-(1-羧基丁基-4-吡啶鎓)壳聚糖氯化物,对灰霉病菌和番茄叶霉病表现出良好的抗真菌活性;Guo等[9]利用O-羧甲基壳聚糖还原胺化制备的N-苄基羧甲基壳聚糖衍生物表现出对尖孢镰刀菌和番茄早疫病菌的抗真菌活性;而Sun等[10]发现磺基化壳聚糖对金黄色葡萄球菌具有良好的抗菌作用。
抗生素与壳聚糖协同作用能有效地提高壳聚糖基敷料的抗菌性能,但是,近年来由于抗生素的滥用导致了多药耐药菌的出现,增加了伤口感染风险[11]。研究者发现无机材料也具有一定的抗菌效果,为进一步提高壳聚糖基抗菌敷料的应用,Lu等[12]向聚糖基敷料中加入无机材抗菌剂如纳米Ag2O及纳米ZnO等,有效地提高了抗菌效果,同时扩大壳聚糖在抗菌方面的应用。随着研究的深入,研究人员发现无机抗菌剂也存在一些不足[13],如无机抗菌剂不具备生物可降解性,不能被机体内源性吸收,所以,开发具有生物相容性、生物可降解性的新型抗菌材料与壳聚糖协同作用,对提高壳聚糖基敷料抗菌方面的应用具有重要意义。
2 壳聚糖在伤口处理过程中的止血作用
导致失控性出血的严重创伤是全球公共卫生问题,创伤性伤害造成的死亡占了意外事故死亡率约十分之一,全世界每年超过580万人死亡,预计这一死亡人数将会在2020年上升到800万[14-15]。伤口部位严重出血若不及时处理,将会出现感染,严重情况下将会出现危及到生命的脓毒症[16],所以开发高效快速的止血剂在生物医药材料发展中极其重要。新型止血材料包括明胶、微纤维胶原、纤维蛋白胶、凝血酶、氧化纤维素或氧化再生纤维素、壳聚糖等,通过对比研究,壳聚糖基止血敷料是非常有效的止血剂,目前,基于壳聚糖及其衍生物的止血剂广泛应用于患者术后出血控制。研究发现壳聚糖凝血机理与壳聚糖正电性相关,壳聚糖聚合物表面的正电基团能够和红细胞膜上的负电基团相互吸引,使得红细胞相互聚集达到凝血的效果,同时加快凝血因子启动,增强凝血,如图3(AnsCareTMChitoClot Bandage安适康壳聚糖止血绷带)。随着研究深入,Yang等[17]发现固态壳聚糖和壳聚糖溶液遵循不同的止血机制,固态壳聚糖利用对液体的吸收作用达到止血的效果,壳聚糖溶液主要利用其正电性对带负电红细胞进行吸附作用止血。

图3 壳聚糖止血作用机制Fig.3 Hemostatic mechanism of chitosan
虽然壳聚糖基止血材料具有快速止血的特性,但是在其应用过程中仍然存在一些缺陷,这些缺陷限制了壳聚糖基止血剂的应用。HemCon止血剂在动物出血模型中能有效止血,但是临床试验发现其不能控制过度出血情况;Celox止血剂会诱导产生严重的炎症反应[18-19]。为了弥补这些缺陷,较有前景的方法是向基质中添加无机材料对壳聚糖进行修饰,形成有效的凝血复合支架[20],如载银壳聚糖-聚磷酸盐复合敷料,因多聚磷酸盐的加入提高了止血性能[21];Liu等[22]研究发现向敷料中掺入黏土矿物可以有效地改善支架性能,如向壳聚糖基材料中加入埃洛石纳米管(HNTs),随着HNT含量的增加,不仅能提高壳聚糖支架的力学性能,还能提高止血性能。研究表明壳聚糖和CaCO3协同作用可有效促进凝血[23],故本实验室目前正在设计壳聚糖/ CaCO3凝胶创伤敷料,一方面利用CaCO3促进凝血作用,另一方面CaCO3能够在酸性条件下生成促凝因子Ca2+加速凝血。然而无机材料不具备生物可降解特性,所以开发壳聚糖搭载生物可降解特性物质,改善壳聚糖力学性能,提高止血特性是重要的研究方向。
3 壳聚糖在伤口处理过程中的伤口愈合作用
伤口愈合是受损伤组织恢复完整的过程,伤口愈合能够防止生物体丧失生理平衡。伤口愈合是一个复杂的过程,涉及凝血、炎症、细胞增殖、瘢痕形成期、表皮及其他组织再生。壳聚糖基创伤敷料作为理想的伤口敷料,拥有良好的创伤愈合作用,具有良好的生物相容性和生物可降解特性,另外,壳聚糖具有很强的组织黏附性,能够更好地合成瘢痕组织以及对伤口收缩具有促进作用[24]。
研究发现,壳聚糖创伤愈合敷料的愈合机制为壳聚糖可以有效地降解释放N-乙酰-β-D-氨基葡萄糖,该物质在伤口愈合过程中可以促进成纤维细胞的增殖;壳聚糖单体有助于创伤部位有序沉积,刺激创伤部位透明质酸的合成增加;壳聚糖为皮肤组织的再生提供了纤维素基质,激活巨噬细胞,阻止异常的生长活性,加快全层皮肤的愈合,阻止瘢痕生成,所以壳聚糖及其衍生物可以用作理想的伤口愈合材料[25]。目前壳聚糖基创伤愈合材料有凝胶、海绵、膜、纳米粒、微粒及纳米纤维等不同形式[26-30]。
伤口愈合是一个复杂的过程,Mao等[31]设计的Ag/Ag@AgCl/ZnO杂化纳米结构,在光催化条件下释放Ag+和Zn2+,刺激免疫产生大量的白细胞和嗜中性粒细胞,协同抗菌并加速伤口愈合;壳聚糖凝胶-纳米ZnO复合敷料,充分利用无机材料提高壳聚糖凝胶力学性能的同时,协同促进愈合作用[32];生长因子在创伤愈合中起到非常重要的作用,但是单一的蛋白疗法必须持续释放才能够对伤口愈合产生强效的促进作用,而蛋白治疗剂半衰期短,大剂量使用不仅增加成本,还可能导致脱靶效应,研究发现可以将生长因子和凝胶载体材料相结合,提高凝胶的力学特性,解决生长因子半衰期短的问题,达到高效促进慢性创伤愈合的作用。随着对创伤愈合研究的深入,新型的愈合技术及创伤愈合材料慢慢出现,如何将这些新方法新材料同壳聚糖基创伤敷料联用,提高愈合效果及力学性能,对壳聚糖创伤愈合敷料的开发具有重要研究意义[33-35]。
4 壳聚糖在伤口处理过程中的镇痛作用
镇痛药是指可以减轻疼痛的一种药物,一般情况下,和抗炎作用有关的药物,大多数都可以镇痛。壳聚糖具有许多生物医学方面的应用优势,目前被认为是一种理想的创伤敷料。通过对壳聚糖和甲壳素镇痛差异研究,发现壳聚糖具有更强的镇痛效果,有人提出这种镇痛效果是由壳聚糖阳离子特性产生,壳聚糖上的氨基可以吸收炎症部位的质子,达到减轻炎症、镇痛的效果。而酸性条件下,壳聚糖溶液中游离的伯氨基降低了所在区的pH,能够起到长效镇痛的作用[36],但是,镇痛效果并不显著。有研究发现含有吗啡的壳聚糖和N,O-羧甲基壳聚糖产品能够提供8~12 h的镇痛效果,所以,将壳聚糖基创伤敷料与镇痛药联合开发,能有效地提高创伤敷料镇痛效果,减轻患者的疼痛[37]。
5 结论与展望
壳聚糖是自然界唯一的带正电的碱性多糖,在创伤愈合过程中发挥重要的作用,具有良好的生物相容性、生物可降解性、止血、抗菌、愈合、镇痛及无毒等特性,可以作为良好的抗菌剂、止血剂、愈合剂以及镇痛剂。随着对伤口处理过程研究的深入,影响创伤愈合的因素很多,虽然壳聚糖表现出适应伤口愈合全过程的功能特性,但是单一使用壳聚糖满足不了生物医学的需求,而壳聚糖在研究和应用过程中存在一些缺点,如壳聚糖只有在溶液中才能产生有效的抗菌效果;凝胶、海绵和膜等形式的壳聚糖基敷料,力学性能较差,这些都是需要解决的问题。
本篇综述主要讨论壳聚糖作为创伤敷料,在抗菌、止血、愈合和镇痛方面的机理及应用,并且对壳聚糖在应用过程中存在的缺陷进行分析,结合目前创伤研究新进展新发现,提出改进方法,进一步提高壳聚糖的应用。创伤处理是一个复杂的过程,涉及止血、抗菌和瘢痕生成等,壳聚糖表现出这些特征,但仍然存在一些问题,通过对壳聚糖衍生化修饰,有助于提高壳聚糖抗菌谱;同新型止血材料、抗菌材料及抑制瘢痕生成材料协同作用,可以有效地提高创伤处理效果;无机材料如ZnO、AgO等展现出良好的抗菌、止血等特性,壳聚糖与无机材料协同作用,既可以提高创伤处理效果,也可以提高创伤敷料的力学性能。
目前创伤愈合敷料主要研究方向为促进慢性伤口持续愈合;通过无机抗菌材料,协同促进愈合;针对特殊伤口,如糖尿病足、溃疡性腿和皮肤癌伤口的治疗与促进愈合等,可以充分利用壳聚糖自身的优势,将壳聚糖的应用与创伤愈合研究最新最热研究方向相结合,扩大壳聚糖应用的同时,促进生物医药材料的开发。

