基于程序升温GC的EA-IRMS联机系统在氮、 碳和硫同位素组成测定中的应用
孟宪菁,杨 斌,马 潇,张宏博,徐 波,王 旭,尹 松
(1.赛默飞世尔科技(中国)有限公司,上海 201206;2.中国科学院西双版纳热带植物园,云南 勐仑 666303; 3.内蒙古自治区食品检验检测中心,内蒙古 呼和浩特 010090;4.中海油能源发展股份有限公司,上海 200941; 5.中国科学院地质与地球物理研究所,北京 100029)
近年来,连续流技术的元素分析-稳定同位素比率质谱仪(EA-IRMS)在线联机系统已经在食品[1-3]、农业[4-5]、地质[6-9]和环境[10-11]等领域取得了广泛的应用。基于快速燃烧的原理,EA-IRMS将固态或粘稠态样品中总氮、总碳和总硫转化为气态的N2、CO2和SO2,实现了δ15N、δ13C和δ34S的高精度准确测量[12-18]。以往大多数EA-IRMS是通过70 ℃恒温气相色谱柱(GC)分离N2、CO2和SO2样品,至少需20 min才能完成1次δ15N、δ13C和δ34S分析[17]。较长的分析时间不但增加了测试成本,而且增加了测定结果的不确定性[6,12]。
目前新推出的EA IsoLink元素分析单元在功能设计上新增了程序升温GC和氦气节约模块[18-19]。程序升温GC能够按设定的程序在2 min内升至指定温度(如240 ℃),从而对样品气进行快速脱附。这不仅可以得到更高灵敏度的峰高信号和尖锐的色谱峰形,还可缩短δ15N、δ13C和δ34S的分析时间(约10 min)[18]。氦气节约模块利用从反应管流出的一部分载气返回并吹扫进样口实现节约氦气。另外,分析时间的缩短也间接地降低了载气(氦气)的使用量。程序升温GC结合氦气节约模块可以将EA-IRMS联机系统的氦气节省60%以上[19]。由于氦气资源的紧缺和价格的上涨,该联机系统在经济上具有很大优势。
记忆效应主要是指前一个样品在该联机系统管路中的残留样品会成为下一个样品测定的“背景值”[20],是影响EA-IRMS联机系统对实际样品测定精度和准确度的重要因素[6,21]。研究表明[5,9-10,14],EA-IRMS对δ15N和δ13C的分析通常不存在显著的记忆效应。由于恒温GC条件下,SO2脱附较慢且不完全,柱残留及色谱峰拖尾会导致34S具有一定的记忆效应[6,12]。基于程序升温GC的EA-IRMS在每次样品分析时均对色谱柱进行烘烤,以保持较低的柱残留[18]。然而,有关其对34S记忆效应影响的研究目前尚未见报道。
鉴于程序升温GC的EA-IRMS在测定总氮、总碳和总硫稳定同位素比率上具有一定的优势和应用前景[18],本研究拟综合分析该联机系统的稳定性和样品测量的准确性。如,评价具有程序升温GC的EA-IRMS性能及长期稳定性;探讨该联机系统测定δ34S时硫的记忆效应;揭示不同种类样品的δ15N、δ13C和δ34S特征。希望为EA-IRMS技术的应用与发展提供基础数据和科学依据。
1 实验部分
1.1 仪器与参数
1.1.1主要仪器 EA-IRMS联机系统主要由EA IsoLink元素分析单元、ConFlo Ⅳ连续流接口装置和DELTA V Advantage稳定同位素比率质谱仪3部分组成,均为美国Thermo Fisher Scientific公司产品。
EA IsoLink配有自动进样器,并安装了双反应器:一个是用于氮(N)、碳(C)、硫(S)同位素比率分析的快速燃烧反应器;另一个是用于氢(H)和氧(O)同位素比率分析的高温转化反应器。快速燃烧反应器可安装18 mm外径的反应管进行常规进样量(小于5 mg)样品的分析;也可安装25 mm外径的反应管用于常规进样量甚至大于50 mg样品量(如,元素含量极低样品)的分析[22]。燃烧反应器采用氧化(三氧化钨,WO3)和还原(铜,Cu)一体式设计,将被测样品在高温和过氧环境下瞬间燃烧,然后在Cu还原作用下形成N2、CO2和SO2气体,这些气体经程序升温GC快速分离后进入ConFlo Ⅳ。
ConFlo Ⅳ是具有自动稀释功能的连续流通用接口,采用高纯N2(99.999%)、CO2(99.995%)和SO2(99.990%)作为参比气,并由高纯氦气(99.999%)稀释和运载,通过内置的开口分流器将参比气和样品气引入DELTA V Advantage同位素比率质谱仪中。
DELTA V Advantage是具有3 kV加速电压的气体稳定同位素比率质谱仪。在1.6×10-7kPa超高真空条件下,采用通用三杯接收器同时采集N2气体电离后产生的[14N2]+、[14N15N]+和[15N2]+分子离子束,或CO2气体电离后产生的[12C16O2]+、[13C16O2]+和[12C16O18O]+分子离子束,或SO2气体电离后产生的[32S16O2]+和[34S16O2]+分子离子束,再由不同电阻值的放大器转化为电压信号,完成δ15N、δ13C和δ34S的检测。
1.1.2仪器参数 EA IsoLink载气流速和进样口吹扫流速分别设定为180、70 mL/min,结合氦气节约模块,从反应管分流的载气以130 mL/min返回并吹扫进样口,约2 min后终止该部分气流的吹扫[19]。氧气流速设为175 mL/min,喷氧时间设为3 s,对于一次进样超过1 mg C的样品,喷氧时间设为6 s。燃烧炉温度设为1 020 ℃,由于锡囊燃烧放热,闪燃温度实际上远大于1 020 ℃,可确保样品充分反应[22]。使用程序升温GC,在δ15N和δ13C测定时GC温度保持在55 ℃,而后2 min内升温至240 ℃进行δ34S测定。
进入ConFlo Ⅳ的N2、CO2和SO2样品气被氦气稀释的比例分别设定为0、79%和0。另外,对于一次进样超过1 mg C的样品,CO2样品气被氦气稀释的比例设为96%。同时测定δ15N、δ13C和δ34S时,在样品N2或SO2出峰之前引入N2或SO2参比气,在样品CO2出峰之后引入CO2参比气。识别N2、CO2和SO2的起/止色谱峰斜率分别设为0.2/1、0.2/0.4和0.2/1 mV/s。背景值扣除方法采用Calc Mean BGD,即取出峰之前5 s的背景值(BGD)信号的平均值[20]。
1.2 实验方法
1.2.1EA-IRMS联机系统性能测试 为了检验EA-IRMS联机系统的气密性,分别对该联机系统m/z28、44、64的背景值(BGD)和空白(空锡囊)信号进行10次测定。如无特别说明,本研究EA-IRMS性能测试和样品分析均采用18 mm外径的反应管。
为了评价参比气的稳定性,分别进行了N2、CO2和SO2参比气的“零”富集测试和线性测试。“零”富集测试中,连续引入10次相等峰高信号的参比气脉冲,m/z28、44、64的峰高信号均为3 V。线性测试中,连续引入5~6次不同峰高信号的参比气脉冲,m/z28、44、64的信号递增区间均设为1~9 V。本研究在SO2钢瓶上安装了一个40 ℃恒温减压阀,并将ConFlo Ⅳ内置的SO2参比气减压阀以及IRMS的进气针阀和离子源切换至加热状态,通过降低SO2气体的粘滞性优化色谱峰形。
在2017年5月至9月这4个月的时间内,连续建立了δ15N、δ13C和δ34S的标准曲线,以检验联机系统的长期稳定性。构建曲线的标准物质信息列于表1。使用USGS40、USGS41和USGS42共3个δ15N和δ13C标准物质,以(59±12) μg N和(221±32) μg C常规进样量,于5月4日、7月27日、8月9日、8月30日和9月4日分别建立了5条δ15N标准曲线和5条δ13C标准曲线。使用IAEA-S-1、IAEA-S-2和IAEA-SO-6共3个δ34S标准物质,以(70±32) μg S常规进样量,于5月4日、5月12日和5月19日建立了3条δ34S标准曲线。此外,还建立了小样品量(9±2) μg N、(33±5) μg C和(8±2) μg S标准曲线,用以比较其与常规样品量标准曲线之间的差异性。
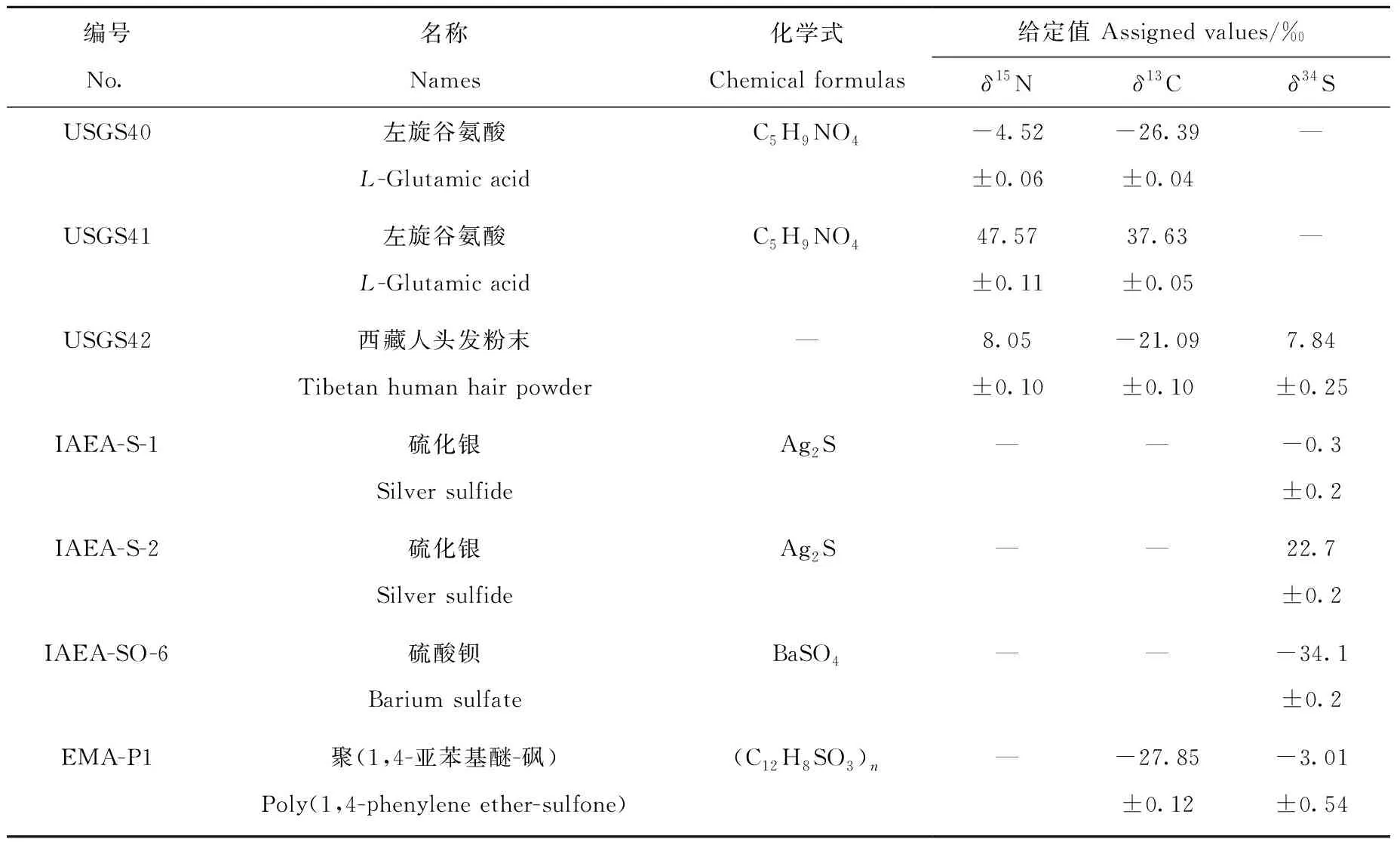
表1 测试标准物质的同位素信息Table 1 Isotopic information of the standards
注:结果采用平均值±1SD/‰表示
1.2.234S记忆效应分析 为了探讨程序升温GC的EA-IRMS联机系统在测定δ34S时硫记忆效应的影响,分别使用18、25 mm反应管测定δ34S相差较大的USGS42、IAEA-SO-6、IAEA-S-1、IAEA-S-2和EMA-P1系列标准物质。每种标物以(50±10) μg S常规进样量,至少重复4次。由于25 mm反应管的SO2样品峰存在一定的延迟和拖尾问题[22],可能导致其分析δ34S时存在记忆效应,本研究通过采用在不同标物间添加空锡囊测定的方法,检验34S记忆效应消除的程度。
1.2.3不同类型样品同位素比率的测定 将烘干的羊肉(包括腹下肌、肱三头肌、背最长肌和肱二头肌)、海参(野生和人工)、金银花、干酪根、木材和琥珀6种样品研磨成粉末,根据N、C、S元素含量分别称取0.6 mg羊肉、海参和金银花,1 mg干酪根,1.5 mg木材, 3 mg琥珀,待测样品用锡囊紧密包裹,每种样品至少重复测定3次。木材样品以及构建δ34S标准曲线的IAEA-SO-6属不易完全燃烧的物质,应与2 mg五氧化二钒(V2O5)一起混入锡囊,由于V2O5的催化作用,即使温度低于1 000 ℃也能充分燃烧[12,23]。实验于2017年5月4日采用程序升温GC的EA-IRMS及其内置热导检测器(TCD),通过一次进样快速完成样品中N、C、S同位素组成及元素含量的测定。样品δ15N和δ13C的测定结果由USGS40、USGS41和USGS42构建的标准曲线进行校正,δ34S由IAEA-S-1、IAEA-S-2和IAEA-SO-6构建的标准曲线进行校正,校正方法参照文献[24]。
2 结果与讨论
2.1 EA-IRMS联机系统稳定性
多次测定表明,EA-IRMS联机系统m/z28、44、64的背景值(BGD)分别小于45、1、20 mV。BGD低信号表明,该联机系统气密性和运行状态良好,受外界环境干扰小[6,10,15-16]。空白(空锡囊)燃烧产生的[14N2]+、[12C16O2]+和[32S16O2]+信号分别小于10、20、15 mV。本研究绝大多数样品信号大于1 V,达到空白信号的50倍以上,因此,可忽略空白对同位素比率测定结果的影响[6]。如果被测样品信号小于1 V,信噪比降低,空白效应则不可忽略,一般采取差减法[15]进行空白校正。
参比气的“零”富集测试表明,δ15N、δ13C和δ34S的测定精度分别为0.018‰、0.033‰和0.038‰,均优于EA-IRMS联机系统出厂技术指标0.06‰的要求[20]。线性测试表明,δ15N、δ13C和δ34S与相应的m/z28、44、64峰高信号之间的线性斜率分别为0.001 3‰/V、0.009 6‰/V和0.059 5‰/V,优于该系统出厂技术指标±0.066‰/V的要求[20]。
不同时间建立的δ15N、δ13C和δ34S标准曲线均具有较好的重现性,示于图1。δ15N和δ13C标准曲线(L1~L5)斜率为0.99~1.01,截距分别为(-1.43±0.07)‰和(-32.38±0.12)‰;δ34S标准曲线(L1~L3)斜率为1.05~1.07,截距为(-2.54±0.13)‰。截距表示参比气的同位素比率[24]均具有良好的重现性。由于SO2目标气中相等质量数的32S18O16O对34S16O2存在干扰,即氧同位素影响硫同位素的测定结果[13],这可能是δ34S标准曲线斜率偏离的重要原因。基于协方差(ANCOVA)和最小显著性差异法(LSD)分析表明,不同时期δ15N、δ13C和δ34S的标准曲线不存在显著差异(p>0.05),即无明显的时间漂移。将USGS42的测定结果(n=41)代入上述任意一条标准曲线中,得到校正后的δ15N和δ13C精度和准确度均优于0.3‰,δ34S精度和准确度均优于0.6‰,能够满足EA-IRMS测试要求[20,22]。这表明,该联机系统每隔1个月只需建立1次标准曲线,以提高样品分析效率。此外,小样品量标准曲线(δ15N和δ13C,L6;δ34S,L4)与常规样品量标准曲线之间存在显著差异(p<0.01)。因此,小样品量样品需要另外建立自身的标准曲线进行校正。
不同时间测定的质控标准δ15N、δ13C和δ34S具有良好的重现性,示于图2。本研究中,δ15N、δ13C和δ34S的测定结果均采用不同时间建立的标准曲线进行实时校正。5个月内重复测定标准物质USGS42的δ15N、δ13C和δ34S,其平均测定值分别为(8.01±0.11)‰、(-21.11±0.13)‰和(7.77±0.23)‰(n=41),分析误差均小于0.1‰。1个月内重复测定IAEA-S-1、IAEA-S-2和IAEA-SO-6三种标准物质的δ34S,其平均测定值分别为(-0.36±0.21)‰(n=14)、(22.56±0.28)‰(n=23)和(-34.14±0.28)‰(n=26),分析误差均小于0.1‰。这些测量结果能够满足氮、碳和硫元素稳定同位素分析精度和准确度的要求[20,22]。
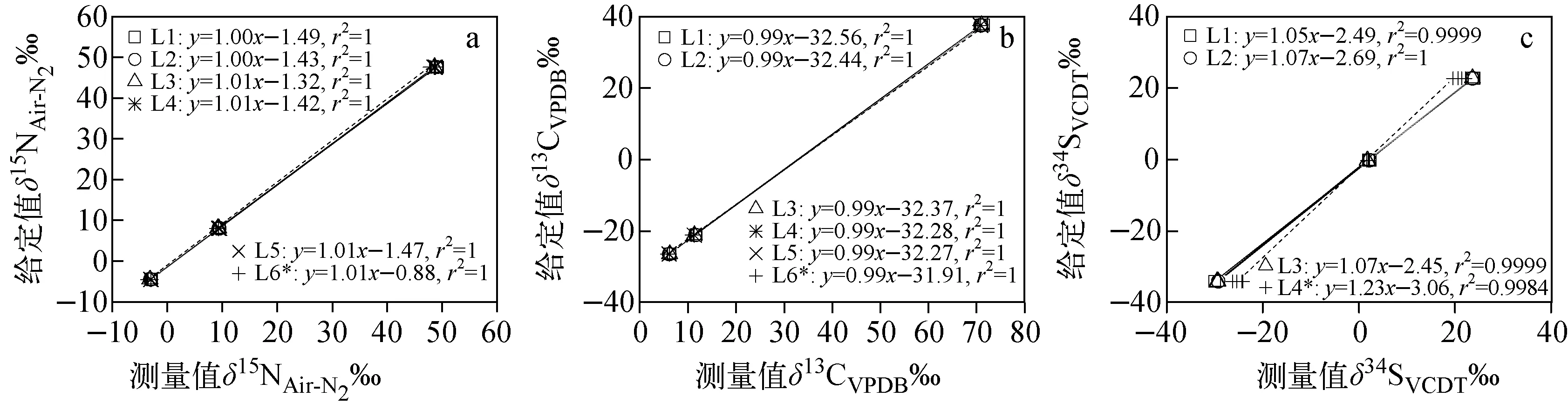
注:*代表小样品量测定结果建立的标准曲线 图1 不同测量时间δ15N(a)、δ13C(b)和δ34S(c)的标准曲线Fig.1 Correction curves of δ15N (a), δ13C (b) and δ34S (c) at different measurement times
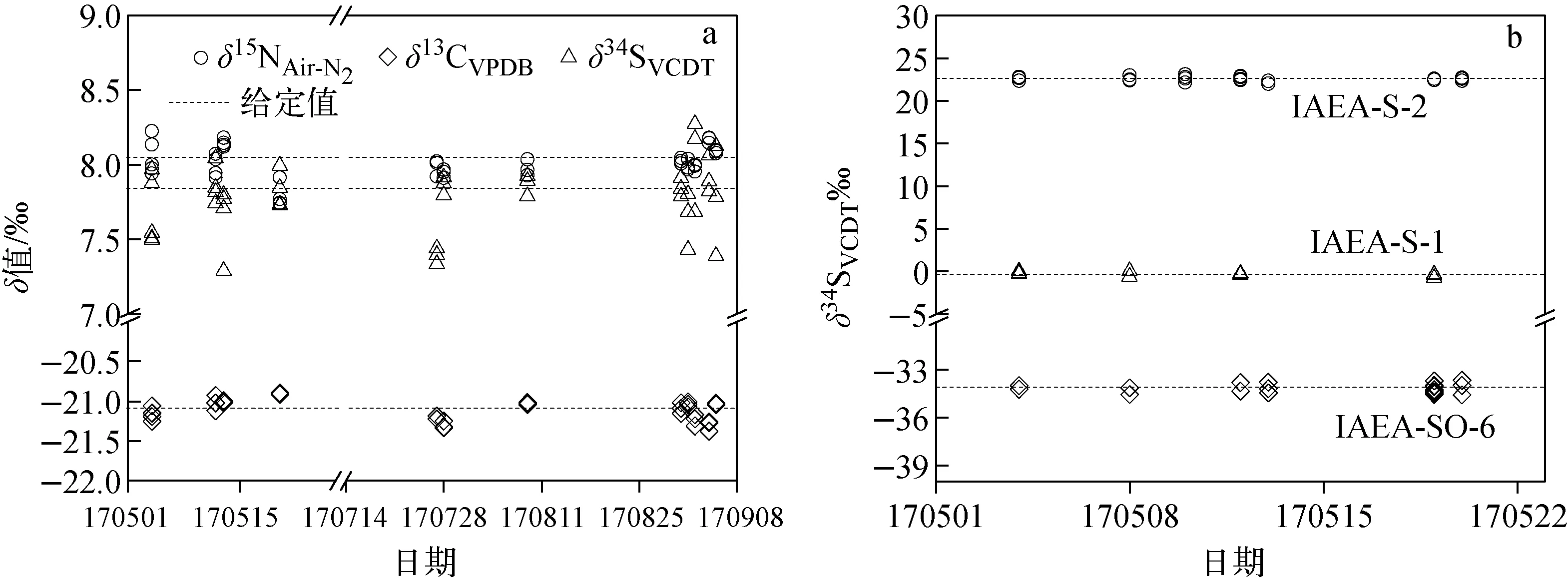
注:a.USGS42;b.无机硫标物 图2 不同测量时间标准物质δ15N、δ13C和δ34S的重现性Fig.2 Reproduction of δ15N, δ13C and δ34S of the standards at different measurement times
2.2 燃烧SO2分析法中34S的记忆效应
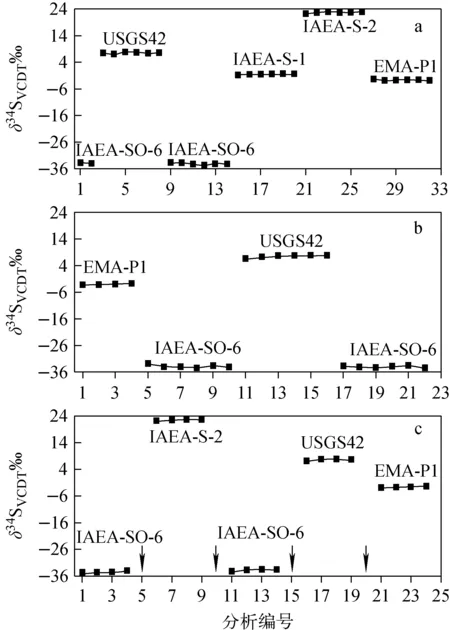
注:↓代表不同标物间添加1个空锡囊 图3 18 mm(a)和25 mm(b, c) 反应管分析δ34S时的记忆效应Fig.3 Memory effects for δ34S measured through the 18 mm (a) and 25 mm (b, c) reactor tubes
由于EA-IRMS联机系统对N2和CO2无显著柱残留及峰拖尾[5,9-10,14],本研究重点探讨了34S的记忆效应,示于图3。结合程序升温GC,每次样品分析时均对色谱柱进行烘烤(240 ℃,4 min),可以保证较低的柱残留[18]。采用18 mm反应管测定δ34S时无显著记忆效应(p>0.05),不同标准物质δ34S的测定精度为0.04‰~0.18‰,示于图3a。虽然18 mm反应管与25 mm反应管测定同一样品δ15N、δ13C和δ34S具有较好的重现性(SD<0.15‰,n=6)和一致性(Δ<0.3‰)[22],但是,采用25 mm反应管测定δ34S时存在一定的记忆效应,δ34S测定精度为0.11‰~0.41‰,示于图3b。这是由于相同条件下,25 mm反应管的SO2样品峰比18 mm反应管略有延迟且拖尾[22]。当采用25 mm反应管测试时,在不同标物间添加1个空锡囊后,记忆效应影响显著减弱,δ34S测定精度达到了0.08‰~0.22‰,示于图3c。
2.3 不同类型样品δ15N、δ13C和δ34S的测试结果
以往的EA-IRMS采用恒温GC分离法,主要用于δ15N和δ13C的分析[4-5,14-16]。但是对于δ15N、δ13C和δ34S同时分析,GC70 ℃恒温条件会导致SO2出峰较晚和拖尾,存在样品分析时间较长以及分析效率较低等问题[6,12,17]。本研究采用程序升温GC的EA-IRMS联机系统对羊肉、海参、金银花、干酪根、木材和琥珀样品中N、C、S元素含量及其同位素组成进行快速测定,结果列于表2。其中,C/N和C/S质量比均小于200的样品,δ15N、δ13C和δ34S测定精度分别为0.1‰、0.05‰和0.12‰。C/N或C/S质量比大于2 000的木材及琥珀类样品,其N2和SO2的信号强度小于0.5 V,此时,δ15N和δ34S测定精度分别优于0.6‰和0.2‰。这表明,该系统测定不同C/N或C/S样品时能够达到研究所需的精度需求[20,22]。进一步分析可知,虽然羊肉不同部位肌肉元素含量差异相差不大(p>0.05),但其δ15N、δ13C和δ34S差异显著(p<0.05),这与文献[1]的研究结果一致。野生海参与人工养殖海参的δ13C存在显著差别(p<0.05),表明二者可能具有不同的食物来源[3]。
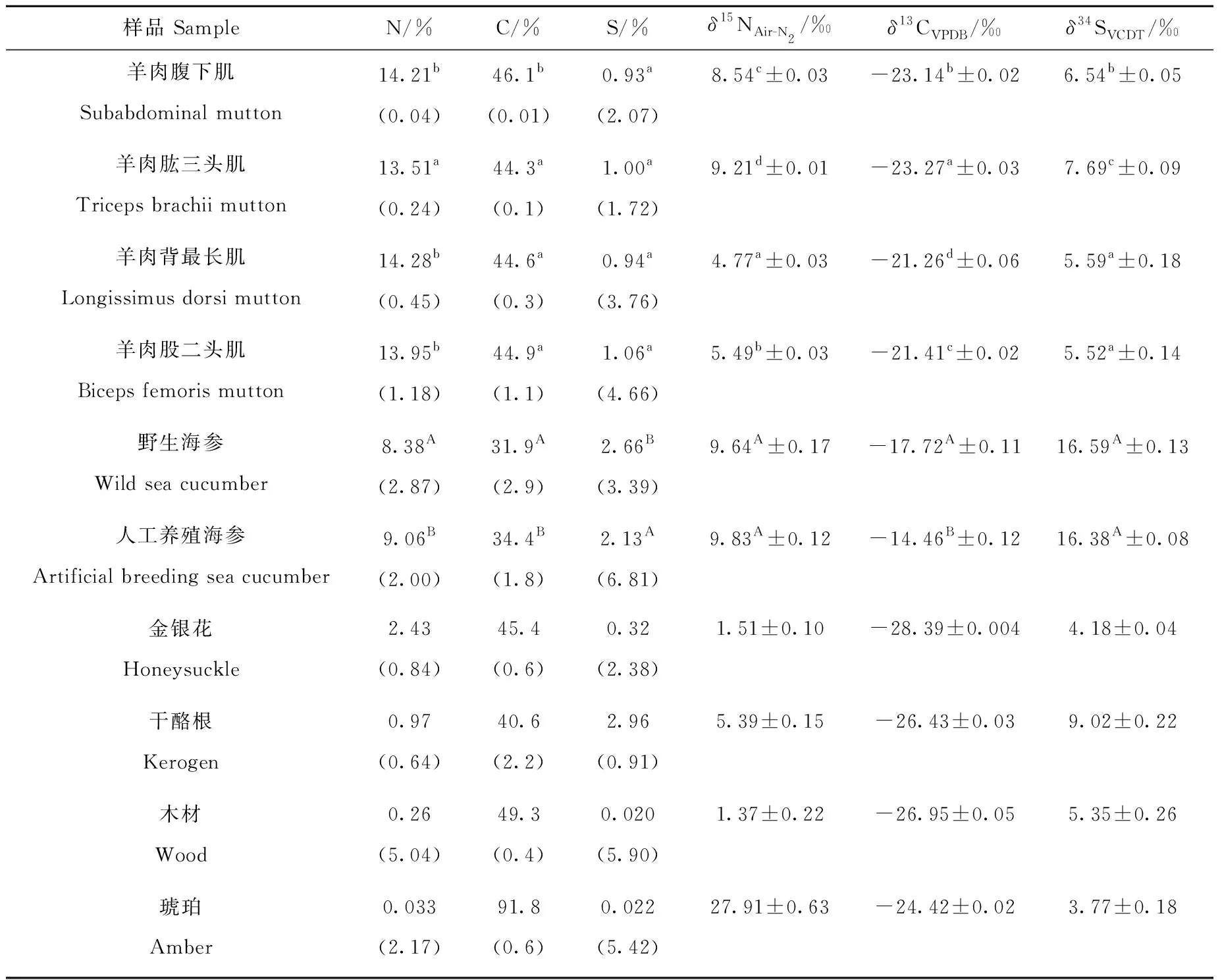
表2 不同类型样品N、C和S同位素组成Table 2 Isotopic composition of different samples
注:元素含量采用平均值(RSD/%)表示,同位素组成采用平均值±1SD/‰表示;每列不同小写(羊肉:abcd)或大写字母(海参:AB)代表差异在p<0.05水平上达到显著
3 结论
本研究采用具有程序升温GC的连续流EA-IRMS联机系统,对δ15N、δ13C和δ34S进行快速(约10 min)测定。结果表明,该联机系统的运行状态良好,m/z28、44、64的背景值都小于50 mV,空白信号都小于20 mV,参比气“零”富集测试和线性测试均优于仪器出厂技术指标0.06‰和±0.066‰/V的要求。δ15N、δ13C和δ34S标准曲线无显著时间漂移,每隔1个月只需建立1次标准曲线。6个月内重复测定δ15N、δ13C和δ34S具有良好的长期稳定性,外精度和准确度分别优于0.3‰和0.1‰。18 mm反应管不存在34S记忆效应,25 mm反应管在添加空锡囊后可将34S记忆效应显著减弱。针对C/N、C/S均小于200的样品,δ15N、δ13C和δ34S的测定精度均优于0.15‰;对于具有极高C/N或C/S的木材及琥珀类样品,δ15N和δ34S测定精度分别优于0.6‰和0.2‰。

