苏丹红Ⅱ纯物质中有机杂质的定性和定量分析
邓 超,张 伟,黄 挺,张 辉,何雅娟,陶 红,全 灿,李红梅
(1.浙江省计量科学研究院,浙江 杭州 310018; 2.中国计量科学研究院化学计量与分析科学研究所,北京 100029)
苏丹红Ⅱ作为苏丹红Ⅰ的衍生物,是一种偶氮化合物类合成色素[1],主要用于纺织品、橡胶、塑料、油漆等工业产品的着色[2]。由于其含有芳香族结构,进入人体后会分解还原成芳香胺,芳香胺化合物再次被人体吸收[3],对人体健康具有潜在的致癌性[4]。中国和欧盟均禁止将苏丹红色素作为食品添加剂使用[5-6],但因其成本低[7]、着色性好,仍被很多商家非法使用[8]。因此,食品中苏丹红色素的检测极为重要[5,9]。
纯度标准物质是溶液和基体标准物质制备的基础,是基体中目标物准确测量的溯源源头[10]。若纯物质的纯度或其中的杂质得不到准确定值,将会对整个国家化学成分测量的量值传递和测量结果产生极其严重的影响,因此,实现纯物质中杂质的准确定性和定量一直是分析测试领域急需攻克的难题[11]。苏丹红纯度标准物质的研制有利于提高检测水平与检测准确度,提高食品质量,有利于保护人民的身体健康,具有广泛的社会效益和一定的经济效益。但目前国内尚无苏丹红Ⅱ纯度标准物质,也无苏丹红Ⅱ中存在的有机杂质的报道。
本实验拟采用高效液相色谱-电喷雾-离子阱-飞行时间高分辨质谱(HPLC-ESI-IT-TOF MS)法,通过优化液相色谱分离及质谱检测条件,对苏丹红Ⅱ中主要的有机杂质进行分析鉴定,并利用液相色谱外标法准确定量,希望为苏丹红Ⅱ一级标准物质的研制提供参考。
1 实验部分
1.1 主要仪器与试剂
高效液相色谱-离子阱-飞行时间/串联质谱仪(配有ESI源)、LC-20AD液相色谱仪:均为日本Shimadzu公司产品;6410QQQ液相色谱-三重四极杆质谱仪、1200型高效液相色谱仪(配有二极管阵列(DAD)检测器):美国Agilent公司产品;XP205型称量天平(0.01 mg):瑞士梅特勒-托利多公司产品;Inertsil ODS-SP液相色谱柱(250 mm×4.6 mm×5 μm):日本GL Science公司产品。
苏丹红Ⅱ标准物质候选物原料:美国Sigma公司产品,经柱层析方法提纯后使用,经液相色谱比较确认无新杂质引入;苏丹红Ⅰ(GB W10056,99.9%):由国家标准物质研究中心提供;溶剂橙2:日本TCI公司产品;乙腈(色谱纯):德国Merck公司产品;甲酸(LC/MS级):美国Thermo公司产品;流动相用水为二次去离子水。
1.2 样品溶液和标准溶液的配制
待测样品溶液和标准溶液均采用质量法配制,以乙腈为溶剂,所有样品及标准储备溶液均于4 ℃下密封保存。
1.3 分析方法及实验条件
1.3.1有机杂质定性分析 采用HPLC-IT-TOF MS法和HPLC-MS/MS法对主成分中的有机杂质进行定性分析,借助质谱仪的高分辨率和精确质量数优势,由杂质化合物各级质谱碎片的测量值、化学式和理论值,推测杂质的分子式和结构。
1) HPLC-IT-TOF MS实验条件
液相色谱条件:Inertsil ODS-SP液相色谱柱(250 mm×4.6 mm×5 μm);流动相为0.1%甲酸水溶液-乙腈(25∶75,V/V);流速0.6 mL/min;柱温35 ℃;检测波长范围190~600 nm;进样量10 μL。
质谱条件:ESI离子源,正离子模式;质量扫描范围m/z100~600;离子源温度200 ℃;曲型脱溶剂管(CDL)温度200 ℃;雾化气(N2)流速1.5 L/min;碰撞能量为MS150%,MS270%;离子分离时间50 ms;碰撞气及冷却气为高纯氩气。
2) HPLC-MS/MS实验条件
液相色谱条件:流速0.5 mL/min,进样量20 μL,其他同HPLC-IT-TOF MS色谱条件。
质谱条件:ESI离子源;全扫描模式和子离子监测模式,正离子扫描监测;出口电压135 V,杂质1~4和苏丹红Ⅱ的碰撞能依次为16、15、10、10、10 eV;干燥气流速8 L/min;干燥气温度350 ℃;雾化气压力3.45×105Pa;碰撞气为高纯氮气。
1.3.2杂质纯品纯度定值HPLC条件 杂质纯品作为对杂质定量的标准品,实验前需确定准确纯度。溶剂橙2因无相应的标准物质,故其标准品经液相色谱面积归一化法确定其准确纯度。对配制的6份溶剂橙2样品溶液进行液相色谱检测,积分得到其有机纯度值。
液相色谱条件:Inertsil ODS-SP 液相色谱柱(250 mm×4.6 mm×5 μm);流动相为纯水-乙腈(30∶70,V/V);流速1 mL/min;检测波长范围190~400 nm;进样量10 μL。
1.3.3有机杂质定量分析 采用液相色谱HPLC外标曲线法对苏丹红Ⅱ纯品中已确定的有机杂质进行定量分析。绘制苏丹红Ⅰ杂质标准曲线(0.01~2 mg/L)和溶剂橙2杂质标准曲线(0.19~4.652 mg/L),配制6份苏丹红Ⅱ溶液,分别进行HPLC检测,HPLC实验条件同HPLC-IT-TOF MS中的液相色谱条件。
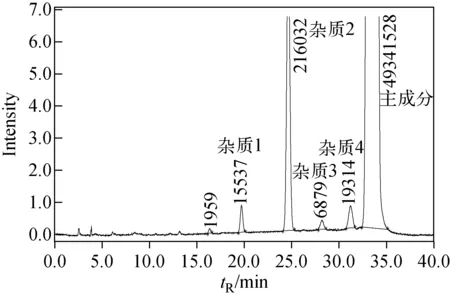
图1 苏丹红Ⅱ纯品中主成分和 杂质分离的色谱图Fig.1 Chromatogram of main component and impurities in Sudan Ⅱ
2 结果与讨论
2.1 苏丹红Ⅱ纯品中有机杂质的定性
通过选择合适的色谱柱对液相色谱流动相的组成、流速等条件进行优化,得到了分离苏丹红Ⅱ及杂质的最佳实验条件,见1.3.1节。苏丹红Ⅱ主成分及其杂质成分的色谱图和总离子流图分别示于图1和图2。
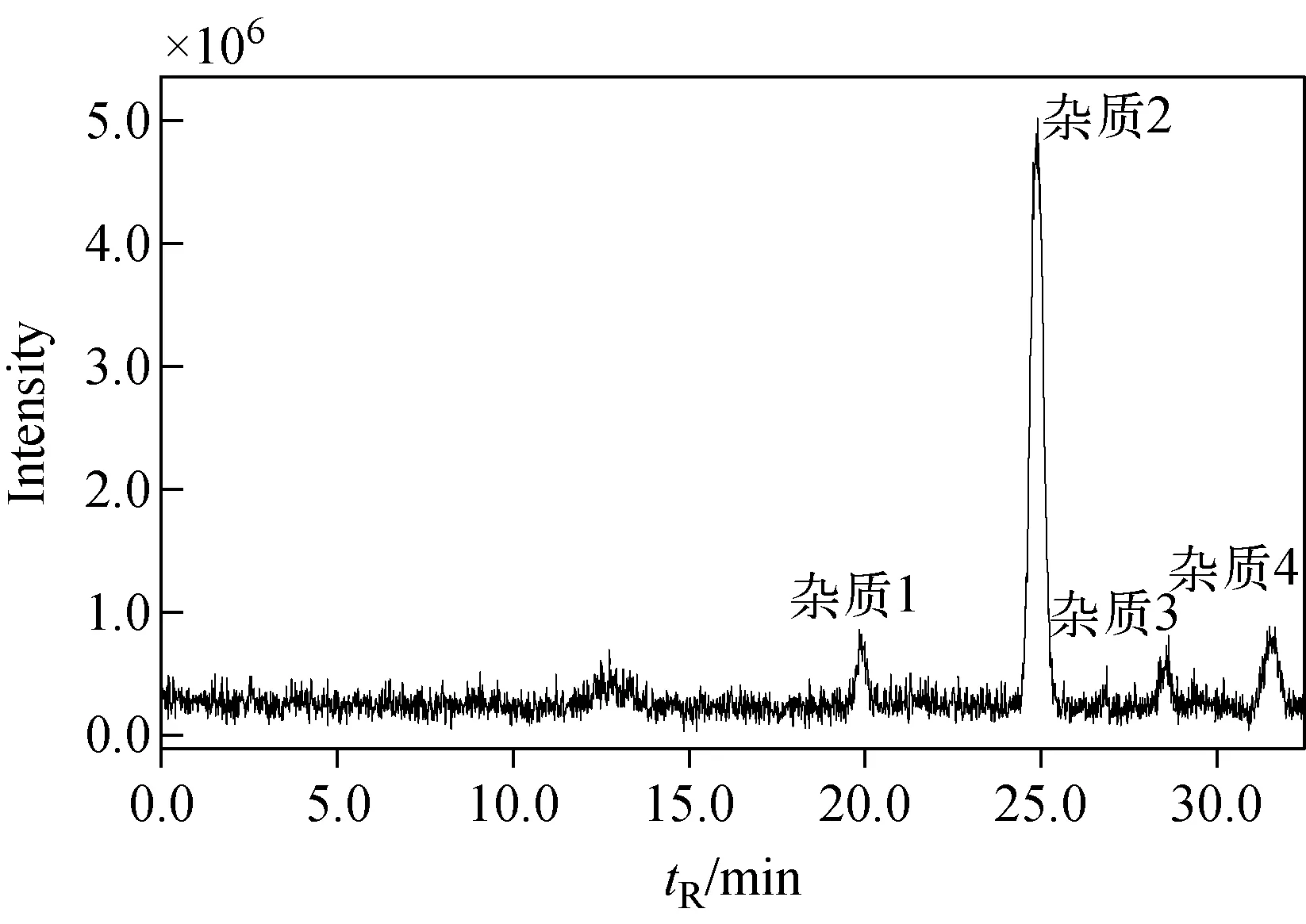
注:为了防止高浓度的主成分苏丹红Ⅱ进入 质谱仪而造成污染,且已无其他杂质出现, 32.5 min后管路自动切至废液中,不进入质谱仪扫描 图2 苏丹红Ⅱ纯品中杂质分离的总离子流图Fig.2 TIC of impurities in Sudan Ⅱ
分析图1中色谱归一化结果,只有杂质2的含量大于千分之一。通过HPLC-IT-TOF MS获得的苏丹红Ⅱ和4种杂质的母离子、子离子的精确分子质量列于表1。由于杂质含量较低,通过HPLC-IT-TOF MS获得的子离子数目较少,因此,采用HPLC-MS/MS法对苏丹红Ⅱ及其4种杂质进行二级质谱裂解,结果示于图3和图4。通过质谱裂解途径解析,预测未知杂质的分子式,并采用相应杂质的纯品进行验证。

表1 苏丹红Ⅱ及其杂质的母离子和子离子参数Table 1 Parent ions and product ions of Sudan Ⅱ and the impurities

图3 苏丹红Ⅱ的碎片离子峰及质谱裂解途径Fig.3 Fragment ions and fragmentation pathways of Sudan Ⅱ
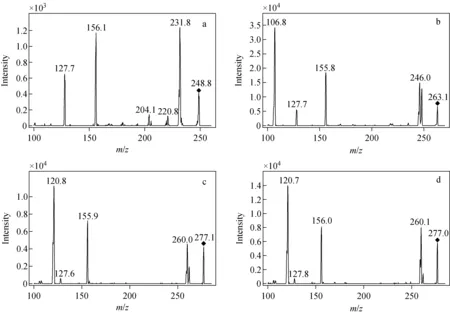
图4 杂质1(a)、2(b)、3(c)、4(d)的碎片离子峰Fig.4 Fragment ions of impurities 1 (a), 2 (b), 3 (c), 4 (d)
由图3和图4可知,杂质1、2和苏丹红Ⅱ均有m/z156碎片峰,因此可通过苏丹红Ⅱ的已知结构对杂质1和2的结构式进行推导。杂质1的分子离子峰[M+H]+为m/z249,比苏丹红Ⅱ的分子离子峰[M+H]+m/z277少28(即2个—CH2),杂质1的可能结构式示于图5a,可能的质谱裂解途径示于图6a。杂质2的分子离子峰m/z263,与苏丹红Ⅱ的分子离子峰m/z277相差14(—CH2),结合苏丹红Ⅱ的结构式推导出杂质2可能的结构式示于图5b和5c,根据这两种结构式查找相关化合物,发现b并无CAS号,即可暂认定杂质2的可能结构式为c。推测其可能的质谱裂解途径示于图6b。

图5 杂质1(a)和2(b、c)的可能结构式Fig.5 Possible structures of impurities 1 (a) and 2 (b, c)

图6 杂质1(a)和2(b)的质谱裂解途径Fig.6 Fragmentation pathways of impurities 1 (a) and 2 (b)
结合文献[12]、结构式分析和质谱裂解规律,初步推测杂质1为苏丹红Ⅰ,杂质2为溶剂橙2。
采用HPLC-IT-TOF MS法对苏丹红Ⅰ和溶剂橙2的纯品进行一级、二级碎片分析,得到的精确分子质量和碎片离子质荷比结果列于表2。
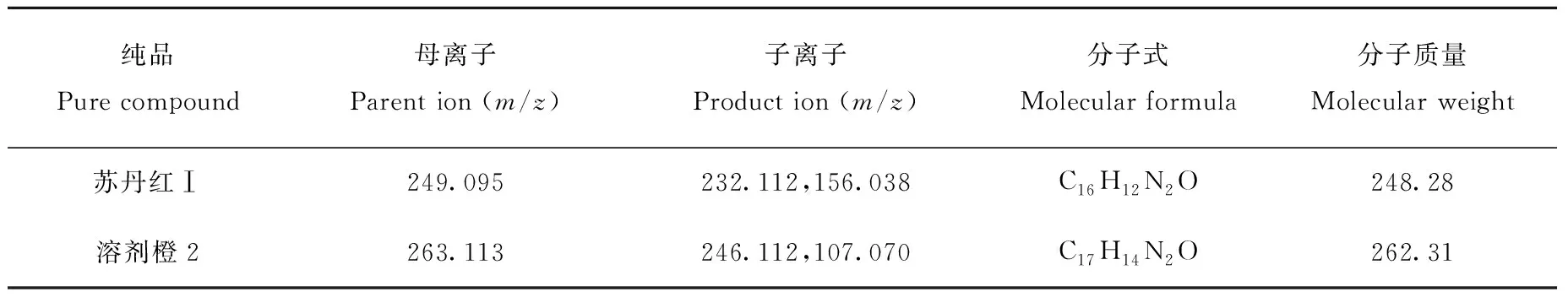
表2 苏丹红Ⅰ和溶剂橙2的母离子和子离子参数Table 2 Parent ions and product ions of Sudan Ⅰand Solvent Orange 2
向苏丹红Ⅱ样品中分别加入苏丹红Ⅰ和溶剂橙2进行HPLC测试,结果示于图7。可知,杂质1和2的峰高明显增加,保留时间完全一致,从而可以确定杂质1和杂质2分别为苏丹红Ⅰ和溶剂橙2。
通过比较苏丹红Ⅱ样品中杂质及纯品的保留时间、分子质量及碎片信息,发现杂质1与杂质2分别与苏丹红Ⅰ、溶剂橙2完全一致。因此,最终确认杂质1为苏丹红Ⅰ,杂质2为溶剂橙2。
杂质3和4的准分子离子峰均为m/z277,且裂解方式符合苏丹红Ⅱ的碎裂特征,推测是苏丹红Ⅱ的同分异构体,即分子式均为C18H16N2O,可能的结构式示于图8。由于市场上没有该物质的纯品,所以无法对该推测结果进行验证。
2.2 杂质纯品纯度定值
杂质苏丹红Ⅰ采用一级标准物质GB W10056,纯度标准值为99.9%。
溶剂橙2的液相色谱面积归一法结果列于表3,溶剂橙2的纯度为99.13%,6次测量得到的相对标准偏差为0.042%。

图7 添加苏丹红Ⅰ前(a)、后(c)和溶剂橙2前(b)、后(d)的苏丹红Ⅱ样品的色谱图Fig.7 Chromatograms of Sudan Ⅱ samples before (a, b) and after (c, d) adding Sudan Ⅰ and Solvent Orange 2

图8 杂质3(a)和4(b)的可能结构式Fig.8 Possible chemical structures of impurities 3 (a) and 4 (b)

样品 Sample纯度 Purity/%199.21299.10399.11499.11599.12699.20平均值99.13相对标准偏差/%0.042
2.3 苏丹红Ⅱ纯品中主要有机杂质的定量
对杂质1和2定性后,选取相应纯品,采用外标工作曲线法对其进行定量测定。由于杂质3和4没有相应纯品,且其是苏丹红Ⅱ的同分异构体,所以采用与主成分苏丹红Ⅱ响应因子一致的方法对这2种杂质进行定量分析[11, 13]。
苏丹红Ⅰ的线性回归方程为y=81.574x-0.288 6,相关系数R2=1。溶剂橙2的线性回归方程为y=83.417x-0.655 4,相关系数R2=1。6份苏丹红Ⅱ样品中杂质1~4的测量结果列于表4。
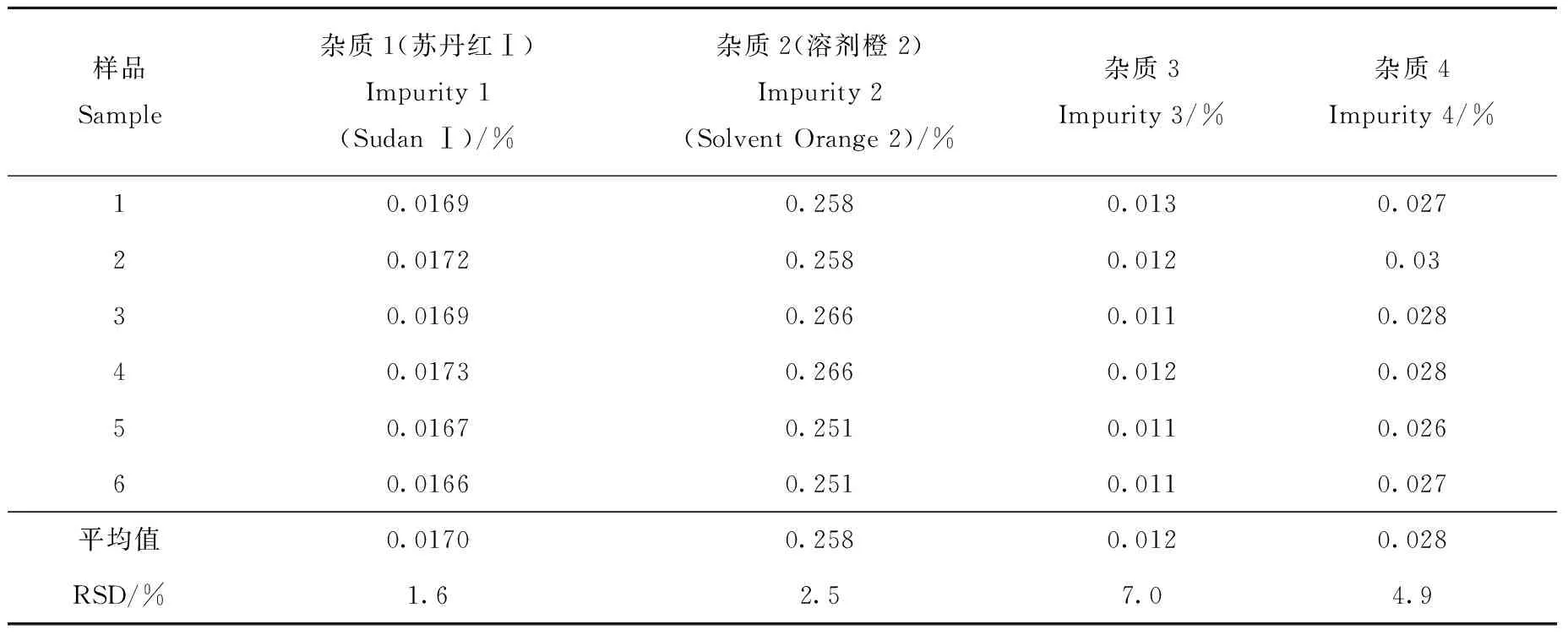
表4 苏丹红Ⅱ中主要有机杂质的含量测定结果Table 4 Contents of main organic impurities in Sudan Ⅱ
3 结论
本实验采用HPLC-IT-TOF MS法和LC-MS/MS法对苏丹红Ⅱ中的有机杂质进行定性分析,采用HPLC外标法对已定性杂质进行定量分析,得到杂质苏丹红Ⅰ和溶剂橙2的含量分别为0.017%、0.258%,相对标准偏差分别为1.6%、2.5%。对未完全定性的杂质3和4采用与主成分苏丹红Ⅱ响应因子一致的方法进行定量分析,其含量分别为0.012%、0.028%,相对标准偏差分别为7.0%、4.9%。该实验可为苏丹红Ⅱ一级标准物质的研制奠定基础,对食品检验等领域中苏丹红Ⅱ的准确测定具有重要意义。

