金属及其化合物考查形式探究
宋 燕
(江苏省启东市第一中学 226200)
金属元素是高中化学的重要内容,有些活泼金属的化学性质活泼,容易与其他物质反应,其化合物的种类繁多,不可能掌握所有金属化合物的性质,因此学习这部分知识除了必要的记忆部分,还需要掌握一定的方法技巧.
一、常见金属化合物溶液配制
溶液的配制是高中化学的重要内容,含有金属元素化合物的溶液称为金属化合物溶液.常见金属化合物溶液的配制主要有Fe(OH)3胶体和Al(OH)3胶体的配制,要注意的是Al(OH)3是两性氢氧化物,能溶于强碱溶液,不溶于弱碱溶液.
例1 (2015 江苏)下列设计的实验方案能达到实验目的的是( ).
A.制备Al(OH)3悬浊液:向1mol·L-1AlCl3溶液中加过量的6mol·L-1NaOH溶液
B.提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和碳酸钠溶液,振荡后静置分液,并除去有机相的水
C.检验溶液中是否含有Fe3+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象
D.探索催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2 mL 5% H2O2和1 mL H2O,向另一支试管中加入2mL 5% H2O2和1 mL FeCl3溶液观察并比较实验现象
解析A项中AlCl3与NaOH反应生成Al(OH)3,而NaOH溶液过量,生成的Al(OH)3会继续与NaOH反应,生成偏铝酸钠,不能制备Al(OH)3悬浊液,A项错误.B项要除去乙酸乙酯中的乙酸,碳酸钠的酸性比乙酸弱,因此饱和碳酸钠可以出去乙酸,还能降低乙酸乙酯的溶解度,式乙酸乙酯析出,静置分液后,就得到纯净的乙酸乙酯,B项正确.C项就加入的新制氯水具有强氧化性,会将Fe2+氧化为Fe3+,这样用KSCN溶液检测出的Fe3+不能确定是原溶液中的,因此C项错误.D项两试管作对照,除了催化剂外其他因素都相同,这样若第二支试管的气泡多于第一支试管,就说明FeCl3是反应的催化剂,可以加快反应速率,D项正确.综上,正确答案为BD.
点评对于常见金属化合物溶液的配制,学生不仅要掌握书本中的常见方法,对于题中给出的用指定物质配制金属化合物溶液的方法也要会分析,类比自己已掌握的方法,判断正误,溶液的配制方法往往不止一种.
二、考查离子方程式
金属元素在化合物中常常是以金属阳离子的形式存在的,因此高考中常以离子方程式的方式考查金属及其化合物知识.在书写离子方程式时,反应物的配比不同,离子方程式就可能不一样,比如Al和NaOH的反应.
例2 (2013 江苏)下列表示对应化学反应的离子方程式正确的是( ).
A.MnO2与浓盐酸反应制Cl2
B.明矾溶于水产生Al(OH)3胶体

C.Na2O2溶于水产生O2

D.Ca(HCO3)2溶液与少量NaOH溶液反应
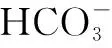
点评本题难度不大,重在对基础知识的考查,需要学生注意题目中的细节.离子方程式的书写中,离子方程式的配平、反应条件、沉淀和气体符号、离子和化合物的书写都是学生容易出错的地方,也是经常设置考点的地方.
三、金属元素化合物的分离和提纯
物质的分离和提纯是高考中常出现的题型,金属元素化合物的分离和提纯同样需要学生大量的知识积累.金属元素及其化合物的分离是要将混合物分离,得到几种纯净物,最终需要将物质还原为原来的状态.而除杂只需将杂质去除即可.
例3 (2016 上海)下列除去杂质的方法正确的是( ).
A.除去N2中的O2:通过灼热的CuO粉末,收集气体
B.除去Cl2中的少量HCl:通过饱和NaHCO3溶液,收集气体
C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后过滤
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液过滤

点评本题考查物质的除杂,均是利用化学性质来除杂,找出一种与杂质反应而不与原物质反应的试剂.要注意不能在除去旧杂质后引入新的杂质,拿捏不准时可以写出化学方程式,确保没有新的杂质生成.
学生在学习金属及其化合物部分的知识时,要学会举一反三,例如三价铁离子是黄色,二价铁离子是浅绿色,则可以根据铁离子在化合物中的价态来判断溶液的颜色.对知识方法多加归纳总结,会有事半功倍的效果.

