分子靶向药物治疗转移性肾细胞癌的疗效及对患者生活质量的影响
陈卫东,刘怀民,张凤仙,马科
商丘市第四人民医院1肾内科,3肿瘤科,河南 商丘476005
2河南省肿瘤医院中西医结合科,郑州4500520
肾细胞癌(renal cell carcinoma,RCC)是泌尿系统常见的恶性肿瘤之一,早期发现可采用外科手术治疗。然而,部分患者初诊时已发生转移或在根治术后出现局部复发或转移,即转移性肾癌(metastatic renal cell carcinoma,mRCC)。mRCC对常规放化疗不敏感,目前多以靶向治疗和免疫治疗为主[1-5]。作为多靶点酪氨酸激酶抑制剂,舒尼替尼具有抗血管生成和抗肿瘤增殖的双重作用,并被推荐为mRCC的一线治疗药物[6-9]。然而,有关舒尼替尼对mRCC患者生活质量的影响及不同转移部位的疗效是否存在区别的报道较少见。本研究回顾性分析75例mRCC患者的临床资料,旨在探讨舒尼替尼治疗mRCC的疗效及对患者生活质量的影响,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2012年1月至2017年6月商丘市第四人民医院收治的75例mRCC患者的临床资料。纳入标准:①经组织学和(或)细胞学检查证实为mRCC;②无骨髓、心、肝、肾等功能严重受损;③生存时间﹥6个月,KPS评分﹥60分;④至少有一处可测量病灶;⑤既往未接受过抗肿瘤治疗。排除标准:①出现肿瘤脑转移者;②缺乏影像学可测量肿瘤组织者;③过敏体质者;④凝血功能、甲状腺功能异常者;⑤接受其他抗肿瘤治疗者;⑥依从性差者。根据治疗方式的不同将患者分为对照组(n=32)和观察组(n=43)。对照组患者接受白细胞介素-2(interleukin-2,IL-2)和重组人干扰素α-2b(recombinant human interferon α-2b,IFNα-2b)治疗,观察组患者接受舒尼替尼治疗。对照组中,男22例,女10例;年龄(63.4±6.8)岁;病理类型:透明细胞癌27例,乳头状细胞癌2例,肉瘤样肾细胞癌、混合细胞癌和集合管癌各1例;转移部位:局部复发或淋巴结转移19例,肺转移13例,软组织转移7例,肝转移4例,骨转移2例。观察组中,男30例,女13例;年龄(64.0±6.2)岁;病理类型:透明细胞癌35例,乳头状细胞癌4例,肉瘤样肾细胞癌和混合细胞癌各2例;转移部位:局部复发或淋巴结转移25例,肺转移16例,软组织转移10例,肝转移4例,骨转移3例,脑转移1例。两组患者的性别、年龄、病理类型及转移部位比较,差异均无统计学意义(P﹥ 0.05),具有可比性。
1.2 治疗方法
对照组患者接受IL-2和IFNα-2b治疗,皮下注射IL-2,每次60~100万IU/m2,每天1次,每周3次;肌内注射IFNα-2b,600万IU/d,每天1次,每周3次。IL-2和IFNα-2b交替应用。如不良反应难以耐受,IFNα-2b可减半,如仍难以耐受,可以停用。观察组患者口服苹果酸舒尼替尼,起始剂量为每次50 mg,每天1次,持续用药4周,休息2周,循环用药(4/2方案);不能耐受者予以2/1方案,即予舒尼替尼胶囊50 mg,用药2周,休息1周,循环用药。直至患者出现无法耐受的药物不良反应或疾病进展而停药。每6周评价一次安全性,完成12周的治疗方可评价疗效。
1.3 疗效评价
依据WHO实体瘤疗效评价标准[10]进行疗效评价:完全缓解(complete response,CR),所有可见病变完全消失并至少维持4周;部分缓解(partial response,PR),肿瘤病灶的最大径及其最大垂直径的乘积减少﹥50%,维持4周以上;疾病稳定(stable disease,SD),介于PR和疾病进展(progressive disease,PD)之间;PD,肿瘤病灶两径乘积增大﹥25%,或出现新病灶。客观缓解率(objective response rate,ORR)=(CR+PR)例数/总例数×100%,疾病控制率(disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%。
1.4 生活质量评价
生活质量评价依据欧洲癌症研究与治疗组织的生活质量核心问卷(EORTC QLQ-C30)。该问卷包括1个总体健康状况、5个功能领域、3个主要症状、含5个反映症状和1个反映经济状况的单项。总体健康状况及功能领域分值越高,表明功能状况越好;主要症状及单项分值越高,表明症状越重。
1.5 不良反应评价
观察并记录用药过程中的不良反应,依据美国国家癌症研究所(National Cancer Institute,NCI)制定的CTCAE3.0评价标准[11]进行不良反应的评价。
1.6 统计学方法
采用SPSS 20.0软件对数据进行统计分析。计量资料以均数±标准差(±s)表示,组内比较采用配对t检验,组间比较采用独立样本t检验;计数资料以率(%)表示,组间比较采用χ2检验或Fisher确切概率法。以P﹤0.05为差异有统计学意义。
2 结果
2.1 近期疗效的比较
所有患者均完成12周以上的治疗,可以评价疗效。观察组和对照组患者的ORR分别为13.95%(6/43)和 6.25%(2/32),差异无统计学意义(χ2=0.477,P=0.490);观察组患者的DCR为76.74%(33/43),高于对照组的53.12%(17/32),差异有统计学意义(χ2=4.606,P=0.032)。(表1)

表1 两组患者的近期疗效
2.2 不同转移部位mRCC患者的近期疗效
对照组和观察组中,分别有19例和25例患者发生局部复发或淋巴结转移,其ORR分别为5.26%(1/19)和12.00%(3/25),DCR分别为52.63%(10/19)和56.00%(14/25),差异均无统计学意义(P﹥0.05)。对照组和观察组中,分别有13例和16例患者发生肺转移,其ORR分别为0(0/13)和6.25%(1/16),DCR分别为30.77%(4/13)和68.75%(11/16),差异均无统计学意义(P﹥0.05)。对照组和观察组中,分别有7例和10例患者发生软组织转移,其ORR 分别为 14.29%(1/7)和20.00%(2/10),DCR分别为57.14%(4/7)和80.00%(8/10),差异均无统计学意义(P﹥0.05)。对照组和观察组中,均有4例患者发生肝转移,治疗后均为PD。对照组2例患者发生骨转移,治疗后均为PD;观察组中3例患者发生骨转移,治疗后均为PD。对照组患者中无脑转移;观察组中1例患者发生脑转移,治疗后为PD。
2.3 生活质量的比较
治疗前,两组患者在功能领域、主要症状、单项及总体健康状况方面的评分比较,差异均无统计学意义(P﹥0.05)。治疗后,两组患者的生活质量均有不同程度的下降,表现为躯体功能评分降低,疲劳、恶心呕吐、食欲降低、便秘、腹泻评分升高,总体健康状况评分下降,与治疗前比较,差异均有统计学意义(P﹤0.05)。治疗后两组患者的各项生活质量评分比较,差异均无统计学意义(P﹥0.05)。(表2)
表2 两组患者EORTCQ LQ-C30评分的比较(±s)

表2 两组患者EORTCQ LQ-C30评分的比较(±s)
注:*与本组治疗前比较,P<0.05
主要症状疲劳恶心呕吐疼痛单项呼吸困难睡眠障碍食欲降低便秘腹泻经济困难总体健康状况观察组(n=43)治疗前 治疗后44.7±5.5 40.2±8.3 49.3±4.7 55.6±7.8 61.8±8.9 39.8±4.0*40.4±5.5 49.7±5.1 54.6±4.3 60.3±6.9 53.1±6.1 33.8±3.1 32.4±2.4 67.0±4.4*38.1±2.5*32.2±2.8 52.7±5.4 33.9±4.0 32.3±3.2 60.0±7.1*36.5±4.2*31.0±3.9 26.6±3.4 30.4±5.6 41.5±4.1 27.7±5.0 28.7±2.5 42.1±3.7 56.7±4.2 27.1±3.4 30.1±4.4 50.5±3.7*33.4±4.4*35.4±4.8*41.2±2.5 51.6±3.1*26.0±3.3 30.7±3.8 42.3±6.0 27.9±7.3 28.3±3.0 42.7±4.9 56.3±5.6 26.3±4.7 30.5±3.6 47.8±5.9*32.3±4.3*34.1±2.6*41.6±5.3 52.6±3.8*
2.4 不良反应发生率的比较
观察组患者发热、肝功能异常和疲劳的发生率均低于对照组,皮肤黏膜反应、高血压和甲状腺功能减退的发生率均高于对照组,差异均有统计学意义(P﹤0.05)。通过对症治疗后,不良反应均得到控制,患者可耐受。(表3)
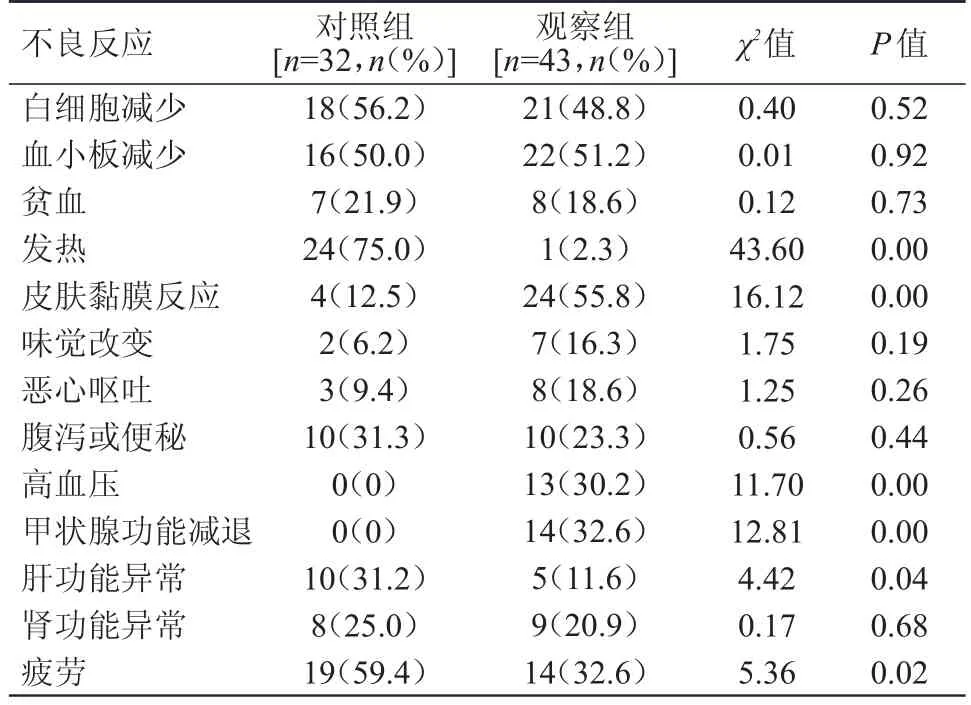
表3 两组患者不良反应发生率的比较
3 讨论
von Hippel-lindau(VHL)基因失活(包括突变、甲基化或杂合性丢失)以及血管内皮生长因子(vascular endothelial growth factor,VEGF)、血小板衍生生长因子(platelet derived growth factor,PDGF)、转化生长因子(transforming growth factor,TGF)高表达是mRCC发病的重要机制之一,作用于上述靶点的药物可对mRCC发挥较好的治疗作用。舒尼替尼可作用于VEGF、PDGF、干细胞因子受体(stem cell factor receptor,SCFR)、集落刺激因子-1(colony stimulating factor-1,CSF-1)受体等多种酪氨酸激酶受体,可直接抑制肿瘤血管生成及肿瘤转移,从而一线作用于mRCC[6-9]。生活质量是全面评价生活优劣的概念,也是评价药物疗效的重要指标之一。国外文献中仅检索到1篇采用EORTC QLQ-C30量表和肾癌症状指数(functional assessment of cancer therapy-kidney symptom index-15,FKSI-15)量表评价药物治疗后mRCC患者生活质量的报道[12];国内也仅有1篇以Karnofsky评分(即KPS评分)为指标评价舒尼替尼对mRCC患者生活质量影响的研究[13],但KPS评分仅从体力状况方面进行评价,不能全面反映药物的影响。因此,本研究采用了具有肿瘤专属性的EORTC QLQ-C30量表[14-16]进行评价。同时,研究中还比较了不同肿瘤转移部位疗效间的差异。
本研究结果显示,采用舒尼替尼治疗的观察组患者的DCR较接受免疫治疗的对照组高(76.74%vs53.12%,P﹤0.05),表明舒尼替尼疗效更好,与汪峰等[17]报道的结果一致。宋继文等[18]研究发现,舒尼替尼一线治疗转移性肾癌时,对不同器官组织转移灶的有效性存在差异,缓解病例多为局部复发及肺转移病灶,进展病例为骨、肝、脑转移病灶,并推测肺转移和软组织转移等实体病灶的生长更依赖微血管形成,因此对舒尼替尼更为敏感。然而,本研究结果显示,舒尼替尼对不同器官组织转移灶的有效性虽有差别,但差异无统计学意义(P﹥0.05),是否与样本量过少有关,仍有待继续研究。张华峰等[19]报道,舒尼替尼对肝转移患者的总有效率为60.0%,远高于本研究,可能与两个研究纳入的肝转移患者数量均较少有关(张华峰的研究中肝转移患者5例,本研究中为4例)。在不良反应方面,治疗后观察组患者发热、肝功能异常和疲劳的发生率较低,与EORTC QLQ-C30量表中疲劳评分较低相一致;皮肤黏膜反应、高血压和甲状腺功能减退的发生率较高,可能与舒尼替尼抑制正常新生组织的血管生成有关[17]。由于甲状腺功能减退早期以疲劳等不典型症状为主,需及时检测体内甲状腺激素水平以确诊并予以对症治疗。需要指出的是,关于舒尼替尼2/1方案的疗效、耐受性是否较4/2方案好的报道不一[20-21],专家建议,在没有充分数据支持的情况下,仍应以舒尼替尼4/2方案为mRCC的初始治疗方案,后续如出现剂量依赖的不良反应方可考虑换用舒尼替尼2/1方案[22]。因此,本研究也以舒尼替尼4/2方案为初始治疗方案,不能耐受者才改用2/1方案。
综上所述,舒尼替尼治疗mRCC疗效肯定,不良反应可耐受,对于患者的长期随访观察仍在进行中。然而,本研究为单中心回顾性研究,这一结论仍有待多中心、多样本研究的进一步验证。

