基于色谱-质谱法的肉类食品中大环内酯类药物残留及其代谢产物分析方法研究进展
贾 玮,王 菡,石 琳,许秀丽,储晓刚,
(1.陕西科技大学 食品与生物工程学院,陕西 西安 710021;2.中国检验检疫科学研究院,北京 100123)
随着许多食品安全事件的发生,食品安全问题日益受到关注,我国《“十三五”国家食品安全规划》为进一步提升食品安全标准管理水平,深入开展了农兽药残留综合治理工作,其中兽药残留问题是我国食品药品监管部门重点控制的问题之一[1-2]。大环内酯类药物(Macrolide drugs,MALs)是兽药中非常重要的一类广谱抗菌性抗生素,普遍应用于治疗猪、羊、牛和家禽的呼吸性及传染性疾病,或在低剂量下作为饲料添加剂促进动物生长发育[3]。但长期食用会导致大环内酯类药物及其代谢物在动物组织及器官内蓄积或储存,当该药物在人体内累积达一定浓度时,可引起胃肠道不良反应和耳蜗神经损害,严重者还会造成肝肾的损伤[4-5],此外,食品中的大环内酯类抗生素残留不仅易造成致敏和毒性反应,致使细菌耐药性升高,引起携带耐药因子菌株的扩散[6-7],残留的药物进入环境中还会导致严重的环境问题[8]。欧盟委员会[9]、我国农业部[10]、美国[11]、日本[12]等均对肉类食品中的大环内酯类药物及其最大残留限量(MRL)进行了限制(见表1),但各国监管机构均未发布针对大环内酯类药物代谢产物的分析方法。开展动物源性食品中大环内酯类药物及其代谢产物残留的监测工作可为制定和完善国家标准提供参考,对于保障肉类食品的食用安全,保障人类健康及肉类食品产业发展具有重要意义。本文介绍了大环内酯类兽药分析检测的背景现状,以及大环内酯类药物进入畜禽类动物体内形成的代谢产物及其分布部位,对国内外肉类食品中大环内酯类兽药残留的前处理方法及检测方法进行研究与探讨,同时对大环内酯类药物及其代谢产物残留分析的研究方向进行了展望。

表1 各国及地区对大环内酯类药物的最大残留限量规定[9-12]Table 1 MRLs of macrolides in different countries and regions[9-12] w/(μg·kg-1)
EU:欧盟;CHN:中国;USA:美国;JPN:日本
1 大环内酯类药物残留检测研究现状
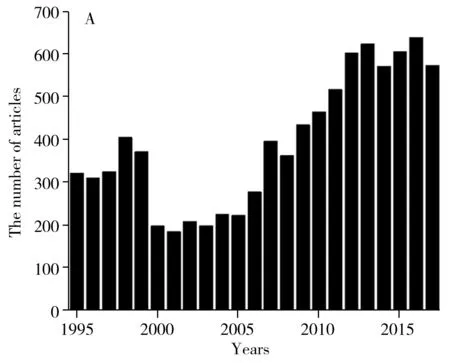
目前在Web of science数据库中,以macrolide(and) detection(or) veterinary drugs(and) detection为主题共检索出10 835篇文献,近5年约占29%,如图1A所示。在中国知网数据库中,以大环内酯为检索词全文检索,共检索出10 640篇,近5年约占44%,如图1B所示。总体上,近10年国内外对大环内酯类抗生素的研究均明显增多,近5年国内外有关大环内酯类药物研究的文献比例均较高,表明大环内酯类药物正引起人们的日益关注。
2 大环内酯类药物代谢产物及其分布
兽药残留是指给动物使用兽药后,蓄积或贮存在动物细胞、组织或器官内的药物原形、代谢产物和药物杂质[13]。大环内酯类药物进入动物机体后,经肠胃的消化会产生复杂的代谢产物,代谢物保留了原有的活性基团,仍具有与原药相似的抗菌活性,部分代谢产物的潜在危害甚至高于原药形式。药物原形和代谢产物通常以游离或结合的形式残留在畜禽产品中[14]。目前国内外对大环内酯类药物的研究多为原药检测,对其代谢物的检测报道较少。为检测食品中的大环内酯类兽药残留总量,需对大环内酯类药物代谢物及其分布进行研究。常见的大环内酯类药物有泰乐菌素、替米考星、西地霉素、红霉素、竹桃霉素、螺旋霉素、吉他霉素、交沙霉素等。

西地霉素在机体内易发生代谢,代谢物有20多种,主要为兰卡杀菌素C、兰卡杀菌醇和兰卡杀菌醇A。西地霉素原药和代谢产物在动物机体内的滞留期短,畜类肝中的药物残留最高,肌肉和脂肪中未检出残留[18]。红霉素广泛分布于各种组织及体液中,并以在胆汁和肝脏中的含量最高,大部分药物在肝脏代谢[19],主要代谢途径为脱氧糖胺的N-去甲基化,代谢物主要为脱水红霉素A和红霉素A烯醇醚等[20]。竹桃霉素内服一般用三乙酰竹桃霉素,三乙酰竹桃霉素可在动物机体内代谢,而竹桃霉素在体内不代谢,在大部分组织如肝、肾中可检测到残留物,主要代谢产物为醋竹桃霉素。因此,检测大环内酯类药物的代谢物对监控此类药物残留更具实际意义。
螺旋霉素经机体吸收后广泛分布于体内,主要代谢产物为新螺旋霉素。螺旋霉素于肝脏代谢,在动物的肝和肾中残留最高[21]。吉他霉素的机体吸收良好,广泛分布于主要的脏器,尤其以肝脏和肾脏中的浓度最高,主要经肝胆系统排泄,在胆汁和排泄物中的浓度高,少量经肾脏排泄。吉他霉素的代谢途径为羟化,其在肠道吸收快,释出也快,因此是在动物组织中残留量最低的一种大环内酯类药物。交沙霉素机体吸收迅速,残留物在组织和脏器中浓度高,特别是在胆汁和肺中浓度较高,主要经胆汁排泄[22]。
目前为止,仅有少量文献对同时检测大环内酯类抗生素及其代谢物进行报道[23-25]。因此,有必要建立多残留分析方法测定肉类食品中大环内酯类药物及其代谢产物的残留。
3 大环内酯类药物及其代谢产物的分析方法
3.1 样品前处理
为制备适用于色谱或液相色谱-质谱(LC-MS)法的供试液,需对样品进行前处理。首先对样品进行研磨或匀浆处理,然后进行提取、净化、浓缩等步骤。由于肉类食品基质的复杂性,一部分大环内酯类药物残留与基质中的大分子(蛋白质等)结合,引起严重的基质干扰,故前处理必须分离药物与蛋白质的结合体,以除去蛋白质等杂质的干扰,最大限度地提取大环内酯类药物残留。目前常见的前处理方法有液-液萃取(Liquid-liquid extraction,LLE)、固相萃取(Solid phase extraction,SPE)、QuEChERS(Quick、Easy、Cheap、Effective、Rugged、Safe)、分子印迹(Molecular imprinting,MI)、加压溶剂萃取(Pressurised liquid extraction,PLE)、在线固相萃取(Online SPE)等。
3.1.1液-液萃取法液-液萃取通过加入一定的极性或非极性有机试剂进行提取,一般采用乙酸乙酯、氯仿等进行提取后过膜处理,除去杂质,用流动相溶解后进样分析。岳振峰等[26]在聚丙烯离心管中用乙腈萃取动物组织中的大环内酯类抗生素,然后以正己烷脱脂,旋转蒸发浓缩后进行测定,得到肉类食品中的回收率为60%~99%。液-液萃取法可用于大环内酯类药物残留的定量检验,对实验条件和仪器要求不高,但该方法的净化效果相对较差、操作费时、有机溶剂消耗大。
3.1.2固相萃取法固相萃取法是最常用的净化方式,该方法是将待测物质从不同样品中分离后,经过不同类型的固相萃取进行富集、净化及除杂[27-28]。目前,已有多种SPE柱被用于大环内酯类药物的纯化,如C18柱[29]、HLB柱[30]、PEP柱[31]、Prime HLB柱[32]等,且均能有效地分离纯化肉类食品中的大环内酯类药物。目前常采用液相萃取结合固相萃取的方法进行大环内酯类药物及代谢产物残留的检测,Cao等[33]在检测家禽肌肉中兽药残留物的过程中,采用PSA和NH2去除提取物中的脂质和碳水化合物,乙腈-乙醇水溶液萃取,正己烷纯化,定量下限为0.05~10 μg/kg。该方法符合欧盟委员会决议2 002/657/EC的标准并已成功用于当地市场(中国)的家禽肌肉样品分析。
3.1.3QuEChERS法QuEChERS法因快速、高效、成本低等特点被广泛用于农药检测领域,近年来也逐渐应用于兽药残留检测,但在肉类食品的大环内酯类药物残留检测中应用较少[34-35]。郭海霞等[36]通过一次提取分步净化的方式,实现了121种兽药的同时分析,该方法对C18、PSA、NH2和GCB 4种吸附剂的净化效果进行了比较,发现C18和PSA结合的效果最好,可更好地去除基质中的有机酸、糖类等干扰物,极大地降低了分析费用,缩短了检测周期,对肉类加工企业的质量安全控制具有较高的实用价值。
3.1.4分子印迹技术分子印迹技术在兽药残留分析领域是一种新兴的分析手段。分子印迹聚合物(MIP)制备简单,稳定性好,能重复使用,故可用作SPE填料或分子印迹薄膜来分离富集复杂基质中的痕量分析物,已被广泛应用于兽药残留的分析[37]。Zhou等[38]以螺旋霉素为模板,制备了对阿奇霉素具有高选择性的分子印迹聚合物整体式微柱,建立了基于分子印迹联用液相色谱-串联质谱检测猪肉中阿奇霉素残留量的简便、高灵敏度的方法。该法克服了复杂基质和杂质的干扰,比传统固相萃取法具有更好的净化效果。
3.1.5加压溶剂萃取法加压溶剂萃取通过升温和加压提高物质的溶解度和溶质扩散效率,从而提高萃取效率。该方法萃取时间短、萃取溶剂用量少、萃取率高、自动化程度高,可应用于食品中大环内酯类药物残留的测定。如Juan 等[39]分析了肉类和牛奶中5种大环内酯类药物残留,使用不同量的海砂和EDTA研究了提取方法以及固相分散萃取法,并对溶剂、提取时间、温度和压力条件进行了优化。将该方法应用于筛查瓦伦西亚社区市场的牛奶和肉类样品中的大环内酯和林可酰胺残留,回收率均在70%以上,4个阳性样本残留量均高于欧盟立法规定的最大残留量,为食品安全风险事件提供了可靠的技术保障。
3.1.6在线固相萃取法与传统固相萃取技术相比,在线固相萃取具有操作简便、稳定性好、检出限低、灵敏度高等优势。张晓光等[40]采用在线固相萃取净化/液相色谱-串联质谱方法检测猪肉中的10种大环内酯类药物残留,样品以乙腈提取,经在线固相萃取柱净化,甲醇洗脱后,转移至色谱柱中进行分离,用四极杆质谱检测。通过对固相萃取参数、液相色谱参数、质谱参数进行优化,有效降低了基质效应;利用在线固相萃取装置,克服了传统固相萃取稳定性差、操作繁琐、成本高、资源消耗大等缺点。该方法实用性强,后期可对检测品种进行扩充。
3.2 检测方法
目前有关大环内酯类药物残留的检测技术主要为高效液相色谱法和液相色谱-质谱联用法(LC-MS),表2列出了部分大环内酯类药物残留的分析条件。

表2 肉类食品中大环内酯类药物的分析条件Table 2 Analysis conditions of macrolide in meat food
(续表2)

Veterinary drugSampleSample preparationStationary phaseMobile phaseScan methodDetection limit/recoveryReference林可霉素、克林霉素、螺旋霉素、红霉素、替米考星、泰乐菌素猪肉Mcllvaine缓冲液提取,液液分配,HLB固相萃取柱、MCX固相萃取柱、QuEChERS基质分散固相萃取净化Waters Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm)流动相A为1 mol/L pH 5.0乙酸铵10 mL+水990 mL,B为1 mol/L pH 5.0乙酸铵10 mL+甲醇990 mLESI+,MRM10 μg/kg/60%[43]替米考星、泰乐菌素牛肝,肌肉乙腈提取,分散固相萃取净化Acquity HSS-T3(100×2.1 mm,1.8 μm)流动相A为水-乙腈(体积比98∶2),含10 mmol/L甲酸铵水溶液,B为甲醇-乙腈(体积比75∶25),含0.1%甲酸ESI±,SRM确定限(CCα)为54~1 147 μg/kg,检测容量(CCβ)为58~1 294 μg/kg[42]克林霉素、红霉素、吉它霉素、林可霉素等猪肉乙腈提取,液液分配,Prime HLB固相萃取柱净化Waters Acquity BEH C18(100 mm×2.1 mm,1.7 μm)流动相A为甲醇,B为0.1%甲酸溶液ESI+,MRM-/77.9%~122.3%[32]阿奇霉素、罗红霉素、吉他霉素等猪肉EDTA 溶液,乙腈-甲醇(体积比95∶5) 提取,PEP-2 固相萃取柱净化Waters UP-LCTM BEH C18(100 mm × 1.0 mm,1.7 μm)流动相A为0.1%甲酸水溶液,B为甲醇,C为水,D为乙腈ESI+,MRM0.2~5 μg/kg/30%~140%[31]林可霉素、托拉菌素、螺旋霉素等猪肉乙腈提取,经在线固相萃取柱(HLB柱)富集净化,甲醇洗脱X Bridge BEH C18色谱柱流动相A为10 mmol/L乙酸铵水溶液,B为乙腈ESI+,MRM0.05~0.3 μg/kg/69.6%~115.2%[39]林可霉素、红霉素、竹桃霉素牛肝乙腈-甲醇提取,Oasis PRiME HLB净化ACQUITY UP-LC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm)流动相A为乙腈,B为2 mmol/L乙酸铵水溶液(含0.2%甲酸)ESI+,MRM0.07~0.78 μg/kg/67.5%~102.0%[47]替米考星、泰乐菌素畜禽肉甲醇洗脱,固相萃取装置,加入乙腈-乙酸铵UPLC BEH C18色谱柱(50 mm ×2.1 mm,1.7 μm)流动相A为乙腈(含0.2%甲酸),B为0.006 mol/L乙酸铵ESI+,MRM0.83,3.05 μg/kg/78.3%~87%[48]螺旋霉素、阿奇霉素、替米考星、红霉素A、泰乐菌素、吉他霉素等猪肉5%乙酸乙腈溶液和Na2EDTA提取,液液分配,300 mg C18和400mg NH2吸附剂的50 mL具塞离心管净化ZORBAXSB-C18色谱柱(100 mm×2.1 mm,3.5 μm)流动相A为乙腈,B为0.1%甲酸水溶液(含5 mmol/L乙酸铵)ESI+,MRM-/67.0%~109.0%[49]交沙霉素、红霉素、克林霉素、罗红霉素、阿奇霉素、泰乐菌素等猪肉Na2EDTA-Mcil-vaine缓冲溶液(pH 4.0)和乙腈提取,无水硫酸钠除水,上清液分两组,用不同的QuEChERS净化剂净化ACQUITY UP-LC HSS T3柱(100 mm×2.1 mm,1.7 μm)正离子模式:流动相A为0.1%甲酸-5 mmol/L乙酸铵,B为甲醇;负离子模式:流动相A为水,B为甲醇ESI+,MRM2.0~10 μg/kg/65.8%~105.7%[36]

红霉素、交沙霉素、螺旋霉素、泰乐菌素、竹桃霉素动物组织样品乙腈提取,液液分配,正己烷脱脂,异丙醇净化Luna C18 色谱柱(150 mm ×2.0 mm,3 μm)流动相A为0.1%甲酸的乙腈-甲醇(1∶1),B为50 mmol/L乙酸铵水溶液ESI+,MRM0.05~5.3 μg/kg/70.3%~102%[26]
(续表2)

Veterinary drugSampleSample preparationStationary phaseMobile phaseScan methodDetection limit/recoveryReference螺旋霉素、替米考星、阿奇霉素、泰乐菌素、林可霉素、克林霉素动物肌肉0.1%甲酸的乙腈提取,高性能分散仪萃取,离心,在聚丙烯管中低温纯化Agela Durashell RP(100 mm×2.1 mm,5 μm)保护柱填充C18(Security Guard Phe-nomenex,4.0 mm×3.0 mm,5 μm)流动相A为0.1%甲酸水溶液和5 mmol/L甲酸铵,B为含0.1%甲酸和5 mmol/L甲酸铵的甲醇ESI+,SRMCCβ为1.0~50.0 μg/kg,CCα为120.3 μg/L[45]林可霉素、克林霉素、螺旋霉素、替米考星、泰乐菌素等家禽肌肉正己烷脱脂,使用PSA和NH2的管中的分散固相萃取(D-SPE)除杂Acquity HSS-T3色谱柱(100 mm×2.1 mm,1.8 μm)流动相A为0.1%(体积分数)甲酸的甲醇,B为0.1%甲酸ESI+,MRM-/60%~139%[33]替米考星、螺旋霉素、红霉素A、阿奇霉素等动物肌肉乙酸乙酯提取,液液分配,1 mL 5%氨水的甲醇溶液洗脱,MISPE纯化Zorbax SB-Aq C18柱(150 mm×2.1 mm,3.5 μm)流动相A为乙腈,B为0.1%甲酸水ESI+,MRM0.1~0.4 μg/g/60.7%~100.3%[44]多拉菌素、伊维菌素牛肉乙腈提取,C18固相萃取柱净化C18 柱(250 mm×4.6 mm,5 μm)流动相A为乙腈,B为水荧光检测器1.5 μg/kg/70.0%~120.0%[41]替米考星、螺旋霉素、红霉素等牛肉、猪肉、鸡肉乙腈、甲酸铵提取,分散固相萃取净化YMC-Triart C18柱(3.0 mm×100 mm,3 μm)流动相A为水(含0.1%甲酸),B为乙腈(含0.1%甲酸)ESI-,MRMCCβ为17~358 μg/kg/60%~217%[50]
-not reported
3.2.1液相色谱法高效液相色谱适用于极性大、沸点高的化合物分离分析。该法采用一定的提取手段将被分析对象溶于可作为流动相的溶剂中,直接进行检测分析,具有柱效高、选择性好、价格低、分析速度快、应用范围广等优势,被广泛应用于食品中兽药残留的检测。根据食品基质的不同选择不同的检测器,常用的检测器有紫外检测器(UVD)、荧光检测器(FLD)、电化学检测器(ECD)、二极管阵列检测器(DAD)等。由于MALs难以气化,并且多具有强的紫外线吸收,所以高效液相色谱法是MALs残留的常用测定方法。王梅等[41]采用高效液相色谱法/荧光检测器测定牛肉组织中多拉菌素、伊维菌素残留量,两种待测物在3.0~200.0 μg/L 范围内呈良好的线性关系,样品加标回收率为70.0%~120.0%,方法检出限为1.5 μg/kg。该方法有效简化了现行农业部781号公告标准的繁琐处理步骤,缩短了衍生时间,有效保护了色谱柱,且操作简单,重复性好,但只能用于已知目标化合物的分析,无法进行未知化合物的筛查。
3.2.2液相色谱-质谱联用法液相色谱-质谱联用法(LC-MS)在兽药分析领域的应用日益广泛,因能够以较高强度提供更窄的峰值,从而可显著提高方法的灵敏度和选择性,并可加快分析速度,具有较宽的线性范围,适合于确证分析,故被用于大环内酯类药物的残留分析[42]。LC-MS除可分析强极性、难挥发、热不稳定的化合物之外,还具有分析范围广、分离能力强、定性分析结果可靠、检出限低、分析时间快、自动化程度高等优点。目前各种食品基质中大环内酯类药物的液质联用检测方法均有报道。
高分辨飞行时间质谱(Time of flight mass spectrometry,TOF MS)近年来在食品安全分析领域的应用也越来越广泛,与低分辨的串联四极杆质谱相比,TOF MS具有定性与定量结果准确、灵敏度高、质量精度高、具有正负切换扫描功能等优势。郝杰等[43]使用高分辨飞行时间质谱对猪肉中包括大环内酯类在内的29种抗菌药物进行同时检测,并比较了不同固相萃取柱的净化效果,选用HLB固相萃取柱,建立了基于精确质量数的筛查数据库和优化的定量方法,29种抗菌药物的定量下限为0.5~10 μg/kg,平均回收率为50.10%~118.33%。该方法满足食品安全风险突发事件快速应急处理工作中高通量、高可靠性确证和定量分析的要求,为相关工作提供了可靠的技术保障。
Song等[44]以泰乐菌素作为模板,甲基丙烯酸作为功能单体合成分子印迹聚合物(MIPs),采用分子印迹固相萃取与液相色谱-串联质谱联用的方法测定动物肌肉样品中10种大环内酯类药物残留。结果表明,MIP对大环内酯类药物具有良好的识别性能,比传统固相萃取具有更好的净化效果。药物的回收率为60.7%~100.3%,检出限为0.1~0.4 μg/kg,该方法可用于动物肌肉中大环内酯类药物残留的常规监测。Jank等[45]建立了肉类食品中大环内酯类药物残留的筛查方法,该方法采用2002/657/EC标准进行了验证,确定了特异性验证参数,检测容量(CCβ)为1.0~50.0 μg/L,确定限(CCα)为120.3 μg/L。该方法快速、简便,适用于常规实验室的高通量分析,已应用于巴西国家残留控制计划,用于抗生素残留确定。
4 结 论
近年来我国在兽药残留检测领域发展迅速,对药物残留的检测能力也大大提升。但随着药物结构的逐渐复杂化、低剂量化和新型药物研发数量的日益增多,对检测技术的要求也越来越高。然而国内关于快速检测大环内酯类药物及其代谢产物的相关研究尚不完善,有待于进一步开发探索,以实现快速准确地从复杂基质中分离大环内酯类药物及其代谢产物,并获得较高的回收率和较好的测定结果。如何高效地将大环内酯类药物及代谢产物从复杂基质中分离,并建立动物源性食品中多类兽药残留及其代谢产物的非定向筛查方法,将成为新的研究趋势。

