KCl部分替代NaCl制作低盐切达干酪的研究
马春丽,屈倩,宋兰兰,石静文,梁佳琪
(东北农业大学食品学院,黑龙江哈尔滨150030)
干酪是乳品营养物质的浓缩,被称为“奶黄金”。含有丰富的蛋白质,脂质,维生素及矿物质,它们在健康膳食中扮演着重要角色[1]。随着人们对健康的关注,干酪产品已不再简单地追求高品质,而是转向更适合消费者的方向,满足消费者的健康需求[2]。
干酪中高钠含量已成为全世界公众健康关注的主要问题[3]。氯化钠(NaCl)几乎是所有种类干酪必不可少的原料[4],依据干酪品种不同,其盐含量在0.7%~6%,切达干酪盐含量约为6.2 g/kg[5]。它可以加快乳清排出[6],控制微生物生长、酶活性、蛋白质水解作用以及脱水收缩作用[7],在干酪的风味、质构和货架期方面扮演着重要的角色[2]。然而,过量的食用钠盐会增加高血压,冠心病,骨质疏松症等慢性疾病的患病风险[8]。因此,应尝试减少干酪尤其是切达干酪中的钠盐含量。
当干酪中盐浓度减少时,蛋白质水解,水分活度,酸度以及苦味就会增加,硬度会减小[9],由于NaCl能显著影响干酪的质构和感官性能,因此很难完全从干酪中移除[10]。用其它盐代替钠盐是减少干酪中Na含量的一个可行方法。KCl被认为是很有潜力的盐替代物[9,11-12],首先KCl替代具有安全性[13],其次KCl与NaCl物理性质相似,能够帮助维持盐味。干酪中KCl替代NaCl对产品的流变性和感官影响最小甚至不影响其感官、流变性和稳定性[14]。然而KCl达到一定呈味阈值具有苦味,因此应该谨慎选择KCl替代NaCl的比例。一些研究也评估了钾盐在干酪中作为钠盐替代物的潜力。有研究报道,在农家奶酪或长时间凝乳的切达奶酪中,减少NaCl添加总量的35%~37.5%,是可接受的[15]。Katsiari等[16-17]报道使用KCl部分替代NaCl,使Feta干酪和Kefalograviera干酪中Na含量成功减少了50%,干酪总成分和感官性能没有受到影响。在另外一些研究中,KCl部分替代NaCl对Minas干酪蛋白质水解没有明显影响[18],对Halloumi干酪的质构特性也没有显著影响[19]。但是,Fynbo干酪中KCl代替NaCl虽然对基本理化指标无影响,但影响蛋白水解作用[20],Ayyash等[21]报道使用部分KCl替代NaCl会改变干酪中的小肽,Demott等[22]报道,当Cottage奶酪中Na替代水平超过50%,会导致干酪风味下降。此外,单独使用KCl盐制作的干酪苦味较重并产生质构的改变[11]。而目前国内对降低干酪中钠盐含量的报道较少。
本研究旨在确定KCl部分替代NaCl对切达干酪化学组分,乳酸菌生长,质构,苦味等方面的影响,以降低切达干酪中钠含量。
1 材料与方法
1.1 材料与试剂
原料乳(新鲜无抗乳):哈尔滨市香坊农场;直投式发酵剂 R-704、凝乳酶 Stamix1150(35 000 U/g):丹麦科汉森公司;NaCl:中国盐业总公司。
试剂均为分析纯。
1.2 仪器与设备
FOSS2300凯氏定氮仪:FOSS公司;XMTW-2000马弗炉:天津市中环实验电炉有限公司;AA-6800原子吸收分光光度计:日本岛津公司;PHS-3C精密pH计:北京朋利驰科技有限公司;干酪槽、干酪刀:东北农业大学食品学院保存;DZDD400/2SB型真空包装机:中国通州腾飞食品包装机械厂;TA-XT plus型质构仪:英国Srablemicro公司。
1.3 方法
1.3.1 切达干酪制作和试验设计
参考Grummer等[23]方法。
新鲜原料乳→标准化→巴氏杀菌(63℃,30 min)→冷却(31℃~32℃)→添加发酵剂(0.01%)→添加氯化钙(0.01%~0.02%)→静置发酵(至pH值6.2)→添加凝乳酶→凝乳(至pH值4.7)→切割→搅拌、加温→排乳清→堆叠→粉碎→加入不同比例盐→压榨成型→真空包装→成熟
根据不同的盐处理方法做成5组干酪:(A)1.7%NaCl,(B)0.85%NaCl,(C)3NaCl:1KCl,(D)1NaCl:1KCl和(E)1NaCl:3KCl。其中 KCl替代部分 NaCl,盐总量为1.7%。
1.3.2 干酪组成成分测定
在干酪成熟 0、7、14、21、28 d 时取样测定组成成分。干酪水分含量的测定采用直接干燥法参考GB 5009.3-2016《食品安全国家标准食品中水分的测定》;蛋白质含量测定采用凯氏定氮法参考GB 5009.5-2010《食品安全国家标准食品中蛋白质的测定》;脂肪含量测定采用罗兹-哥特里法参考GB 5009.6-2016《食品安全国家标准食品中脂肪的测定》;灰分含量测定参考国标GB 5009.4-2010《食品安全国家标准食品中灰分的测定》。
1.3.3 矿物质元素Na、K含量的测定
钠、钾含量测定采用火焰原子吸收分光光度法参考GB 5009.91-2017《食品安全国家标食品中钾、钠的测定》。
1.3.4 干酪pH值测定
取干酪样品1 g,加入10 mL去离子水,6 000 r/min匀浆1 min,静置30 min,过滤,用pH计测定。
1.3.5 干酪微生物指标测定
从干酪成熟期第 0、7、14、21、28天分别无菌取样1 g,采用平板菌落计数法,利用MRS琼脂培养基,37℃培养48 h,测定干酪中乳酸菌总数。
1.3.6 干酪质构分析
利用质构分析仪测定干酪的硬度和弹性。将待测样品切为(2.00±0.05)cm的立方体,室温下放置 2 h,测试前探头下降速度为2 mm/s,测试速度为1 mm/s,测试后探头回程速度为2 mm/s,下压距离10 mm,间隔时间 10 s,触发压 5 g,探头型号 P/0.5[7]。
1.3.7 干酪苦味评价
感官鉴定前,将干酪样品放在4℃过夜,然后于室温放置1 h。以不同浓度的硫酸奎宁作为参比溶液(2.9×10-3、5.8×10-3、1.2×10-2、和 2.4×10-2mmol),对干酪苦味进行感官评价。评定员用水彻底漱口后,取1.5 cm3大小的干酪样品于口中停留10 s,参照表1评分标准进行打分,打分均值就是苦味值[24]。

表1 切达干酪苦味评定标准Table 1 Grading standard for bitterness of cheddar cheese
1.3.8 统计学分析
每个试验重复3次,采用SPSS22.0统计软件进行分析处理,LSD法用于差异显著性分析,采用Microsoft Excel 2007作图。
2 结果与分析
2.1 干酪成熟过程中主要组成成分分析
5组切达干酪理化指标结果见表2。
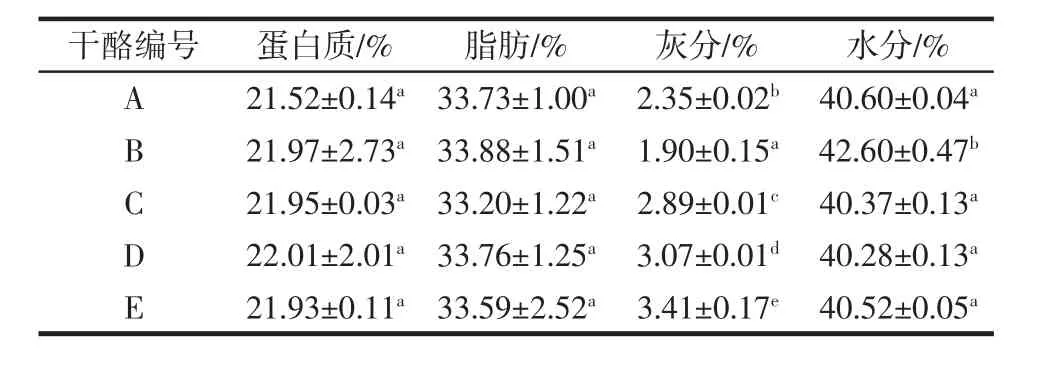
表2 切达干酪主要理化指标Table 2 The main physicochemical properties of cheddar cheese
从表2中可以看出各组干酪蛋白质,脂肪含量差异不显著(P>0.05),该结果与 Aly[25]、Katsiari等[17]和Fitzgerald等[26]使用KCl替代NaCl对不同种类干酪组成成分的影响一致。B组低盐干酪水分含量显著高于A组干酪,这与Schroeder等[27]研究的低盐干酪比正常盐干酪水分含量高的结论一致。而KCl部分替代NaCl对干酪的水分含量无显著影响(P>0.05),主要是由于KCl的性质与NaCl极为相似,同样可以增加干酪的持水力[28]。而每组干酪中灰分含量随着KCl添加比例增大而增多,原因可能是KCl渗入干酪比NaCl多,增加了钾含量,进而增加灰分含量[29]。
2.2 干酪成熟过程中pH值变化
切达干酪成熟期间pH值的变化见表3。
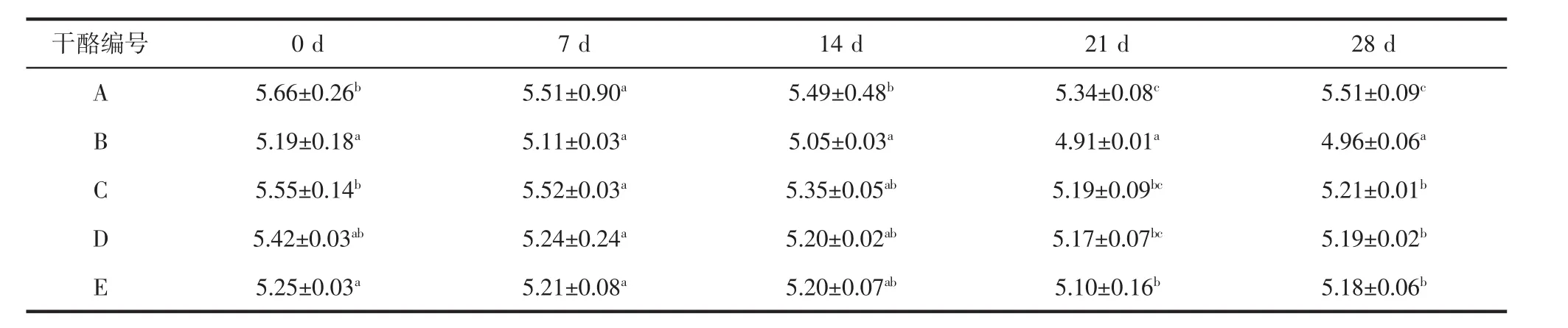
表3 切达干酪成熟期间pH值的变化Table 3 The Changes of pH during ripening of cheddar cheese
由表3可以看出,各组干酪随成熟期的增加,pH值先下降后增加。5组干酪前21天pH值下降可能由于乳清被排除后,乳酸菌分解乳糖为乳酸造成的。21天后,干酪pH值又略有上升的趋势,这可能由于干酪中发酵产生的分解酶来分解蛋白质进而产生一些碱性的物质,使pH值开始增加。成熟过程低盐干酪pH值显著低于正常盐干酪(P<0.05),此结果与Aly[25]得出的结论一致。使用KCl替代NaCl制作的干酪pH值会有轻微降低,此结果与Grummer等[23]使用KCl替代Na-Cl,干酪pH值略有降低结果一致。C、D、E组干酪随着KCl/NaCl比例增加而pH值降低,这是由于细胞内钾离子提供一个发酵的酸环境,使大部分乳糖分解,pH降低,这与McMahon等[30]报道的随着切达干酪中KCl添加量的增加,乳酸含量增加的结果一致。
2.3 干酪成熟过程中矿物质Na、K含量分析
干酪成熟过程中Na、K含量变化如图1和图2所示。

图1 干酪成熟期钠含量变化Fig.1 Sodium content of cheddar cheese during its ripening periods
由图可知,干酪中Na和K的含量与盐溶液中Na、K含量是一致的。每组干酪中Na和K的含量随成熟时间变化不显著(P>0.05),但呈上升趋势,这是由干酪成熟过程中脱水作用所致[7]。而在相同的成熟期,各试验组Na、K含量又有明显不同(P<0.05),这与Ayyash等[9]的研究结果一致。A、B两组干酪之间钾含量差异不显著(P>0.05),随着KCl替代NaCl比例增大,切达干酪中Na含量逐渐减小,K含量逐渐增加。使用 KCl替代 25%,50%,75%NaCl制作的 C、D、E组干酪,均达到了降低切达干酪中钠盐含量的目的。
2.4 干酪成熟过程中乳酸菌的分析
5组切达干酪在成熟期乳酸菌生长情况见图3。
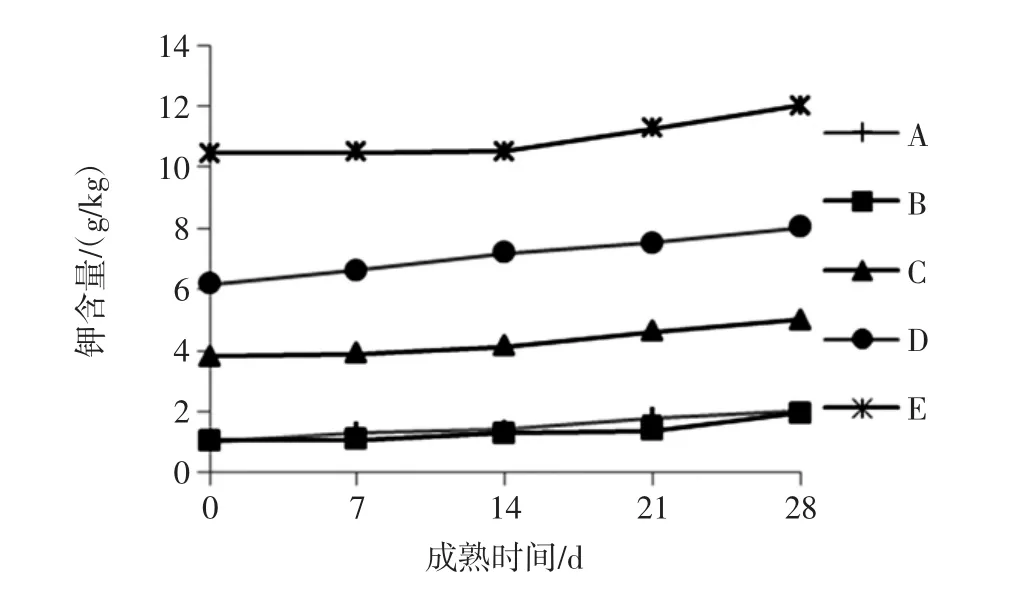
图2 干酪成熟期钾含量变化Fig.2 Potassium content of cheddar cheese during its ripening periods
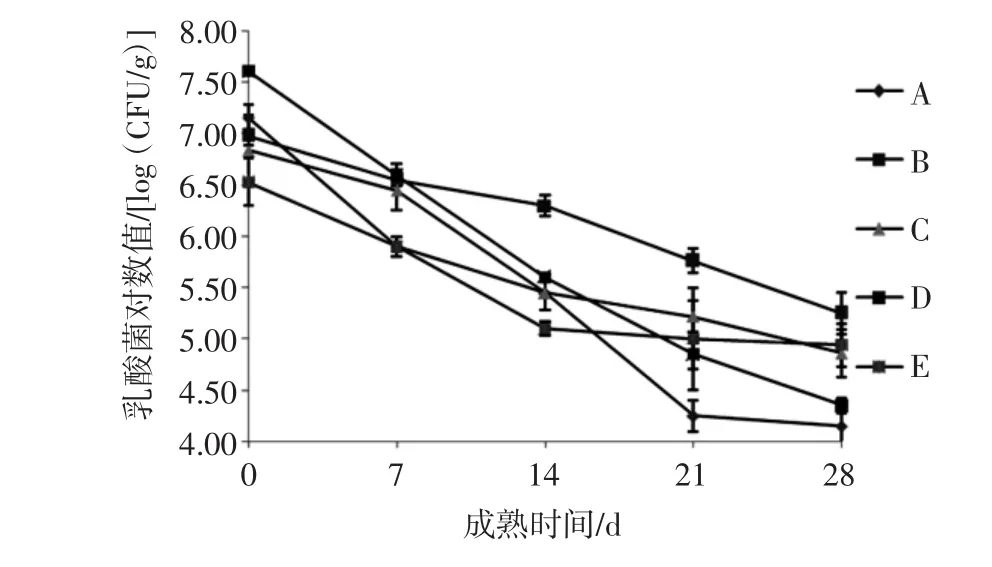
图3 干酪成熟期乳酸菌总数的变化Fig.3 Lactic acid bacteria counts of cheddar cheese during its ripening periods
从图3中可以看出,在成熟初期(0~7 d)乳酸菌总数变化不显著(P>0.05),初期下降趋势没有后期(7 d~28 d)明显,原因可能是成熟初期乳酸菌具有较高活性,使得乳酸菌数保持在一定的数量。各组干酪随着成熟时间的增加,乳酸菌总数逐渐下降,变化显著(P<0.05),这可能是随着成熟期的增加,消耗大量营养物质,导致乳酸菌失活。在同一成熟期,NaCl浓度的减少促进了乳酸菌的生长,其中在干酪成熟28 d时,低盐B组干酪乳酸菌数最高,这说明低盐有利于乳酸菌生长,但会导致苦味的产生。而添加KCl的干酪乳酸菌数比正常盐干酪高,这可能由于Na+和K+对细菌磷脂膜的结合效果不同,K+比Na+的结合要弱,因此对细菌细胞膜的损伤较小[31]。
2.5 干酪成熟过程质构的变化
干酪成熟期间硬度和弹性结果见表4和表5。
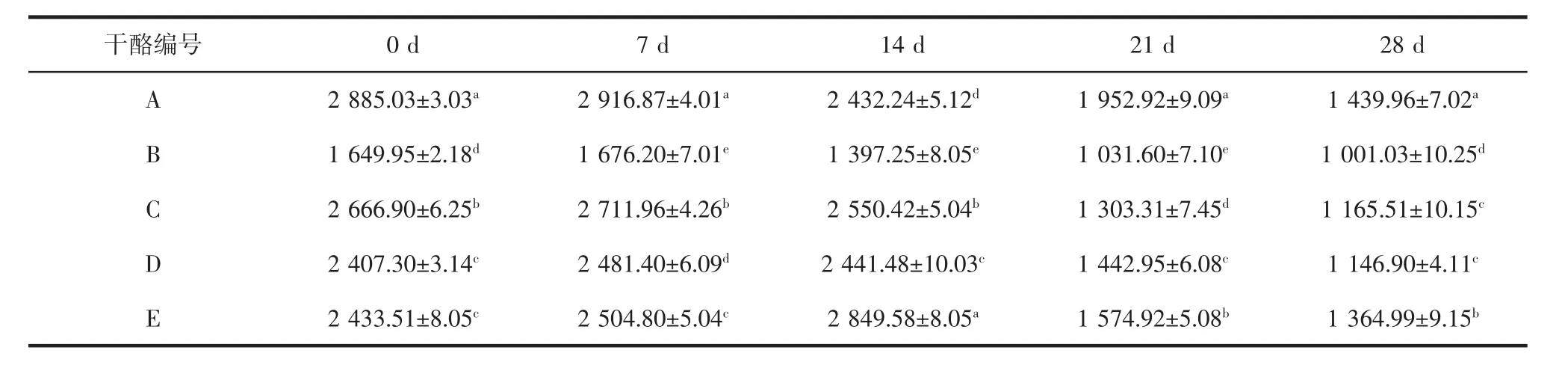
表4 切达干酪成熟期硬度的变化Table 4 The changes of hardness of cheddar cheese during its ripening periods
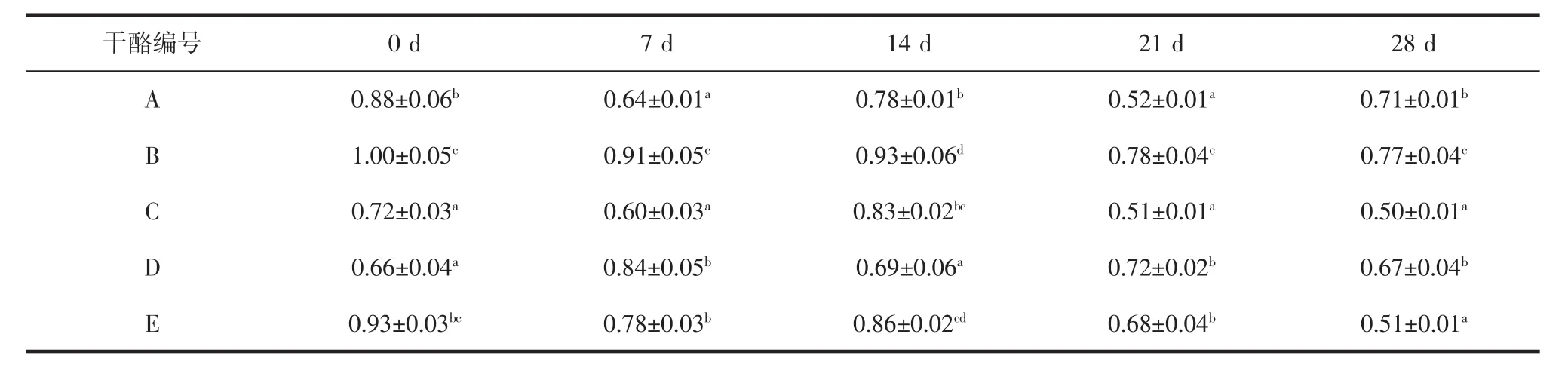
表5 切达干酪成熟期弹性的变化Table 5 The changes of springiness of cheddar cheese during its ripening periods
通常硬度值与水分含量成负相关,酪蛋白吸收水分引起其网络结构膨胀,则弹性增强,硬度减弱[32]。在7 d时,A组干酪硬度值最大为2 916.87 g,其蛋白结构最致密,抵压能力和维持干酪完整性能力强。由表3和4可以看出,硬度和弹性在成熟过程中呈下降趋势。随着成熟时间的增加,5组干酪蛋白质发生水解,引起干酪内部网络结构降解,空穴变大,蛋白质结构松散,干酪硬度下降;随着蛋白质水解加快,质地变得柔软,弹性变差。这些结果与Gunasekaran S等[33]的结果一致。在同一成熟期,低盐B组干酪硬度最小,即添加0.85%NaCl容易生产出松散易碎的干酪,而使用KCl替代的干酪硬度高于低盐组干酪,可以弥补这一缺陷。B组低盐干酪弹性最大,说明盐添加量的减少使干酪弹性大大增加。在干酪成熟28 d时,50%KCl替代对干酪弹性无显著影响(P>0.05),说明50%KCl替代NaCl可以生产出弹性适宜的切达干酪。
2.6 干酪成熟过程中的苦味评价
切达干酪成熟28 d时苦味程度评价值见图4。
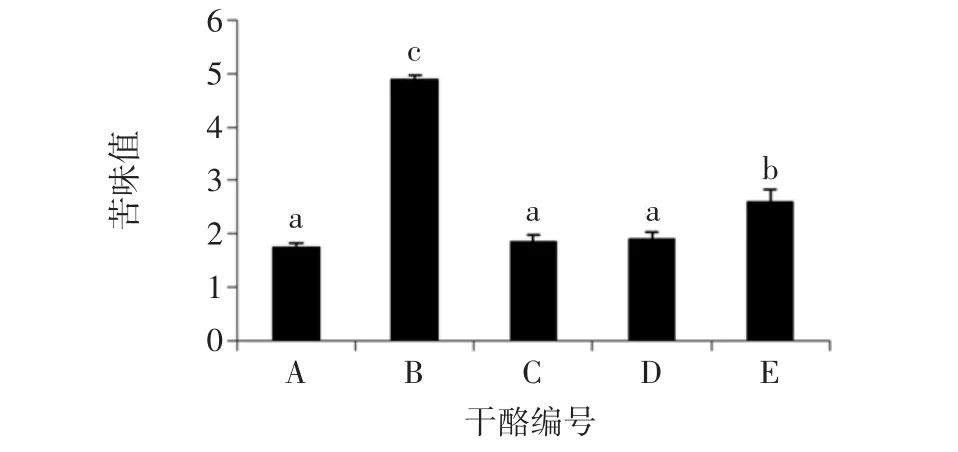
图4 切达干酪苦味值Fig.4 Bitterness of cheddar cheese
低盐B组干酪苦味评分显著高于对照A组干酪(P<0.05),呈强苦味,这可能是由于盐含量降低,菌株相对活跃,酶活性不平衡,蛋白质水解大大增加,导致干酪中苦味肽积累而形成苦味。添加25%和50%KCl的C、D组干酪与正常盐A组干酪差异不显著(P>0.05),但添加75%KCl的E组干酪与A组干酪差异显著(P<0.05),这可能由于KCl达到一定呈味阈值具有苦味。这说明KCl可以替代50%的NaCl,若替代量再高会引起苦味。
3 结论
从以上试验结果可以看出,在盐浓度为1.7%时,KCl 替 代 NaCl 比 例 为 3NaCl:1KCl,1NaCl:1KCl 和1NaCl:3KCl对切达干酪蛋白质,脂肪,水分含量无显著影响,对乳酸菌总数,pH值影响较小,但对灰分,钠含量,钾含量影响显著。使用KCl替代可以弥补低盐干酪松散易碎,硬度较小的的缺陷,在干酪成熟28 d时,1NaCl:1KCl盐替代的干酪弹性与正常盐干酪差异不显著,使用 3NaCl:1KCl,1NaCl:1KCl盐替代的干酪苦味值与正常盐干酪差异不显著,能够改善低盐干酪的苦味缺陷。综合以上分析添加1NaCl:1KCl的干酪整体品质较好,并能有效降低干酪中钠离子含量。钾离子在干酪中的作用还有待于进一步研究。

