粒径对Fe3O4@Con A吸附脱脂乳中乳铁蛋白的影响
张基亮,韩雪,马莺,张兰威,2,*
(1.哈尔滨工业大学化学与化工学院,黑龙江哈尔滨150001;2.中国海洋大学食品科学与工程学院,山东青岛266100)
乳铁蛋白是一个分子量约为80 kU的糖蛋白,参与多种生物学途径,如抗炎、抗微生物、抗肿瘤以及促进成骨细胞增殖等[1]。由于其良好的生物学活性,人们对乳铁蛋白的需求量日益增大。乳铁蛋白可以从脱脂乳中提取,但更多获得其的途径是干酪生产中的副产物乳清。从乳清中提取乳铁蛋白,不仅可以降低乳清高生物需氧量污染的环境问题,同时可以提高乳清利用率,获得更多的乳铁蛋白,是解决限制乳铁蛋白应用瓶颈的一个有效办法。
从上世纪开始,许多分离纯化乳铁蛋白的方法被开发出来,不同提取乳铁蛋白方法的利弊见表1[2-9]。

表1 提取乳铁蛋白方法的利弊比较Table 1 Advantages and disadvantages of different methods on recovery lactoferrin
由于乳铁蛋白对热敏感,容易失活,因此,不需加热、快速提取乳铁蛋白势在必行。纳米材料研究是一个快速发展的科学领域,由于纳米粒子在生物、环境和技术等领域都具有很广泛的应用潜力,发展趋势很大程度上和纳米粒子能够提供的特殊性质和如何改造以适应需要的应用有关。磁性纳米粒子能够有效地纯化蛋白,对于其的研究以及在生命科学中的应用很重要,从选择性和可靠性来说磁性分离和纯化特殊的蛋白是一个便利的方法[10]。磁性纳米粒子另外的一个应用价值体现在磁性纳米粒子表现出来的超顺磁性,这意味着在磁场存在的情况下,磁性纳米粒子具有很强的磁性,而这种强磁性在撤去磁场时会立刻消失,磁性纳米粒子就会重新悬浮于溶液中[11]。由于Fe3O4磁性纳米粒子的各种优点,其有可能成为满足快速、高效乳铁蛋白的材料。
1 材料与方法
1.1 材料、试剂与仪器
FeCl2·4H2O、FeCl3·6H2O:天津博迪化工股份有限公司;50%的腈氨、25%氨水、无水乙醇:天津市天力化学试剂有限公司;伴刀豆蛋白A:北京coolaber公司;磷酸氢二钠、磷酸二氢钠、氯化钠、丙烯酰胺、十二烷基硫酸钠、四甲基乙二胺和过硫酸铵:阿拉丁试剂(上海)有限公司。
PW1800/10X射线衍射仪:荷兰飞利浦公司;AVATAR-360傅里叶变换红外光谱:美国赛默飞公司;S600扫描电镜:日本日立公司;Lakeshore-7300振动磁强计:美国Lakeshore公司;Zetasizer Nano ZS90激光粒度仪:英国马尔文公司。
1.2 方法
1.2.1 磁性纳米粒子的制备
磁性纳米粒子的制备采用共沉淀的方法,具体方法根据Alzahrani[12]的报道。将Fe3+和Fe2+以摩尔浓度比为2∶1的比例溶于250 mL去离子水中,完全溶解后转移至三颈瓶中,将瓶口用胶塞封紧,并在溶液底部通入纯度为99%的高纯N210 min,去除溶液中的溶解氧。10 min后将除去氧的铁离子溶液在100 r/min或200 r/min的机械搅拌下滴加浓度为25%的氨水10 mL,维持溶液的pH值在10~10.5的范围内,持续搅拌10 min。搅拌结束后,将三颈瓶置于80℃的水浴中维持30 min,并保持溶液的pH值在10以上。水浴结束后将铁溶液转移至烧杯中,用磁铁在烧杯底部吸附反应后所生成的黑色沉淀,待绝大部分吸附后,小心除去上清的液体,将沉淀分别用去离子水和乙醇清洗3次,去除未反应的铁及氨水,每步清洗结束后都用磁铁吸附。最后将沉淀在80℃真空干燥箱内烘干,研钵磨碎后备用。
1.2.2 磁性纳米粒子的修饰
磁性纳米粒子的修饰根据lai等[13]的方法略加修改,每20 mg磁性纳米粒子与20 mL pH6.0的磷酸盐缓冲液混合后,在额定功率为650 W的超声功率下超声30 min形成胶体溶液。5 mL浓度为2.5 mg/mL的腈氨溶液加入到胶体溶液中,继续超声30 min,然后将0.5 mL浓度为1 mg/mL的伴刀豆蛋白A(concanavalin A,Con A)溶液加入到胶体溶液中,继续超声30 min,整个超声过程在4℃的环境下进行。用磁铁在烧杯底部吸附修饰Con A后的磁性纳米粒子后,去掉反应溶液,将磁性纳米粒子悬浮在磷酸盐缓冲液中,保存于4℃的冰箱中。
1.2.3 磁性纳米粒子的表征
通过X射线衍射仪(X-ray diffraction,XRD)对制备的磁性纳米粒子进行晶型的分析[14],CuKα为X射线源,波长为λ=1.541 78 Å,加速电压为50 kV。
固体样品采用KBr压片法制样,通过傅里叶变换红外光谱(fourier transform infrared spectroscopy,FTIR)对制备的磁性纳米粒子样品中的非极性化学键进行测量[15],测试的波数范围为 400 cm-1~4 000 cm-1。
将不同转速获得的磁性纳米粒子样品喷金处理10 min后,通过扫描电镜(scanning electron microscope,SEM),加速电压为15 kV,测定磁性纳米粒子的自组装的形态和有序程度[16]。
将不同转速获得的磁性纳米粒子样品通过振动磁强计(vibrating sample magnetometer,VSM)对配体修饰前后的磁性纳米粒子进行测定,最大的外磁场强度为10 kOe,获得其磁滞回线[17]。
利用激光粒度仪对不同转速获得的修饰Con A配体后的磁性纳米粒子样品的平均直径进行测定。
1.2.4 磁性纳米粒子对乳清中乳铁蛋白的吸附作用
将磁性纳米粒子与乳清在烧杯中混合后,吸附一定时间后,用磁铁在烧杯底部使磁性纳米粒子沉淀,弃掉乳清后,加入去离子水清洗磁性纳米粒子沉淀两次后,加入1 mol/L的NaCl进行洗脱,洗脱后用同样的方法沉淀磁性纳米粒子,将收集的洗脱液用十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE) 观察洗脱液的组成。
2 结果与分析
2.1 磁性纳米粒子的晶格特征
制备的磁性纳米粒子中的晶格可以通过XRD来进行表征,XRD的结果见图1。

图1 磁性纳米粒子的X衍射图Fig.1 The XRD image of magnetic nanoparticles
从图1可以看出,该产物的XRD曲线表明磁性纳米粒子存在着7个特征峰,这些特征峰分别为2θ=18.5°(111)、2θ=30.1°(220)、2θ=32.3°(311)、2θ =43.2°(400)、2θ=54.1°(422)、2θ=57.5°(511)以及 2θ=62.6°(440),这些特征峰均为Fe3O4晶体的特征峰,这与Niu等[18]报道的Fe3O4磁性纳米粒子特征峰一致,证明合成的磁性纳米粒子为Fe3O4。
2.2 磁性纳米粒子的FT-IR分析
傅里叶红外光谱可以用于样品中特定官能团、组成和化学结构等的检测,对于官能团的检测具有很高的精确度以及分辨率。磁性纳米粒子的FT-IR结果如图2所示。
从图2中可以看出,在579 cm-1位置的对应峰为Fe3O4中的Fe-O键的伸缩振动,具有Fe3O4的典型特征。这与Safarik报道的结果一致[19],同样证明了采用共沉淀法制备的磁性纳米粒子为Fe3O4。
2.3 磁性纳米粒子形貌分析
采用扫描电镜SEM考察不同搅拌速度对磁性纳米粒子表面形貌的影响,一些具有代表性的SEM图见图3。
从图3A可以看出,转速为100 r/min所制得的磁性纳米粒子的形态不规则,从椭球形到不规则形态都存在,没有较为一致的形貌,而且磁性纳米粒子的粒径分布极其不均匀;从图3B中可以看出,转速为200 r/min所制得的磁性纳米粒子的形态比图3A中所制得的磁性纳米粒子的形态要规则的多,绝大多数的磁性纳米粒子呈现出椭球形。
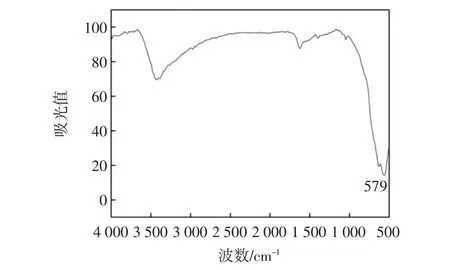
图2 磁性纳米粒子的FTIR图Fig.2 FTIR spectra of magnetic nanoparticles

图3 磁性纳米粒子形貌的扫描电镜图Fig.3 SEM images of morphology of magnetic nanoparticles
2.4 修饰配体后磁性纳米粒子的平均粒径
利用激光粒度仪对修饰配体后的磁性纳米粒子的平均粒径进行测定,其结果表明,转速为100 r/min和200 r/min修饰Con A后的磁性纳米粒子的平均粒径为(82.49±20.34)nm 和(9.77±0.02)nm。结合 SEM图的比例尺观察,其粒径大小相差几乎是10倍。
2.5 磁性纳米粒子磁滞回线
通常讲,磁性纳米粒子的粒径越小,纳米粒子的小尺寸效应越明显,即磁性性能与宏观产物的大小有明显的区别。通过振动样品磁强计在室温下对不同转速获得的磁性纳米粒子进行磁性强度的测定,测得的磁滞回线见图4。
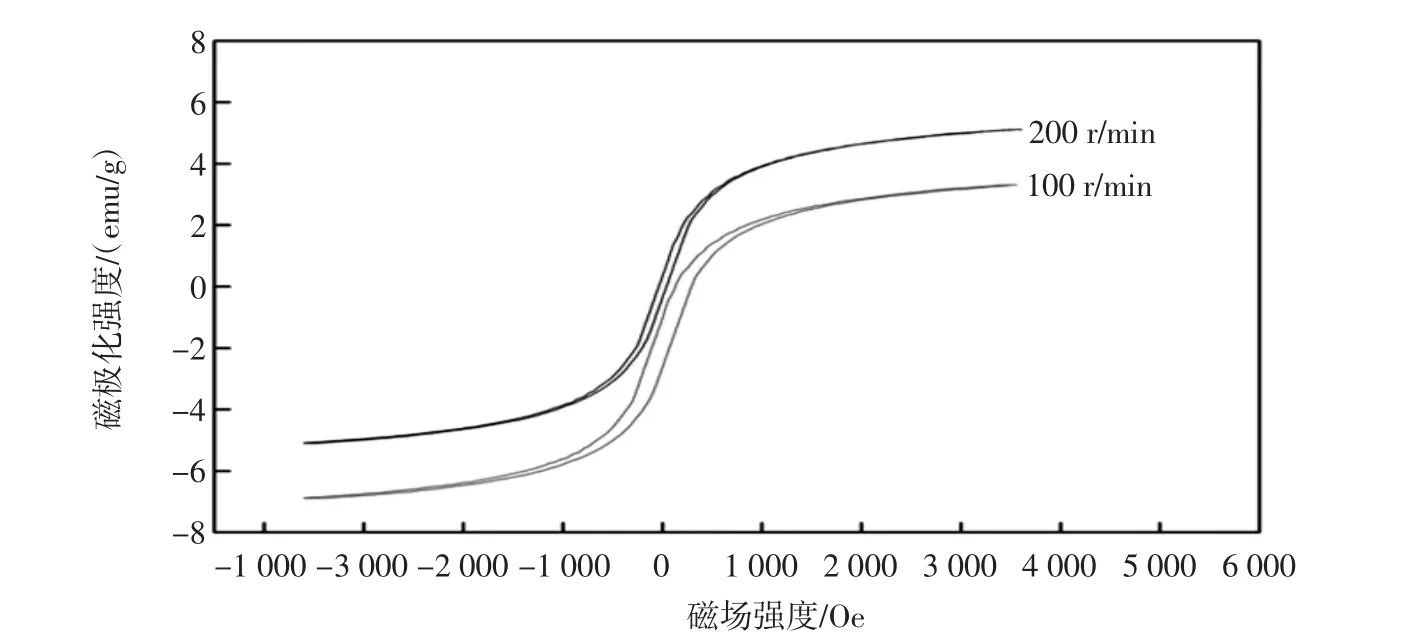
图4 Fe3O4磁性纳米粒子的磁滞回线Fig.4 Hysteresis loop of Fe3O4magnetic nanoparticles
由图4可以看出,在转速为100 r/min的机械搅拌 下所制得的磁性纳米粒子的磁强度为3.68 emu/g,而转速为200 r/min所获得的磁性纳米粒子的磁强度为5.36 emu/g。200 r/min比100 r/min所获得的磁性纳米粒子的磁强度提高了45.65%。不同转速获得的磁性纳米粒子都具有超顺磁性。此外,在外加磁场存在的情况下,Fe3O4磁性纳米粒子具有明显的磁响应性,其结果见图5。

图5 Fe3O4磁性纳米粒子磁性响应图Fig.5 The images of Fe3O4magnetic nanoparticles under an external magnetic field
从图5A可以看出,在没有外源磁场存在的情况下,磁性纳米粒子均匀的分散于水溶液中,说明其具有良好的分散性。从图5B中可以开出,在有外源磁场存在的情况下,磁性纳米粒子都集中在外加磁铁处,说明磁性纳米粒子具有很好的超顺磁性和磁相应性。这与zhang等[20]研究Fe3O4磁性纳米粒子的磁性相应的趋势一致。
2.6 磁性纳米粒子回收脱脂乳中乳铁蛋白的专一性
两种粒径的磁性纳米粒子从脱脂乳中回收乳铁蛋白的效果见图6。
从图6可以看出,不同粒径的磁性纳米粒子都可以从脱脂乳中回收得到乳铁蛋白,图6A中E1~E3有一条带与乳铁蛋白标准品的位置一致,说明该蛋白为乳铁蛋白,另外还有一些其他蛋白出现,通过灰度分析得知乳铁蛋白大约占洗脱液中的23%。图6B中E4~E6的吸附效果与E1~E3的趋势一致,但是在E4~E6中乳铁蛋白所占的比例明显提高,经灰度分析结果表明,乳铁蛋白大约占洗脱液中的38%。说明粒径小的磁性纳米粒子对乳铁蛋白的吸附效果好。
研究报道,Gao等[21]使用多巴胺作为配体,成功的合成了一种可以回收含6个组氨酸标签的蛋白,表面积大和良好的分散性使得磁性纳米粒子可以增加蛋白质结合能力,提高专一性。由于目标蛋白可以有效地快速递覆盖在磁性纳米粒子表面,这样就减少了总体未被占据的表面吸附非目标蛋白的因此获得了高的特异性。200 r/min获得的Fe3O4磁性纳米粒子修饰Con A后的的平均粒径小,仅为(9.77±0.02)nm,因此,小粒径的磁性纳米粒子被杂蛋白占据的表面比大粒径的少,其吸附效果更好。
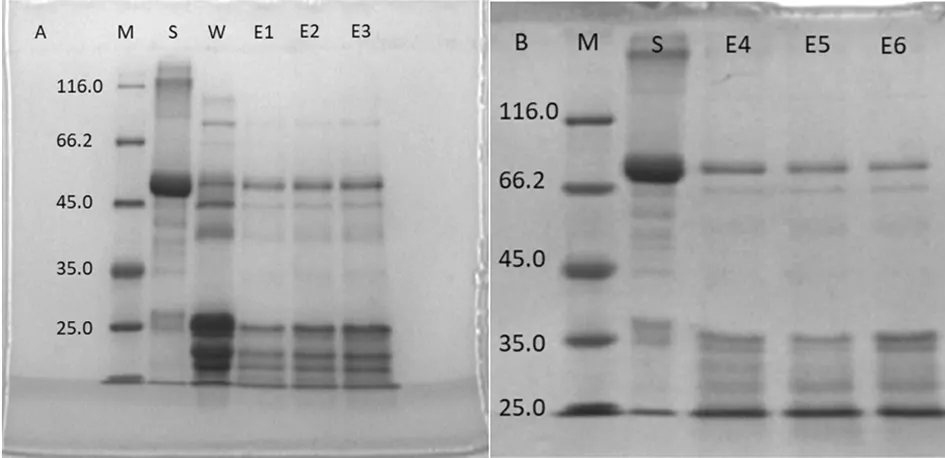
图6 不同磁性纳米粒子从脱脂乳中回收乳铁蛋白的效果Fig.6 The effect of different particle size of magnetic nanoparticles on lactoferrin recovery from skimmed milk
3 结论
以共沉淀法制备磁性纳米粒子,转速为100 r/min获得的磁性纳米粒子形貌不规则、粒径大小不一致;而转速为200 r/min获得的磁性纳米粒子形貌规则、呈现椭球形并且粒径大小均一一致、通过XRD对磁性纳米粒子进行分析发现,磁性纳米粒子具有7个属于Fe3O4的特征峰、通过FT-IR试验结果发现,在579 cm-1位置的对应峰为Fe3O4中的Fe-O键的伸缩振动,判断合成的磁性纳米粒子的晶格为Fe3O4、通过VSM对磁性纳米粒子进行磁强度分析发现,100 r/min和200 r/min获得的磁性纳米粒子的磁强度分别为3.68 emu/g和5.36 emu/g都具有超顺磁性,并且在外加磁场存在的情况下,表现出了良好的磁响应,将Con A修饰到磁性纳米粒子表面以后,粒径小的磁性纳米粒子比粒径大的磁性纳米粒子能更有效地从脱脂乳中回收乳铁蛋白。

