水体中营养盐离子及溶解性有机质对磺胺二甲基嘧啶光解的影响
陈 慧,贾晓晨,李瑞敏,贾青竹
(天津科技大学海洋与环境学院,天津 300457)
抗生素在预防治疗人类和牲畜疾病等方面应用 广泛[1–2];但由于合法监管的缺失,导致抗生素过度使用甚至滥用,所以大量的具有母体和/或中间产物形式的抗生素被排放到污水厂或自然环境中[3–4].然而由于其分子结构的稳定性高,常规活性污泥法处理过程对抗生素的去除效率非常有限[5],导致我国城镇污水厂二级出水中抗生素浓度较高[6],广谱性抗生素如磺胺类药物几乎在所有的水中均能被显著检出,严重威胁水生生物安全并可能损害人类健康[7-10].
光解是水环境中抗生素进行降解和矿化的重要途径[11-12].天然水体组成(如离子、和)、pH 和黄腐酸(FA)等均可能会对抗生素的光解产生影响[13].郑晓冬[14]研究了 Nordic湖中腐殖酸(N-HA)和 Nordic湖中富里酸(N-FA)对三氯生光解的影响,N-FA和 N-HA均显著地抑制了三氯生光解,N-HA主要是通过光屏蔽作用抑制三氯生的光解,而 N-FA 除光屏蔽作用外,还可能通过动态猝灭抑制三氯生的光解.张楠等[15]建立了 pH、光强、温度、丙酮和双氧水对双氯芬酸光解影响的模型.葛林科等[16]通过中心组合实验研究了 Fe3+、、N-HA和 Cl-对沙拉沙星与加替沙星光解的影响,其结果显示 Fe3+、Cl-对氟喹诺酮类药物光解的动力学常数无显著影响,而和HA等均起到了抑制作用.
1 材料与方法
1.1 试剂
SMZ,优级纯,Adamas试剂公司;KH2PO4、KNO3、(NH4)2SO4、K2SO4,分析纯,天津江天化工技术有限公司.
1.2 测定方法
采用高效液相色谱法对 SMZ进行检测,测定条件为:色谱仪器检测波长 268,nm;分离柱为 C18色谱柱(5,µm,4.6,mm×250,mm);流动相V甲醇∶V水=40∶60;温度为室温;流量 1,mL/min;DAD 检测器;进样量10,µL.其定量分析采用外标法.
通过 Waters 2767-3100型色质联用检测紫外光下 SMZ降解过程中的中间产物.检测条件[17]如下:色谱仪器检测波长设置为 254,nm,色谱柱为 Apollo C18 色谱柱(5,µm,4.6,mm×250,mm).流动相为甲醇(A)和超纯水(B).流动相的流量为 1,mL/min,10,µL的进样体积,SMZ保留时间为 6.07,min.采用ESI+/ESI-模式检测;源温度 120,℃,去溶剂气体温度 350,℃;去溶剂气体流量 600,L/h;锥孔气体流量50,L/h;锥孔电压30,V;质荷比(m/z)100~1,500.
1.3 光解实验
光解实验装置如图 1所示[17].SMZ反应液体积为 100,mL,溶液初始质量浓度为 10,mg/L,pH为 5,反应过程均不曝气,光源为紫外灯(波长为 254,nm,25,W),所有实验均重复 3次,实验数据误差均小于0.3%,,本文报道结果是3次实验的平均值.
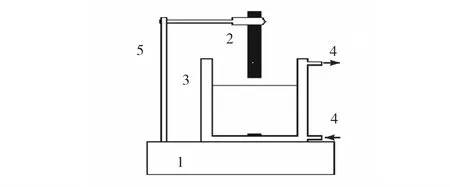
图1 光解反应器Fig. 1 Photolysis reactor
2 结果与讨论
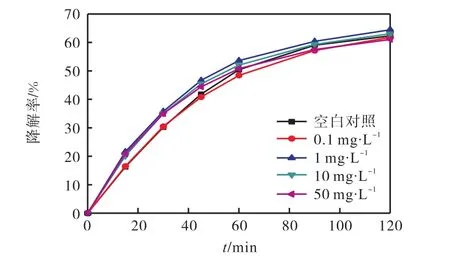
图2 KNO3对SMZ光解的影响Fig. 2 Effect of KNO3 on the photolysis of SMZ
由图 2可知:随着 KNO3质量浓度的增加,SMZ的降解率亦有相应的变化.未加入KNO3时,120,min时 SMZ的降解率为 62.3%,;当 KNO3质量浓度大于1,mg/L时,SMZ降解率随着其质量浓度的增加而减小,KNO3质量浓度为 1,mg/L时,SMZ在光解120,min后降解率提高到 64.5%,;但是当 KNO3质量浓度继续增大为 50,mg/L时,SMZ的降解率稍有降低,光解 120,min后为 61.1%,.光解动力学分析表明,KNO3质量浓度为1,mg/L时,SMZ光解过程中的k 值(ρ=9.930,e-0.010,22,t)为无 KNO3时(ρ=9.983 e-0.009,480,t)的 1.08倍,此时对 SMZ光解的促进作用最明显.
为考察富营养元素 N的不同形态对 SMZ光解的影响,本工作探索了((NH4)2SO4质量浓度分别为 0.1、1、10、50,mg/L)对 SMZ 光解的影响,实验结果如图3所示.
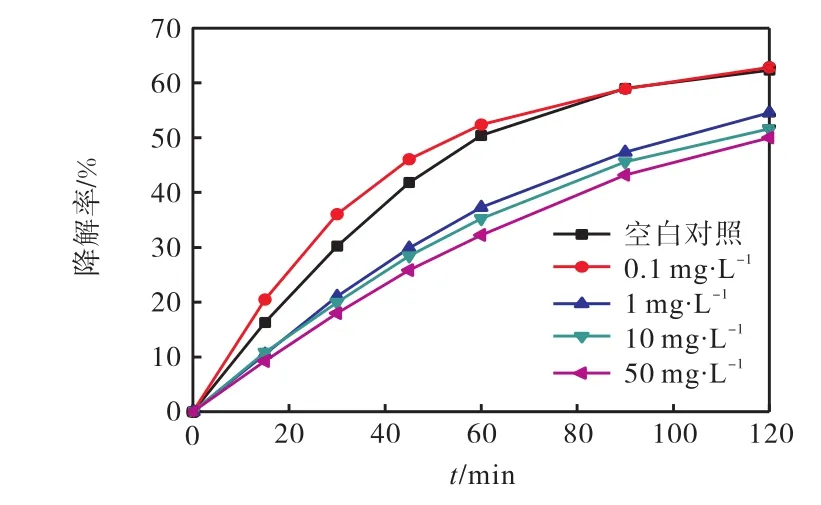
图3 (NH4)2SO4对SMZ光解的影响Fig. 3 Effect of (NH4)2SO4 on the photolysis of SMZ
由图 3可知:(NH4)2SO4对SMZ光解起到了一定的抑制作用,尤其是随着(NH4)2SO4质量浓度的急剧增加,SMZ光解120,min后SMZ的降解率均有所下降.与未添加(NH4)2SO4相比,当(NH4)2SO4质量浓度为1,mg/L时,SMZ光解 120,min后 SMZ的降解率从 62.3%,降低为 54.5%,;当(NH4)2SO4质量浓度继续增大为 50,mg/L时,SMZ光解过程中的 k值(ρ=9.963,e-0.008,761,t)为无(NH4)2SO4时(ρ=9.974 e-0.010,070,t)的0.87倍.
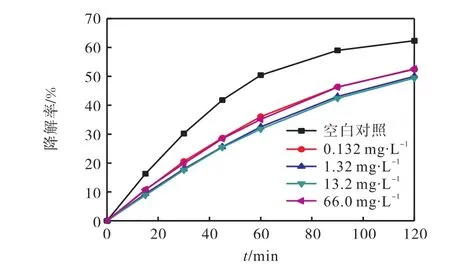
图4 K2SO4对SMZ光解的影响Fig. 4 Effect of K2SO4 on the photolysis of SMZ
磷元素是引起水华和赤潮的主要原因之一.为了研究磷元素对SMZ光解的影响,采用KH2PO4(质量浓度分别为 0.005、0.5、5、20,mg/L)代替水体中的活性磷酸盐进行实验,结果如图5所示.
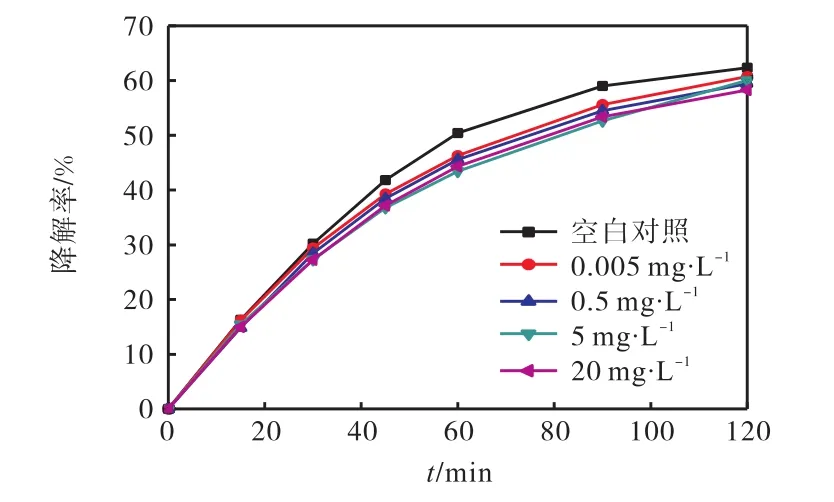
图5 KH2PO4对SMZ光解的影响Fig. 5 Effect of KH2PO4 on the photolysis of SMZ
从图5中可看出:不同含量的KH2PO4均能轻微降低 SMZ光解效率.与未添加 KH2PO4相比,KH2PO4质量浓度为 5,mg/L时,光解 120,min后SMZ的降解率由62.3%,降为59.0%,.
KH2,PO4对 SMZ光解抑制作用的原因可能有两个方面:其一,KH2PO4可吸收一部分光(λ>290,nm),能产生光掩蔽效应导致 SMZ光解被抑制[18];其二,可能成为了 H+和·OH 的清除剂,使溶液中的·OH 减少,同时生成自由基 H2PO4·,该自由基的氧化能力弱于·OH.因此,在 KH2PO4共存条件下,SMZ光解120,min后降解率会有所降低.
2.4 黄腐酸对SMZ光解的影响
为了考察水体中溶解性有机质对有机污染物光解过程的影响,本工作探讨了不同质量浓度黄腐酸对SMZ光解的影响,实验结果如图6所示.
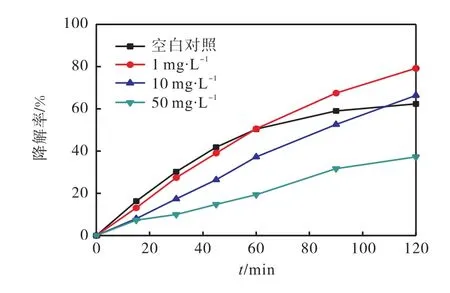
图6 黄腐酸对SMZ光解的影响Fig. 6 Effect of fulvic acid on the photolysis of SMZ
由图 6可知:少量的黄腐酸促进了 SMZ的光解,而大量的黄腐酸抑制其降解.在添加 1,mg/L的黄腐酸和光解120,min后,SMZ降解率为79.1%,,相比不添加黄腐酸情况下,SMZ降解率增加了16.8%.当50,mg/L黄腐酸存在时,SMZ光解120,min后降解率低于40%,.进行动力学分析后得知SMZ的光解符合准一级动力学模型,SMZ光解动力学常数k随着黄腐酸质量浓度的增加先增大后减小(图 7),计算结果表明在高质量浓度黄腐酸共存体系(50,mg/L)中SMZ的光解半衰期相比纯水中的光解半衰期增加了 103.7,min.
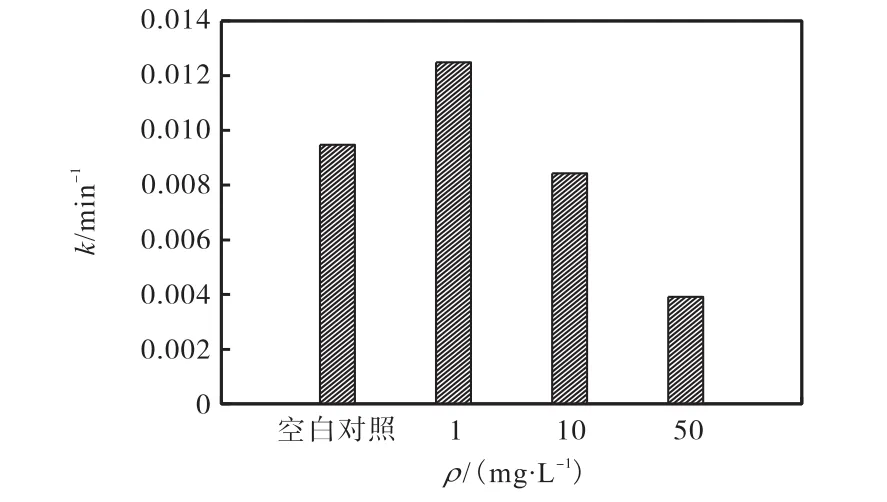
图7 SMZ光解动力学常数与黄腐酸质量浓度的关系图Fig. 7 Plot of photolysis kinetic constants of SMZ with the increasing mass concentration of FA
黄腐酸分子既能吸收光子,又能进行光敏化作用,产生活性分子,这些活性分子有利于SMZ光解,所以低质量浓度黄腐酸的存在能促进 SMZ光解.另一方面,由于黄腐酸的特殊复杂结构,即紫外光区内具有较强吸收峰,因此黄腐酸易与 SMZ竞争光子,抑制 SMZ光解.并且,黄腐酸能捕获活性物质·和·OH[19],从而对SMZ的自敏化起到了抑制作用.
2.5 SMZ光解中间产物的鉴定与分析
图8为SMZ经紫外光解后样品的液相图谱,其中 6.07,min处的出峰物质为 SMZ,其余几处出峰初步怀疑为其光解过程产生的中间产物.SMZ是由苯环(78)、氨基(14)、磺酰基(79)和甲基基团(107)组成,进一步对其进行质谱MS检测.

图8 SMZ光解过程LC扫描图Fig. 8 LC scan of sulfamethazine during photo-degradation process
从质谱结果可以看出,6.07 min时该物质质荷比为 277~279,证明该物质是 SMZ.2.92,min处出峰物质正离子质荷比为 215,这极有可能是 SMZ脱去SO2的产物 C12H14N4.6.73,min处出峰物质正离子质荷比为124,推测其可能是C6H9N3.
综合分析,SMZ的光解机理推导如下:
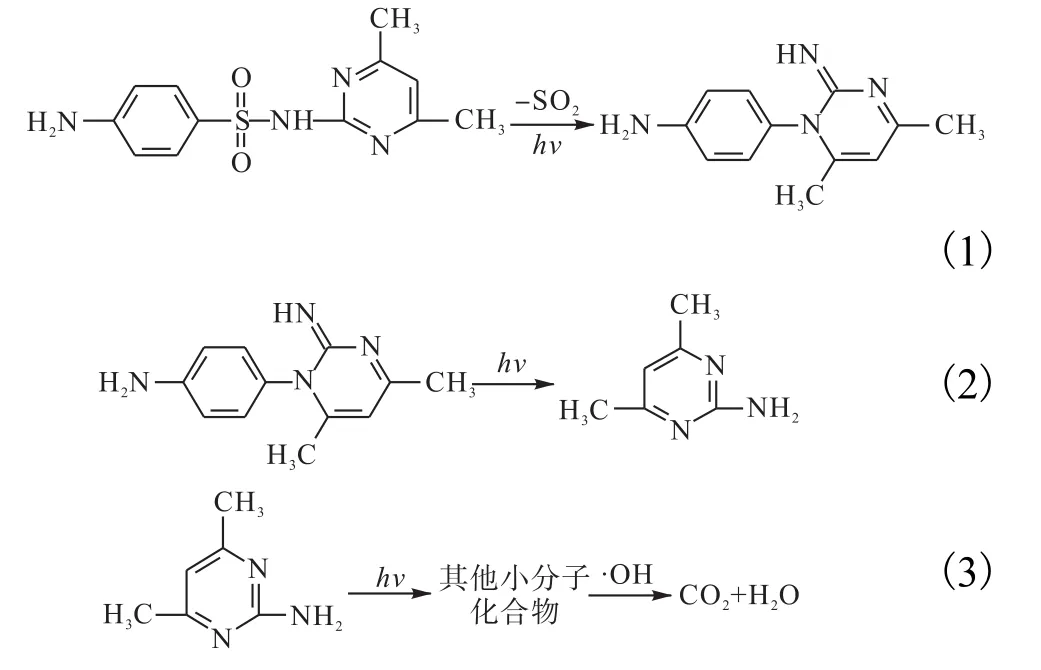
在紫外光下,SMZ先被活化,脱去 SO2生成C12H14N4(反应式(1)),接着 C12H14N4被开链重组形成 C6H9N3(反应式(2)),C6H9N3分解为小分子有机物,继续分解为CO2和H2O(反应式(3)).
3 结 论
在其他溶解性离子或者有机质共存条件下,SMZ在水体中的光解过程符合准一级动力学模型.不同溶解性离子对 SMZ光解动力学过程会产生不同程度的影响.氮元素的不同形态对 SMZ光解的影响稍有差异,其中共存的对SMZ光解影响很小,而共存的对 SMZ光解的影响表现出两面性.抑制 SMZ光解,其中,高质量浓度的抑制作用更显著.水体中溶解性有机质对 SMZ光解的影响具有两面性,低质量浓度黄腐酸会促进 SMZ的光解,高质量浓度黄腐酸则表现出抑制作用.综上,当水体污染富营养化严重时,水体中有机污染物的光解去除过程也受到不同程度的影响.

