前入路腹腔镜在治疗胰腺假性囊肿中的应用(附12例报告)
杨斌,毛根军
(浙江省金华市中心医院 肝胆胰外科,浙江 金华 321000)
胰腺假性囊肿(pancreatic pseudocyst,PPC)是急性重症胰腺炎恢复期或严重胰腺外伤后的常见并发症。75%左右的PPC由急性重症胰腺炎导致,慢性胰腺炎继发PPC的比率为10%~30%左右[1]。当前有关PPC的诊疗指南中认为,当PPC的直径超过6.0 cm大小,持续时间超过6周,假性囊肿自行消失的可能性较小,同时患者出现严重并发症(如胃肠道梗阻、呕吐、贫血、严重营养不良、囊肿内囊液继发感染导致发热和急性弥漫性腹膜炎等)则为外科干预指征。目前临床工作中PPC的手术方式分为囊肿外引流术、囊肿内引流术(囊肿十二指肠吻合术、囊肿空肠Roux-en-Y吻合术、囊肿胃吻合术)和胰体尾部切除术。近年来随着微创技术的发展及器械的改进,外科医师的手术经验积累,临床工作中腹腔镜技术用于治疗PPC的文献报道呈现增多趋势[2-6]。本单位自2010年1月-2015年6月共收治PPC患者12例,12例患者均实施完全前入路腹腔镜下胰腺囊肿胃吻合术,术后恢复良好,术后随访无囊肿复发。现报道如下:
1 资料与方法
1.1 一般资料
本组病例共12例。其中,男9例,女3例,年龄27~62岁,平均年龄38.5岁,本组病例既往均采取保守治疗控制病情。8例患者以进食后上腹部饱胀不适入院,2例患者以进食后呕吐入院,2例患者以腹痛腹胀伴肛门排气减少入院。本组12例病例经彩超、上腹部增强CT、上腹部增强磁共振成像(magnetic resonance imaging,MRI)+磁共振胰胆管造影术(magnetic resonance cholangiophancreatography,MRCP)等证实均存在PPC,同时排除其他胰腺囊性占位性疾病。12例PPC都位于胰体尾部,囊肿直径6.0~10.0 cm,平均7.5 cm,最大10.0 cm×7.0 cm×5.0 cm。本组病例体重下降从4~15 kg不等,平均体重下降7 kg。病因方面,5例为胆源性胰腺炎同时合并胆囊结石,7例考虑高脂血症引起。
1.2 手术方法
1.2.1 术前准备 结合病史、体格检查,腹部彩超、腹部增强CT、腹部增强MRI+MRCP等了解囊肿性质及其周围脏器毗邻关系。部分患者因囊肿和主胰管关系影像学检查上难以确认,5例行经内镜逆行胰胆管造 影(endoscopic retrograde cholangiopancreatography,ERCP)检查。主胰管和囊肿是否相通按D'Egidio分型12例患者均为I型[7]。5例患者同时有胆囊结石病史及慢性胆囊炎相关症状,经患者同意后术中同时行腹腔镜胆囊切除术去除病因。因胰腺周围为消化道脏器,本组所有病例均按消化道手术行术前准备工作(术前禁食、术前留置胃管、肠道准备)。
1.2.2 主要手术步骤 患者常规取仰卧截石位,左季肋部根据情况可适度垫高以方便操作,垫高一般约30°,常规取头高脚低位,主刀站位于患者右侧,第一助手站位主刀对侧,扶镜手站于患者两腿之间,肚脐下侧缘做一10 mm切口为腹腔镜窥视孔,气腹针成功建立气腹后插入10 mm大小的Trocar,常规使用二氧化碳CO2作为气腹,气腹压控制在12~15 mmHg(1 mmHg=0.133 kPa),手术开始前常规腹腔镜探查全腹腔,其他穿刺孔位于左右肋弓下2.0~3.0 cm腋前线处及脐上3.0 cm左右腹直肌外缘水平,其中主操作孔位于脐上3.0 cm右侧腹直肌外缘水平处,Trocar的具体位置术中根据囊肿的大小、部位及术中操作习惯可灵活变动;术中探查发现局部胃壁明显隆起考虑为囊肿压迫所致改变,术中为谨慎考虑,全部患者均行术中超声定位囊肿所在部位与囊肿和脾脏、脾动静脉及胃壁的毗邻关系;将隆起处所在处胃前壁使用电凝切开处理(图1),进一步置入腹腔镜检查胃腔,发现前壁切开处相对应胃后壁较周围正常胃壁明显水肿增厚,腔镜下在该处胃后壁行穿刺处理,抽出暗褐色液体,并送穿刺液淀粉酶测定,进一步证实胰腺囊肿所在部位;将穿刺处进一步电凝扩大至1.0 cm左右,将囊液及囊肿内坏死组织进一步清除干净,通过胃前壁置入一次性切割闭合器,闭合器钉砧一侧置入囊肿侧,另外一侧置入胃腔侧,闭合时从胃壁向囊肿方向关闭激发,完成囊肿胃吻合(图2)。腹腔镜进一步检查吻合情况,将脱落钉清理,检查吻合口情况,吻合口创面如有出血电凝或缝合止血,将胃前壁关闭处理(切割闭合器或缝合关闭处理)(图3);如有胆囊结石,进一步加行胆囊切除;检查腹腔内无明显胃瘘、胰瘘、胆瘘及消化液外渗情况,使用温盐水冲洗腹腔,小纱条擦拭腹腔有无异常颜色液体外渗,根据术中情况,放置腹腔引流管1或2根,引流管从操作孔内引出并予固定,再次检查腹腔无明显异常情况,关闭气腹,皮下缝合切口。
1.3 术后处理及随访
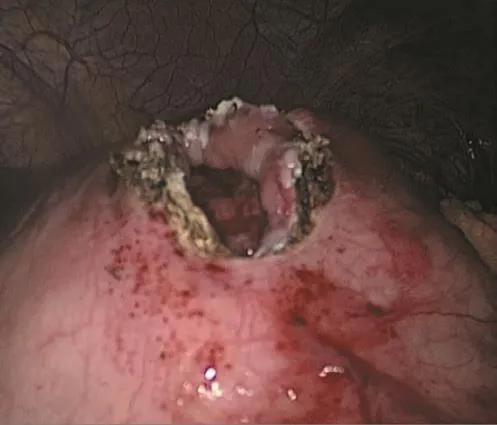
图1 胃前壁切开Fig.1 Cut the anterior wall of stomach
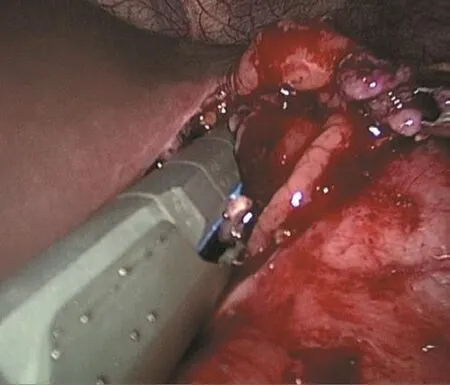
图2 囊肿胃后壁吻合Fig.2 Posterior gastric wall anastomosis of cysts
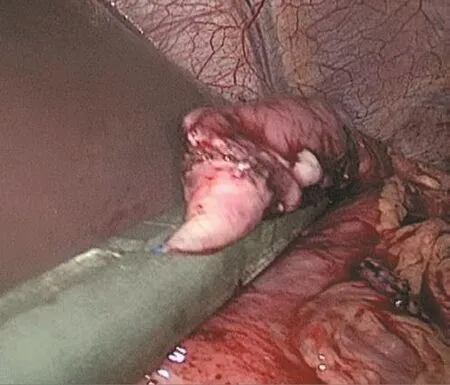
图3 胃前壁关闭Fig.3 Close the anterior wall of stomach
术后常规抗炎和肠外营养支持,术后给予奥曲肽针0.1 mg皮下注射,每8 h一次,共计3 d,术后第4天恢复流质饮食;术后第6天拔除腹腔引流管,术后第8天出院。术后1个月、3个月、6个月和1年复查腹部B超、血糖及测量体重,其中术后6个月一并复查腹部CT。
2 结果
本组所有患者手术均成功实施前入路腹腔镜胰腺囊肿胃吻合手术,无中转完成手术。本组病例手术时间(70.0±15.0)min,出血量(70.0±18.0)ml,术后(1.0±0.0)d下床活动,术后(2.5±0.5)d肛门恢复排气,术后第4天进流质饮食。12例患者均顺利恢复,无胰漏、出血和胃瘘等手术相关并发症发生。术后平均住院时间为(8.0±1.5)d。术后随访1年,本组患者术后均恢复顺利,无胰腺炎、无囊肿复发、无糖尿病及肠梗阻等长期并发症发生,术后体重较术前平均增加(6.0±1.0)kg。
3 讨论
PPC的外科治疗大体上分为引流术和切除术两大类。患者既往一般有多次急性胰腺炎发作病史,胰腺炎的炎症反应往往较为强烈,这就导致了上腹部的结构紊乱及粘连。PPC大多数位于胰腺体尾部,由于解剖学的关系,胰腺尾部往往紧贴脾脏,在临床实践中发现,行脾脏的切除手术中往往都会造成胰尾部的损伤,同样的道理,在胰腺囊肿切除过程中也有可能导致脾脏的损伤。脾脏是人体内比较脆弱的器官,手术操作容易导致脾脏的副损伤及出血,手术过程中被迫行脾脏切除时有发生。脾脏作为人体的重要免疫器官,近年来得益于脾脏基础理论及外科理论的不断发展,生理学家及外科医师对脾脏的生理功能越来越重视,脾脏切除后容易引起发热及门静脉系统血栓,严重者导致重要脏器栓塞或导致功能不全严重影响患者的生活质量,少部分患者会并发严重感染,有鉴于此目前大多数学者倾向保留脾脏功能。目前保脾的腹腔镜下胰体尾切除手术也逐步开展,近年来有更多相关报道出来[8-11]。但保留脾脏的腹腔镜下胰体尾切除术,手术本身难度大,操作困难,对外科医师的要求更高,在临床实践中,能够掌握保留脾脏的腹腔镜下胰体尾切除手术的外科医师并不多。同时在行胰腺体尾部切除术中,虽然囊肿也一起切除了,但部分胰腺组织仍被不可避免的切除,胰岛细胞在胰腺体尾部的分布密度是最密的。因此,手术后仍有少部分患者并发糖尿病,对患者的生活质量造成不良影响,其中对年轻患者影响更甚。外引流目前临床上已很少采用。由于切除术及外引流术的不足,胰腺囊肿的内引流治疗的地位就显得更加重要了,目前已成为PPC的主流治疗方案。
近年来随着腹腔镜技术的不断进步,操作器械的不断改进,外科医师的手术经验积累,同时由于腹腔镜技术具有创伤更小、并发症更少和术后恢复更快等较为明显的优势,腹腔镜微创技术治疗PPC目前已成为主流的手术方式,而传统开腹手术使用的越来越少。国外的这方面早在90年代就有相关报道,相关的报道提示腹腔镜治疗效果理想[12-14]。
国内方面治疗PPC临床上目前最常用的手术方式为腹腔镜下PPC空肠Roux-en-Y吻合术,这方面的报道近年来较多[15-18]。本手术操作步骤多,术中需要将上段空肠进行离断,术中同时行囊肿空肠吻合和空肠侧侧吻合,手术导致2个吻合口产生,增加了手术复杂性,同时也增加了手术难度,延长手术时间,增加医疗费用支出。该手术方式对消化道进行了一定程度的重建,改变了消化道走行,不可避免的会影响到患者的消化功能。同时吻合口越多导致消化道漏、消化道出血等并发症的概率就更多。微创外科的真正意义不应该停留在追求体表切口的微创化,更应该着力于手术治疗本身的微创化。如何使用科学的治疗方法达到对患者心理生理创伤影响的最小化和脏器功能的最大程度的保护,这才是微创外科医师努力和奋斗的方向。近年来加速康复外科(enhanced recovery after surgery,ERAS)理念在外科引流中的应用越来越广泛[19-20],简单的手术能够解决的问题不能使用复杂的手术,在临床工作中,外科医师要不断总结不断反思不断创新,如何用更微创的技术让患者获益是外科医师工作的不懈追求。PPC一般位于胃后方,胃壁往往是囊肿壁的一部分,采用囊肿胃吻合术,最符合人体生理及解剖,不影响其他脏器,不需要改变消化道走行,对人体的创伤可以达到最小化,有广阔的发展空间和临床应用价值。
本文重点讨论前入路腹腔镜PPC胃吻合术,本组病例中,笔者所采用的均是囊肿胃后壁吻合,入路采用前入路方法,术中笔者是将囊肿所在处胃前壁打开,行胃后壁穿刺证实胰腺囊肿所在位置后,将胃后壁连同囊肿壁部分切开,将囊肿内液体及坏死组织清理干净后,使用切割闭合器钉砧一侧置入胃腔,另一侧置入囊肿内,将切割闭合器激发行囊肿胃吻合术,胃前壁切开处使用切割闭合器关闭或缝合关闭均可。由于囊肿胃吻合口径大,本组病例中没有出现食物残留在囊肿内继发感染及出血的相关并发症发生。本组所有患者术后随访囊肿均消失,手术效果良好。在术后早期,胃管留置时间一般持续3~5 d左右,恢复流质饮食时间一般在手术4 d以后为宜,术后恢复期,常规使用小剂量奥曲肽来抑制胰腺分泌,同时也可减少消化液分泌,可以减轻消化道的液体负担,有效地促进吻合口的愈合。在本组患者的手术过程中,笔者发现部分患者上腹部仍有较为致密的粘连,同时由于营养不良及贫血等情况,上腹部的脏器组织往往有一定程度的水肿,解剖层次欠清晰,术中如果要将胰腺囊肿进行解剖显露,往往需要解剖胃结肠韧带,而在手术过程中不可避免的会导致出血等情况,严重者有可能导致其他脏器的副损伤。胰腺属于后腹膜脏器,前方为胃,后方为后腹膜组织,上腹部重要血管以胰腺为中心分布,故胰腺手术是上腹部最困难的手术操作,对外科医师的技术水平要求高,特别是行胰腺囊肿切除,解剖操作更加困难,尤其是术中保留脾脏更是难上加难。前入路腹腔镜胰腺囊肿胃吻合术,术中不需要进行解剖显露胰腺,不解剖胰腺就不会有手术导致的并发症发生,术中保留脾脏简单可行,脏器功能的保护往往是术中最困难的。本术式能够最大程度地保护脏器功能。前入路手术操作步骤更少,手术时间更短,由于术中使用切割闭合器进行囊肿胃吻合,吻合口直径更大,可达4~6 cm左右,较使用常规弯管吻合器形成的吻合口直径更大,避免了术后吻合口的狭窄及相关并发症。同时因为胃的血供非常丰富,手术本身不需要离断胃的任何血管,术中行胃前壁的关闭可靠,术后无1例胃瘘发生。本组病例中,5例患者同时行胆囊切除术去除胆囊结石病因,一次手术解决病因和胰腺囊肿,较分次手术费用更少,患者痛苦更少,避免了患者的再次住院,节省医疗费用的同时也为国家医保减少支出。本组病例中笔者使用常规器械,不需增加特殊器械,不增加额外的医疗成本和费用,该类手术同样适合在贫困地区和基层医院开展。
前入路腹腔镜手术治疗PPC,手术入路选择合理,主要的操作步骤简单,术中不需要行胰腺的解剖显露,术中轻松保留脾脏,对外科医师的操作水平相对要求不高,外科医师容易掌握该手术,手术学习曲线短,基层医院的外科医师也可以很好地掌握该手术,是一种简单、有效、实用性很高的手术方式,值得在临床上广泛推广。

