实验室克仑特罗残留检测方法比对
(北京市朝阳区动物疫病预防控制中心,北京 100018)
2006年9月17日,上海连续发生“瘦肉精”食物中毒事故,波及全市9个区、300多人。
2011年3月15日“双汇瘦肉精”事件曝光至23日18时,查获含“瘦肉精”饲料若干批次。
“瘦肉精”是一类动物用药,而不是一种特定的物质,是指能够促进瘦肉生长的饲料添加剂,有数种药物被称为瘦肉精,例如盐酸克仑特罗、莱克多巴胺、沙丁胺醇等能够实现这种功能的物质,又叫作β-兴奋剂的药物,将瘦肉精添加于饲料中,可以增加动物的瘦肉量、抑制肥肉生长、减少饲料使用、使肉品提早上市、降低成本,但在组织和内脏中残留量很大。
我中心实验室肩负着让全区老百姓吃上“放心肉”的重要责任,作为“菜篮子工程”的第一道安全防线,我们有必要努力追求工作的质量与效率,自从2009年开展了克仑特罗的实验室初筛检测,经过比对与筛选,2012年复认证时最终选定了北京维德维康生物技术有限公司生产的克仑特罗快速检测卡(Ⅱ型)和莱克多巴胺酶联免疫试剂盒(三合一)。并于2013年底购置一台液相色谱串联质谱仪(岛津20A+AB的API5000),积极学习与开展,在2015年6月通过实验室计量认证成功扩项,使我实验室实现了克仑特罗药物残留检测从初筛到定性确证的整套流程。日常监测中时有出现的阳性样品,使我统计了检测数据进行比对,并自己设计了实验计划,对目前可以开展的三项不同的检测手段进行准确性和可信度比较,从我实验室角度分析了几种检测手段临床使用的可行性和适用性,以及给出的检测结果的临床参考意义。
1 检测方法详解
1.1 胶体金免疫层析法
1.1.1 原理
利用竞争法胶体金免疫层析技术,检测卡含有被事先固定于硝酸纤维素膜测试区(T)的抗原和控制区(C)的Ⅱ抗,以及固定于结合垫上的金标抗体。检测液中的Clen与金标垫上的金标抗体结合形成复合物,若Clen在检测液中浓度低于灵敏度值,未结合的金标抗体流到T区时,被固定在膜上的Clen-BSA偶联物结合,逐渐凝集成一条可见的T线;若Clen浓度高于灵敏度值,金标抗体全部形成复合物,不会再与T线处Clen-BSA偶联物结合形成可见T线。未固定的复合物流过T区被C区的二抗捕获并形成可见的C线。C线出现则表明免疫层析发生,即试纸有效。
以我实验室使用的北京维德维康生物技术有限公司生产的克仑特罗快速检测卡(Ⅱ型)为例。
1.1.2 检测步骤
(1)使用前将试剂板和待检样本溶液恢复至室温。
(2)取5g匀浆去脂肉样于50mL离心管中,放入沸水中加热10min,用微量移液器或滴管取出管中液体移至干净离心管中,冷却至室温(注意:样品温度应控制在20±5℃!)。
(3)取出检测卡,平放于桌面,使用本产品自带的滴管,吸取离心管中的上清液加3~4滴于样品孔中。
(4)加样后3~5min,观察显色区,判断结果,其他时间判断无效。
结果判读:阳性(+):仅质控区(C)出现一条紫红色条带。在测试区(T)内无紫红色条带出现。
阴性(-):两条紫红色条带出现。一条位于测试区(T)内,另一条位于质控区(C)内。
无效:质控区(C)未出现紫红色条带,无论测试区(T)内有无紫红色条带出现,都提示测试失败或试纸已失效。
1.2 酶联免疫吸附法(ELISA)
1.2.1 原理
利用免疫学抗原抗体特异性结合和酶的高效催化作用,通过化学方法将植物辣根过氧化物酶(HRP)与克仑特罗(CL)结合,形成酶偶联克仑特罗。将固相载体上已包被的抗体与特异性的抗克仑特罗抗体结合,然后加入待测克仑特罗和酶偶联克仑特罗,它们竞争性与克仑特罗抗体结合,洗涤后加底物,根据有色物的变化计量待测克仑特罗量。若待测克仑特罗多,则被结合的酶偶联克仑特罗少,有色物量就少。用目测法或比色法测定样品中的克仑特罗含量,比色的最佳波长为450 nm,参比波长应大于600 nm。
以我实验室使用的北京维德维康生物技术有限公司生产的莱克多巴胺酶联免疫试剂盒(三合一)为例。
1.2.2 检测步骤
(1)试剂
①组织稀释液:称取1g三氯乙酸,加入100ml去离子水充分溶解。
②1M氢氧化钠溶液:称取4g氢氧化钠加入去离子水溶解并定容至100ml。
③0.5M氢氧化钠溶液:称取2g氢氧化钠加入去离子水溶解并定容至100ml。
④0.1M盐酸溶液:量取0.86ml浓盐酸并用去离子水定容至100ml。
⑤洗涤工作液:用去离子水按1份浓缩洗涤液+19份去离子水稀释。
(2)样品前处理
①准确称取2±0.01g匀质后的样品于50ml离心管中;
②加入3mL洗涤工作液,再加3ml组织稀释液,高速涡旋1min;
③离心机4000g以上离心5min;
④取1ml中间层清液于新的离心管中(注意:避免取到上、下层固体,否则影响检测结果!);
⑤加入40µl0.5M氢氧化钠溶液,涡旋10s混匀;
⑥离心机4000g以上离心5min;
⑦取20µl样液进行检测。
(3)检测
将所需的酶标板条插入酶标板架上,并记录下各标准品和样品的位置;
将40µl各标准品工作液分别加入对应的标准品孔中;
先将20µl样品稀释液加入样品孔中,再加入20µl待测样品液;
配制酶标记物工作液:按1份酶标记物浓缩液+10份酶标记物稀释液的体积比混合,轻柔混匀。室温(25±2℃)平衡20~30min(注意:操作中应严格控制该步骤时间,即工作液平衡20~30min后立即使用!!);
在每孔中加入60µl酶标记物工作液;
盖好盖板膜,轻轻振荡10s,充分混匀,室温(25±2℃)避光反应30min;
揭开盖板膜,倒掉板孔中液体,每孔加入260µl洗涤工作液,充分洗涤4次,每次浸泡15~30s;
倒掉板孔中液体,将酶标板倒置于吸水纸上,拍干;
立即在每孔中加入100µl底物A、B混合液(注意:底物A液、底物B液按体积1:1混合,混合液在5min内使用,避免使用金属盛装、搅拌试剂!);
盖好盖板膜,轻轻振荡酶标板10s,充分混匀,室温(25±2℃)避光反应15~20min;
揭开盖板膜,板孔中加入50µL终止液,轻轻振荡酶标板10s,充分混匀;
用酶标仪在双波长450nm、630nm下检测吸光度,在5min内读取检测数据。
1.3 液相色谱-质谱/质谱法(HPLC-MS/MS)
1.3.1 外标法
原理:
试样中的残留药物经酶解,用高氯酸调pH值后高速离心沉淀蛋白,上清液调pH值后分别用乙酸乙酯和叔丁基甲醚提取,再用MCX固相萃取柱净化,液相色谱-串联质谱法测定。
以我实验室认证的《农业部1025号公告-18-2008动物源性食品中β-受体激动剂残留检测液相色谱-串联质谱法》为例。该检测方法为外标法。
本标准适用于猪肝、猪肉、牛奶和鸡蛋中克仑特罗、莱克多巴胺、沙丁胺醇、特布他林等9种β-受体激动剂单个或混合物残留量的检测。
1.3.2 检测步骤
(1)样品的制备:
取适量新鲜或冷冻的猪肉,绞碎并匀质,储存于-20℃以下备用。
(2)制备试料:
取匀质的供试料品作为供试试料;
取匀质的空白样品作为空白试料;
取匀质的空白样品,添加适宜浓度的标准工作液作为空白添加试料。
(3)酶解:
准确称取匀浆样品2.00g于50mL离心管内,加入0.2mol/L乙酸铵溶液(pH=5.2)8.0ml,再加入β-盐酸葡萄糖醛苷酶40µl,涡旋混匀,于37℃避光恒温振荡16h。
(4)提取:
酶解后放置至室温,涡旋混匀,10000r/min离心10min,转移上清液于另一50ml离心管中,加入高氯酸溶液5mL,涡旋混匀,用高氯酸调pH至1.0±0.2,10000r/min离心10min,转移上清液于另一50ml离心管中。用氢氧化钠溶液调pH至9.5±0.2,加入乙酸乙酯15ml,涡旋混匀,振荡10min,5000r/min离心5min,取上层有机相至另一离心管中,再在下层水相中加入叔丁基甲醚10mL,涡旋混匀振荡10min,5000r/min离心5min,合并有机相,50℃平行蒸发至干,用甲酸水溶液5mL溶解,备用。
(5)净化:
MCX固相萃取柱依次用甲醇、2%甲酸水各3mL活化,取备用液全部过柱,再依次用2%甲酸水、甲醇各3mL淋洗,抽干,用3%氨水甲醇2.5ml洗脱,在50℃下氮气吹干,残留物用甲醇+0.1%甲酸溶液(10+90,V/V)0.2ml溶解,涡旋混匀,样液经0.2µm针孔过滤器过滤后供液相色谱-串联质谱测定。
(6)液相色谱-串联质谱条件:
色谱柱:BEH C18柱,50 mm×2.1mm(i.d.),粒度1.7µm。
流动相:A相:0.1%甲酸乙腈溶液;B相:0.1%甲酸水溶液。
梯度洗脱:0~2min,维持4%A;2-12min,4%A线性变化至60%A;12~12.1min,60%A线性变化至4%A;12.1~16min,维持4%A。
流速:0.3ml/min。
进样量:10µl。
柱温:30℃。
离子源:电喷雾ESI正离子。
扫描方式:多反应监测MRM。然后以30℃/min升至260℃,保持1min,再以20℃/min升至280℃,保持2min,直至样品的组分全部流出。
监测离子对:克仑特罗m/z 277.1-202.8(定量离子)、277.1-258.9(定性离子);
(7)质谱分析:在上述工作条件下,通过仪器工作软件绘制标准曲线,以色谱峰面积定量。
(8)液相色谱-串联质谱确证:
取试料溶液和空白添加标准溶液,做单点或多点校准,外标法计算,即得。试料溶液及空白添加标准溶液中目标化合物的峰面积均应在仪器检测的线性范围之内。试料溶液中的离子相对丰度与空白添加标准溶液中的离子相对丰度相比,符合允许偏差范围,方可确定为同一物质。
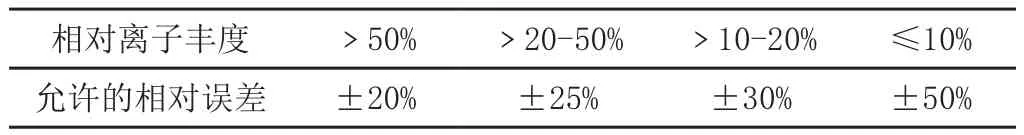
相对离子丰度 >50% >20-50% >10-20% ≤10%允许的相对误差 ±20% ±25% ±30% ±50%
(9)准确度:本方法在0.25µg/kg~2µg/kg添加浓度范围内,用空白添加校准校正,其回收率范围为70%~120%。
(10)结果判定:
β-受体激动剂液相色谱-串联质谱检测法的方法检出限为0.25µg/kg,定量限为0.5µg/kg,判定检测结果大于0.5µg/kg时为阳性。
1.4 内标法
1.4.1 原理
试样中的残留药物经酶解,用高氯酸调节pH值,沉淀蛋白后高速离心,上清液用异丙醇-乙酸乙酯提取,再用阳离子交换柱净化,液相色谱-串联质谱法测定,内标法定量。
以我实验室使用的《GB/T 22286-2008动物源性食品中多种β-受体激动剂残留量的测定液相色谱串联质谱法》为例。该检测方法为内标法。
本标准适用于猪肝和猪肉中克仑特罗、莱克多巴胺、沙丁胺醇、特布他林等11种β-受体激动剂残留量的检测。
1.4.2 检测步骤
参照外标法检测步骤,仅区别于外标法检测步骤2.4提取之前添加100µl的10ng/ml的内标工作液于待测样品中。
2 检测结果比对
2.1 日常监测数据比对
从2015年8月至2017年3月,快速检测卡初筛检测2260份畜禽组织样品,阳性检出52份;ELISA试剂盒检测1080份重合畜禽组织样品(包含初筛52份可疑样品),阳性检出32份;液相色谱串联质谱法检测185份重合畜禽组织样品(包含初筛52份可疑样品),阳性检出31份。
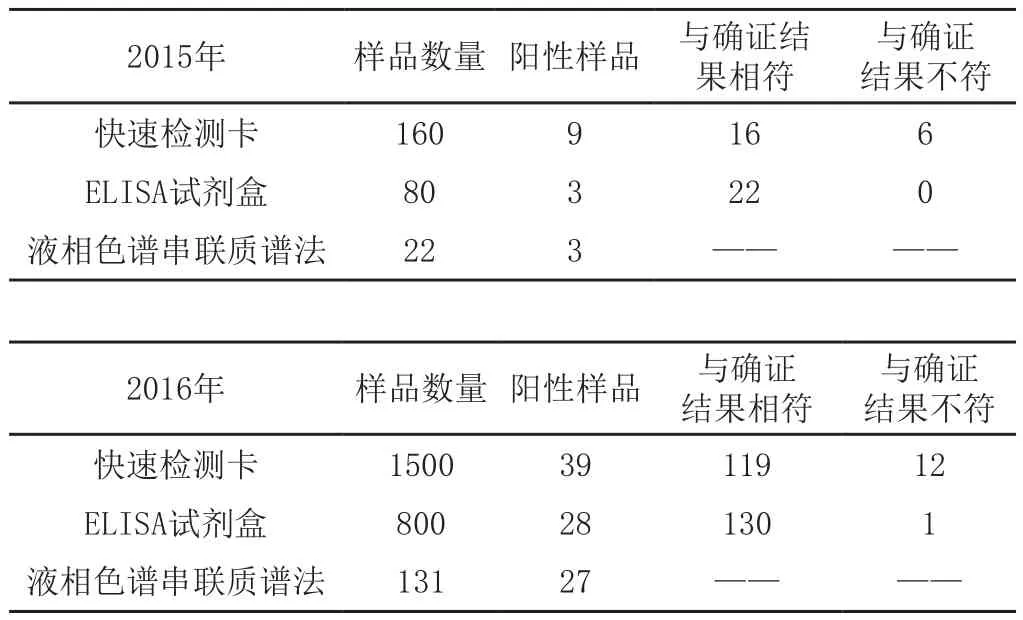
与确证结果不符快速检测卡 160 9 16 6 ELISA试剂盒 80 3 22 0液相色谱串联质谱法 22 3 —— ——2015年 样品数量 阳性样品 与确证结果相符与确证结果不符快速检测卡 1500 39 119 12 ELISA试剂盒 800 28 130 1液相色谱串联质谱法 131 27 —— ——2016年 样品数量 阳性样品 与确证结果相符
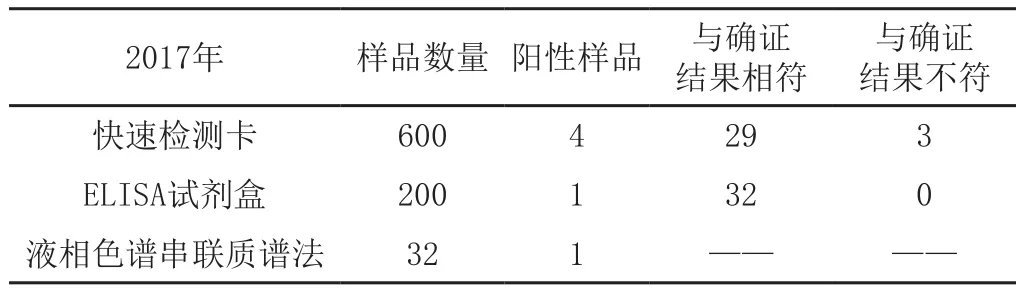
2017年 样品数量 阳性样品 与确证结果相符与确证结果不符快速检测卡 600 4 29 3 ELISA试剂盒 200 1 32 0液相色谱串联质谱法 32 1 —— ——
2.2 实验设计数据比对
运用三种检测手段,对1倍检出限添加,2倍检出限添加,5倍检出限添加,10倍最高检出限添加结果进行比对。
2.3 优化确证方法数据比对
3 数据比对结论
3.1 日常监测数据比对结论
经过三年对日常监测数据的统计分析,快速检测卡初筛检测阳性检出率为2.3%,与定量确证结果符合率为59.6%;ELISA试剂盒检测阳性检出率为2.9%,与定量确证结果符合率为99.5%;快速检测卡初筛与ELISA试剂盒检测结果符合率为61.5%。据此可以看出,快速检测卡的假阳性率比较高,基本不会疏漏阳性样品,但操作简单,日常监测中可以作为有效的初筛手段;ELISA试剂盒检测准确率较高,经过方法认证后可以作为日常监测的主要检测手段;液相色谱串联质谱检测法是目前我实验室具有的最终确证手段,可以达到准确定量的目的,但检测过程比较烦琐,日常进行合理的质量控制,对可疑样品进行确证即可。
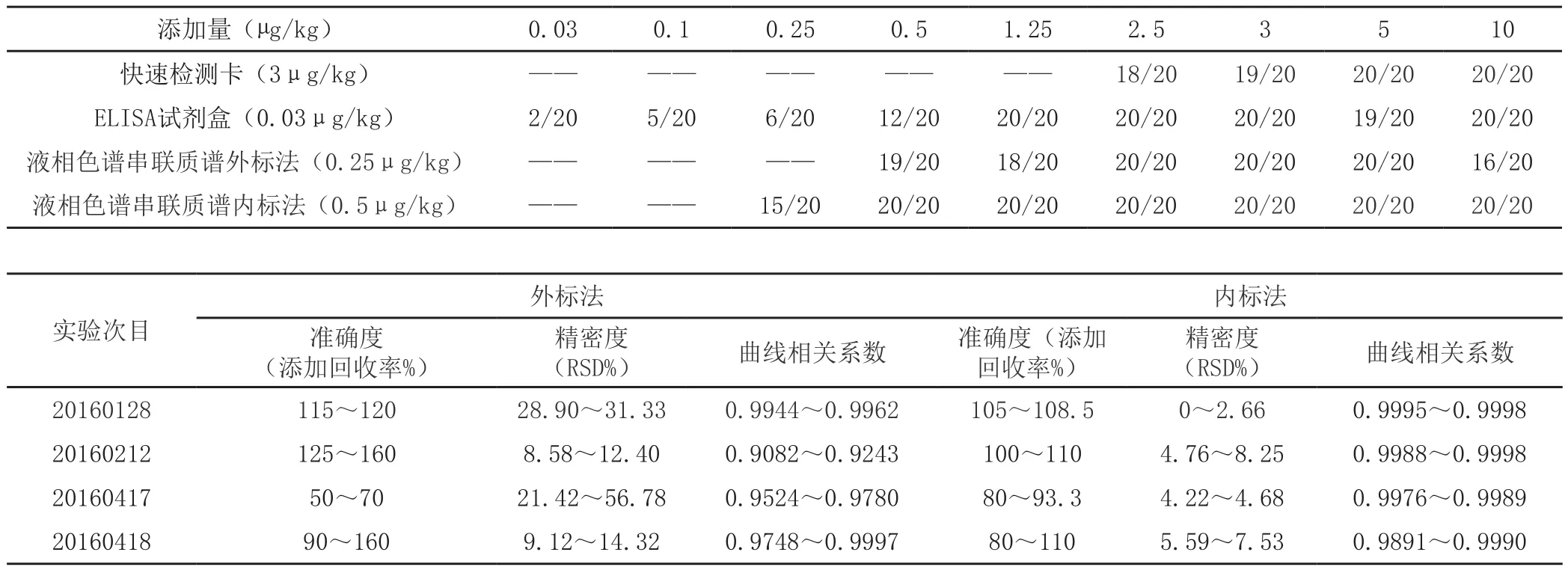
添加量(μg/kg) 0.03 0.1 0.25 0.5 1.25 2.5 3 5 10快速检测卡(3μg/kg) —— —— —— —— —— 18/20 19/20 20/20 20/20 ELISA试剂盒(0.03μg/kg) 2/20 5/20 6/20 12/20 20/20 20/20 20/20 19/20 20/20液相色谱串联质谱外标法(0.25μg/kg) —— —— —— 19/20 18/20 20/20 20/20 20/20 16/20液相色谱串联质谱内标法(0.5μg/kg) —— —— 15/20 20/20 20/20 20/20 20/20 20/20 20/20外标法实验次目内标法准确度(添加回收率%)(RSD%)曲线相关系数准确度(添加回收率%)精密度精密度(RSD%) 曲线相关系数20160128 115~120 28.90~31.33 0.9944~0.9962 105~108.5 0~2.66 0.9995~0.9998 20160212 125~160 8.58~12.40 0.9082~0.9243 100~110 4.76~8.25 0.9988~0.9998 20160417 50~70 21.42~56.78 0.9524~0.9780 80~93.3 4.22~4.68 0.9976~0.9989 20160418 90~160 9.12~14.32 0.9748~0.9997 80~110 5.59~7.53 0.9891~0.9990
3.2 实验设计数据比对结论
经过对520份添加样品进行4种不同方法,不同添加浓度区间进行比对。快速检测卡初筛检测符合率为98.3%,ELISA试剂盒检测符合率为68.9%,液相色谱串联质谱外标法检测符合率为94.2%,液相色谱串联质谱内标法检测符合率为100%。据此可以看出,可能由于技术手段的原因,ELISA试剂盒检测无法达到说明书推荐的检出限,其余各种检测方法在推荐检测区间的检测结果准确率非常高,临床实践运用中毋庸置疑。
3.3 优化确证方法数据比对结论
通过多次实验结果准确度和精密度的比对,可以清楚地判断β-受体激动剂的液相色谱-串联质谱检测的内标法优于外标法。内标法灵敏度高,定性准确,可以更有效地保证准确性的稳定性,精密度的一致性,同时保证校正曲线的相关系数达到实验的要求,在一定程度上保证实验有效,出具结果准确,因此,我们在临床实验中推荐将β-受体激动剂的液相色谱串联质谱检测外标法改进为内标法。
4 结语
通过实验设计数据和日常监测数据综合比对结果我们发现,ELISA试剂盒检测我中心实验室可操作检出限需要提高到0.5µg/kg,说明日常监测出的可疑阳性样品中克仑特罗残留量一般高于该数值。而想真正达到较低的检出限水平,目前我实验室可操作的最好方法就是液相色谱串联质谱检测内标法。
目前,HPLC,GC/MS,CE方法对β-兴奋剂的检出限均在0.5µg/kg左右,并且检测过程耗时长,必须由专业人员操作,所用仪器价格昂贵,不能进行现场检测。而ELISA法检出限可在0.03µg/kg,但也存在假阳性的问题,也不能现场检测。如果能找到一种检测耗时短、准确度高、灵敏度高、自动化水平高,无须专业人员操作的检测方法将具有广阔的应用前景[3]。

