改性生物炭对水体中头孢噻肟的吸附机制
吴鸿伟,陈 萌,黄贤金 ,苏宗杰,孙泰龙,谭晓燕,冯启言 (.枣庄学院化学化工与材料科学学院,山东 枣庄 27760;2.中国矿业大学环境与测绘学院,江苏 徐州 226;3.中国矿业大学低碳能源研究院,江苏 徐州 226)
我国是抗生素生产和消费大国,2013年我国抗生素产量为24.8万t,总消费量约为16万t[1].头孢噻肟(CFX)是 β-内酰胺类抗生素,因其价格便宜,疗效好,广泛的应用于畜牧,水产及非法食物保鲜等行业[2].由于CFX的大量使用及处理不当导致环境基质中残留检出率较高[3],严重威胁生态安全,引起了社会广泛关注[4].CFX的去除方法主要有还原降解[5]、光电催化法[6]、吸附法[7]、芬顿氧化法[8]等.吸附法由于成本低廉、操作简单,在水处理中被广泛应用.
生物炭是一种将含碳丰富的生物质在无氧或缺氧的条件下低温热解所得的多孔芳香化产物[9].农业废弃物、木屑、城市污泥、动物粪便等其他含炭固废均可以制备生物炭[10].生物炭具有成本低廉,原料来源广泛,活性官能团丰富等优点,是一种新型环境友好材料,广泛的应用于污染物治理[11].然而,由于生物炭热解温度较低(<700℃)[12],孔道不丰富,吸附能力有限[13],因此需要进一步改性制备改性生物炭(MB)以增加其孔容、比表面积和官能团数量.本实验采用浸渍方法制备酸、碱及氨水等改性生物炭,并用以去除水体中CFX.采用红外光谱、扫描电镜、比表面积测定仪及元素分析仪分析表征生物炭表面形貌和组成.同时,考察体系的温度、pH 值、吸附剂使用量及污染物初始浓度等对吸附率的影响并探讨了其吸附机理.
1 实验方法
1.1 实验试剂
CFX 标准品(环境保护部标准样品研究所),氢氧化钠、硫酸、氨水、醋酸及氯化钠(分析纯,国药集团化学试剂有限公司),甲醇(色谱纯,国药集团化学试剂有限公司).生物炭购于安徽易能生物能源有限公司(厌氧条件下 500℃热解木屑制得),配溶液用水为超纯水.
1.2 实验仪器
恒温振荡箱(ZD-85,常州国华仪器有限公司),高效液相色谱(1260,美国 Agilent公司),电子天平(FA1004N,上海精密科学仪器有限公司).
1.3 改性生物炭制备
称取洗净并干燥的初始生物碳(OB) 40g,按照1:10(W/V)的比例分别加入3mol/L NaOH溶液、10%H2SO4(V/V)和5%氨水(V/V),60℃搅拌2h,过滤并用大量去离子水洗至近中性,100℃干燥 12h,保存备用,分别记作BC-NaOH,BC-H2SO4和BC-NH3[14].
1.4 样品表征
采用元素分析仪(EA, Vario Macro, Elementar公司,德国)测试各生物炭元素含量,测量模式为 CHN,动态燃烧.采用扫描电镜(SEM,Quanta TM250,FEI公司,美国)表征样品表面形貌.采用表面积测定仪(BET,Micromeritics ASAP 2460,麦克默瑞提克仪器有限公司,美国)测定生物炭比表面积及孔径分布.样品经真空干燥12h(373K),然后在77K条件下进行N2吸附脱附实验.采用傅里叶红外光谱(FTIR,Vertex 80V,Bruker公司,德国)表征生物炭表面官能团的种类及变化.样品粒径为 200目以下,掺杂 KBr压片,扫描光谱范围为4000~400cm-1.
1.5 吸附试验
分别称取 250mg吸附剂(OB、BC-NaOH、BC-H2SO4和BC-NH3)加入到250mL 16mg/L CFX溶液中.反应体系置于避光恒温振荡箱中,振荡速率为200rpm,温度为 298K.在固定的时间间隔,取样,离心后过0.45µm滤膜,采用HPLC测定.每组实验做三次,用平均值表示结果.同时,在相同实验条件下做空白试验.
1.6 溶液中CFX的含量测定
采用 Agilent 1260高效液相色谱测定溶液中CFX的浓度.测定条件为:C18柱,检测波长为254nm,流动相为 0.1%乙酸-甲醇溶液(70:30, V/V),柱温298K.
CFX 的去除率(W)及吸附量(qe)分别按照式(1,2)进行计算:
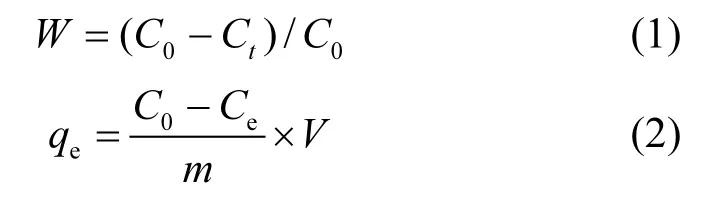
式中:C0, Ct及Ce分别为CFX初始浓度, t时刻浓度及体系平衡时浓度, mg/L; V为溶液体积,mL; m为吸附剂质量, g.数据采用软件Origin 9.0分析.
2 结果与讨论
2.1 材料表征
2.1.1 红外光谱分析 OB、BC-NaOH、BC- H2SO4和BC-NH3的红外光谱如图1所示.由图1可知,4种生物炭红外光谱曲线相似,但是某些官能团对应的峰强度及位置发生改变.波数在3600, 2917, 1545, 1100,1030, 792, 463cm-1对应的峰分别为醇羟基的伸缩振动峰、脂肪族C—H的伸缩振动峰、芳香环C—C伸缩振动峰、C—O伸缩振动峰、Si—O—Si不对称伸缩振动峰、Si—O—Si对称伸缩振动峰及Si—O—Si弯曲振动峰[14-15].其中,BC-NaOH在1545cm-1处,对应峰强明显大于其他生物炭,说明强碱改性后,明显的增加了生物炭表面的芳香性.而BC-NaOH在463cm-1处对应的峰强最弱,说明强碱和生物炭中的硅元素发生化学反应,生成可溶解的SiO32-[14].在 BC-H2SO4红外光谱中,醇羟基对应的峰消失,而出现羧酸羟基对应的峰(3400cm-1),说明硫酸改性后,生物炭表面酸性基团增加.
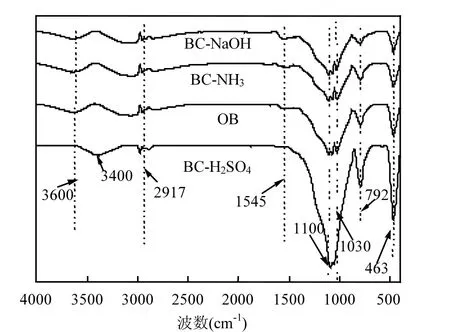
图1 试样的红外光谱Fig.1 FTIR spectra of materials

图2 不同材料的吸附-脱附等温线Fig.2 Adsorption-desorption isotherms of the samples
2.1.2 N2吸附-脱附曲线 样品OB、BC- NaOH、BC-H2SO4和BC-NH3的N2吸附-脱附等温线如图2所示.结果表明,4种生物炭的等温线均属于Ⅳ型等温线,在高压范围内有毛细凝聚现象,呈明显的 H3型滞后环.滞后环的存在及形状说明生物炭样品为微介孔结构且存在裂隙孔材料的孔结构[16].经氢氧化钠改性后,N2吸附量明显增强,说明材料比表面积增大.4种生物炭的孔结构参数见表1.

表1 不同样品的孔结构参数Table 1 Pore structure parameters of the samples
2.1.3 扫描电镜 OB、BC-NaOH、BC-H2SO4和BC-NH34种生物炭的SEM图谱如图3所示.初始生物炭表面粗糙,为吸附污染物提供了较多的吸附点位(图 3a).经改性后,炭表面发育出更多的微孔结构,特别是 BC-NaOH,呈蜂窝状,展现出更多的微孔和粗糙的表面,说明了这种生物炭的比表面积有所增大.材料的N2吸附-脱附等温线实验同样证实了这个结果.
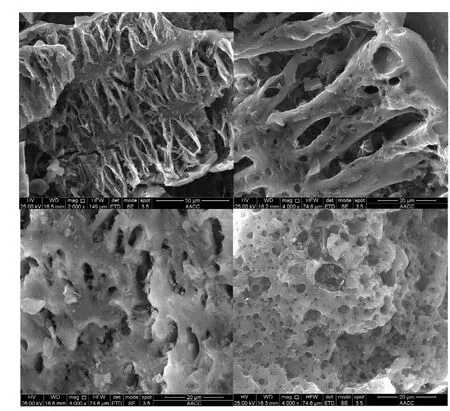
图3 OB, BC-H2SO4, BC-NH3和BC-NaOH的SEMFig.3 SEM images of OB, BC-H2SO4, BC-NH3 and BC-NaOH
2.1.4 元素分析 四种生物炭的元素组成如表2所示,氢氧化钠改性后,O和 H两种元素含量明显降低,说明改性后生物炭表面酸性-OH下降.H/C及(O+N)/C均下降,说明BC-NaOH的极性降低而芳香性增加[17].另外,BC-NaOH的灰分含量明显小于其他类型生物炭,说明了在改性过程中,初始生物炭所含的硅元素与强碱发生化学反应,生成了可溶性硅酸盐,导致无机元素含量降低.硫酸改性后生物炭则增加了酸性-OH 的含量,极性也随之增大,芳香性减弱.氨水由于碱性较弱,各元素含量与初始生物炭相比,基本保持不变.
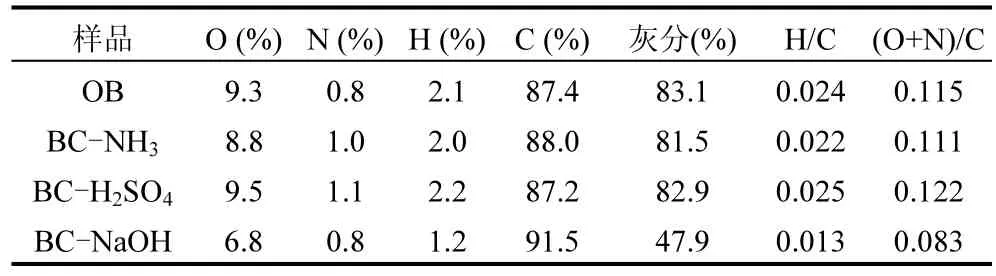
表2 不同样品的元素组成Table 2 Elemental composition of the biochar samples
2.2 不同生物炭吸附CFX的比较
不同类型生物炭对 CFX的去除率如图 4所示.实验条件为:1.0g/L吸附剂,16mg/L CFX,反应时间为30min, 温度298K.由图4可知,BC-NaOH和BC-NH3两种生物炭在30min内快速达到平衡.30min时,OB、BC-NaOH、BC-H2SO4和BC-NH3对CFX的去除率分别为5%,83%,8%和33%.BC-NaOH去除率明显的高于其他3种生物炭,这和其比表面积大于其他生物炭相一致.另外,BC-NaOH和其他生物炭相比疏水性增强(表 2),在吸附 CFX 的过程中,强极性水分子和CFX相互竞争吸附点位,而疏水性越强,对水分子的排斥力越大,越有助于 CFX的吸附[18].由空白试验结果可知,周围介质及CFX自身分解对吸附效果影响可以忽略.
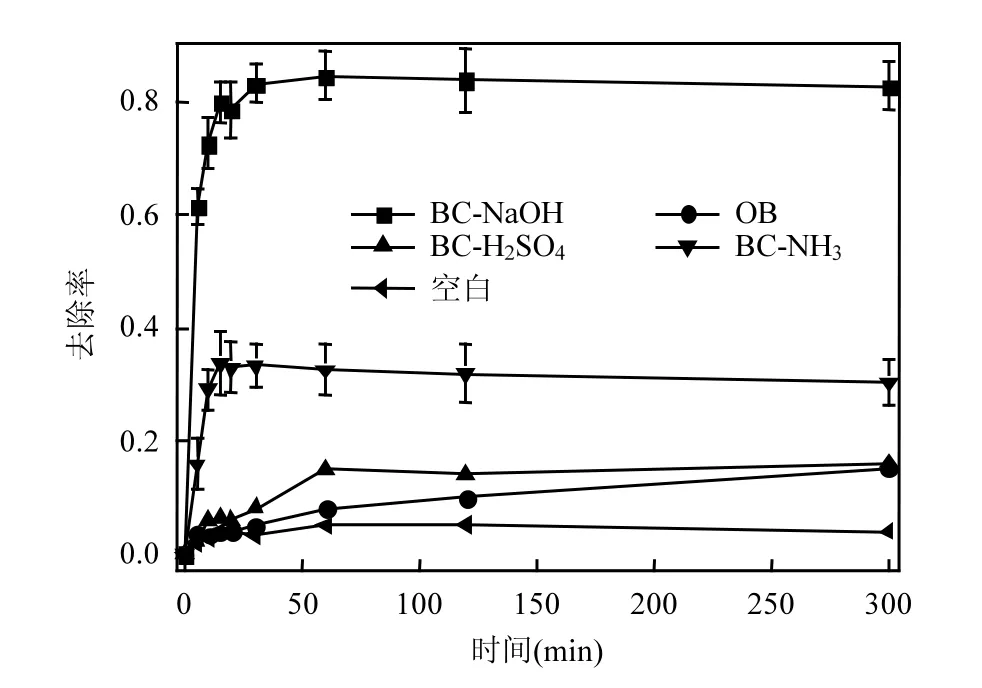
图4 不同生物炭吸附CFX对比Fig.4 Comparison of cefotaxime adsorption by different biochar
2.3 CFX吸附动力学研究
为了进行 CFX去除的动力学研究,实验采用伪一级动力学方程、伪二级动力学方程和颗粒内扩散模型拟合实验数据.伪一级动力学线性方程如式(3)所示:

式中:k1是伪一级动力学反应常数,1/min;C0,Ct分别为CFX初始浓度及t时刻的浓度,mg/L.伪二级动力学线性方程如式(4)所示:
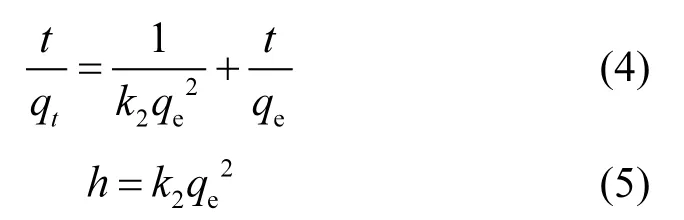
式中:k2是伪二级动力学反应常数,g/mg/min;qt,qe分别为t时刻和吸附平衡时的吸附量,mg/g.式(5)中的h为初始反应速率,mg/g/min[19].颗粒内扩散模型方程如(6)所示[19]:

式中:qt为 t时刻的吸附量,mg/g; ki为内扩散速率常数,(mg⋅min1/2)/g; C 为常数.
表3显示了4种生物炭去除CFX的动力学参数.由表3和图5(a)可知,BC-NaOH对伪二级动力学方程拟合较好(R2>0.99).BC-NaOH 反应常数和初始反应速率最大,分别是其他材料的 1.9~17.9倍和 11.2~478.9倍.以上分析表明,BC-NaOH对CFX的吸附速率主要受化学吸附机理控制.图5(b)表示了4种生物炭对颗粒内扩散模型拟合度.由图5(b)及表2~5可知,在吸附初始阶段,4种生物炭的拟合度较好,相关系数(R2)均大于 0.90,说明在生物炭吸附初始阶段,颗粒内扩散起到了重要的作用[20].

表3 不同材料去除CFX的动力学参数Table 3 Kinetics parameters of cefotaxime removal by various materials

图5 生物炭的动力学曲线及拟合Fig.5 Application of linear models for CFX adsorption by biochars
2.4 CFX吸附热力学研究
吸附热力学研究有助于进一步的明确 BCNaOH与CFX之间的作用原理.Freundlich等温线模型、Langmuir等温线模型和Temkin等温线模型是最常用的模型.Freundlich等温线模型的表达式如式(7)所示:

式中:qe为吸附平衡时的吸附量,mg/g;KF为Freundlich常数,(mg(n+1)⋅Ln)/g,表示吸附容量;n表示吸附强度[21].Langmuir等温线模型的表达式如式(8)所示:

式中:Ce是吸附平衡时 CFX浓度,mg/L;qmax是最大吸附量,mg/g;KL是 Langmuir常数,L/mg,代表吸附强度[22].常数 RL能够反应 Langmuir模型的本质特征,其表达式如式(9)所示:

式中:C0是 CFX初始浓度,mg/L;KL是 Langmuir常数,L/mg.RL=0 时,表示吸附为不可逆吸附;0<RL<1 时,表示优先吸附;RL=1时,表示线性吸附[19].
Temkin等温线模型表达式如式(10)所示:

式中:R为气体常数,8.314J/mol/K;bT是 Temkin常数,J/mol,与吸附热有关;T为绝对温度,K; KT是Temkin模型结合常数,L/mg.
分别配制16, 24和32mg/L的CFX溶液于250mL锥形瓶中,加入250mg BC-NaOH, 按照2.1.5所述步骤测定CFX浓度.生物炭的热力学模型参数如表4所示.
由表4可知,4种生物炭的n值均大于1,说明生物炭的吸附强度大,易于吸附.采用酸碱改性后的生物炭,n及 KF值均增加,说明改性后生物炭的吸附能力增强.其中BC-NaOH的 KF是其他几种生物炭的7.9~24.7倍,吸附能力最强.在 Langmuir模型中,BC-NaOH的qmax和KL也明显的大于其他几种生物炭,说明 BC-NaOH具有较大的吸附量及吸附强度.CFX浓度为16, 24和32mg/L 时,RL的数值分别为0.27, 0.20和0.16,均小于1,说明BC-NaOH对CFX的吸附为优先吸附.
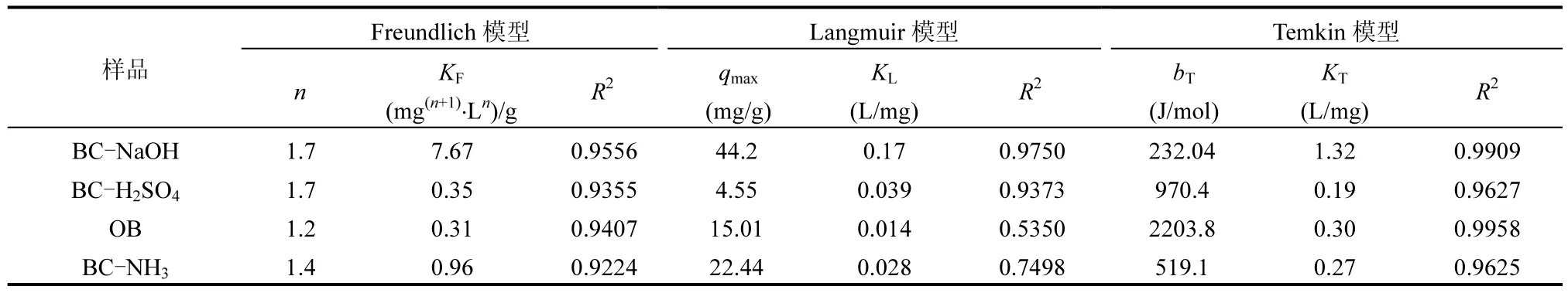
表4 不同材料去除CFX的热力学参数Table 4 Isotherm parameters of cefotaxime removal by various materials
4种生物质炭对CFX的吸附过程均能较好的符合 Temkin模型,其拟合系数 R2均大于 0.96.Temkin模型认为由于吸附质分子之间的排斥导致每层的分子吸附热都随着覆盖率增大线性降低[23].由表 4可知,BC-NaOH的分子吸附热最小,说明BC-NaOH表面的覆盖率最大,吸附最强.Temkin模型用以说明吸附过程是存在较强静电作用的化学吸附,这表明4种生物炭在吸附CFX时,存在静电引力作用[24].
2.5 CFX吸附影响因素
2.5.1 吸附剂用量 在初始溶液pH值为6.5,CFX浓度为16mg/L,温度为298K条件下,考察BC-NaOH的投加量为0.8, 1.0, 1.6和2.0g/L时溶液中CFX去除效果,如图6所示.由图6可知,4种投加量下,BC-NaOH对溶液中CFX的吸附随投加量的增加而增加.30min时,投加量为0.8, 1.0, 1.6和2.0g/L的去除率分别为71%,83%,92%及94%.CFX去除率增大的原因主要是随着BC-NaOH投加量的增加,吸附剂提供的活性吸附位点和总比表面积随之增加.在溶液中,CFX与BC-NaOH的接触机会增加,而CFX分子之间的竞争吸附减少.当投加量由 1.6g/L增加到 2.0g/L时,BC-NaOH的使用量增加了25%,而CFX的去除率仅增加 2%,这说明吸附剂的投加量进一步加大时,吸附效率有所下降[25].因此,后续试验中,除非特殊说明,吸附剂的使用量为1.6g/L.

图6 BC-NaOH投加量对CFX去除率的影响Fig.6 Effect of BC-NaOH dosage on removal efficiency of CFX
2.5.2 污染物浓度 在250mL溶液中,BC-NaOH的投加量为 1.6g/L,初始溶液 pH值为 6.5,振荡速率为200rpm,温度为298K条件下,考察CFX浓度为8,16,24和32g/L时溶液中CFX去除效果,如图7所示.由图7可知,CFX的去除率随初始浓度的增加而降低.在30min内,初始浓度为 8g/L的 CFX 溶液,去除率为98%.当浓度增加到 16,24和32g/L时,去除率分别为91%,84%和 66%.去除率降低的主要原因是在相同的体系下,BC-NaOH提供的吸附活性位点是固定的,CFX初始浓度越大,分子之间的竞争吸附越严重.在CFX初始浓度增加的过程中,一方面 CFX分子之间竞争吸附增加;另一方面随着CFX浓度的增加, CFX与生物炭表面活性位点之间的接触几率增加[26].CFX初始浓度由8g/L增加到16g/L时,初始反应速率常数(h)由 14.5mg/(g⋅min)增加到 39.3mg/(g⋅min).这说明CFX与 BC-NaOH之间接触几率增加的程度大于CFX分子之间竞争吸附的增加.当 CFX初始浓度进一步增加时,h则下降,说明了竞争吸附的增加占优势地位[15].
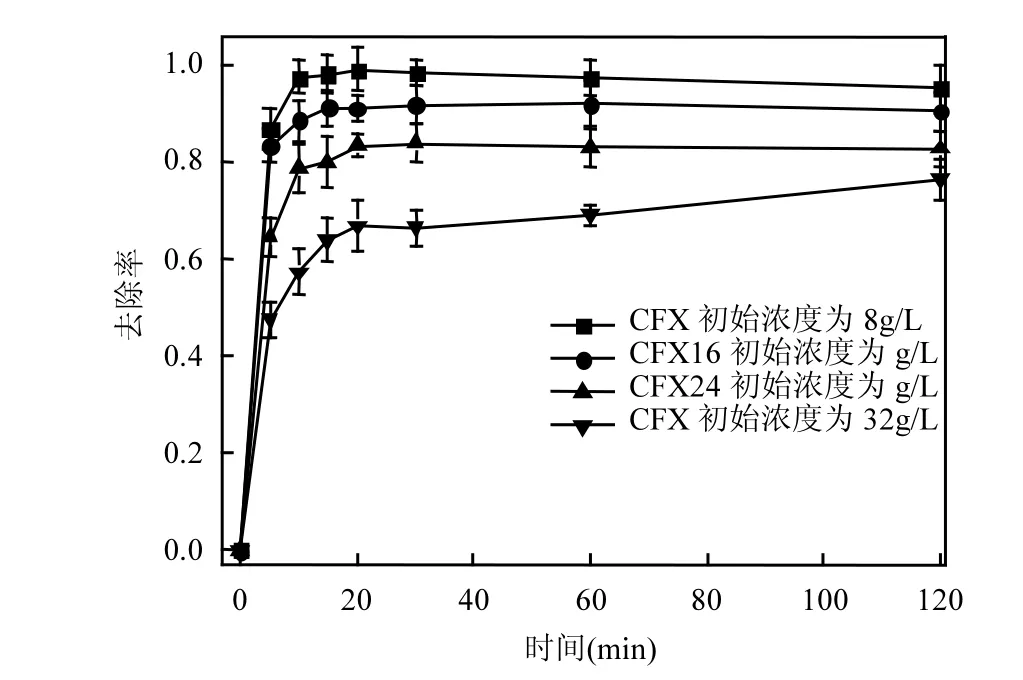
图7 CFX初始浓度对去除率的影响Fig.7 Effect of initial CFX concentration on removal efficiency
2.5.3 pH值 溶液pH值能够影响吸附剂的表面电荷分布,进而影响BC-NaOH对CFX的吸附[27].不同的pH值条件下CFX的吸附变化如图8所示.实验条件为:16mg/L CFX,1.6g/L BC-NaOH,温度为 298K,平衡时间为60min.由图8(a)可知,各pH值条件下,30min时CFX的吸附基本能达到平衡,且其去除率随pH值的增加而减小.初始pH值为2, 4, 6, 8, 10时,对应的去除率分别为98%,95%,92%,84%和74%.CFX属于β-内酰胺类化合物,在强酸条件下稳定性较差.扣除背景溶液的影响后,溶液初始pH为4和6时,对应的实际去除率分别为90%和89%,大于在强酸及碱条件下的去除率,如图8(b)所示.
CFX在溶液中存在三级电离平衡(pKa =2.1, 3.4,10.9).在 pH<2.1时,CFX 主要以阳离子形式存在;pH>2.1时,主要以阴离子存在[28].因此,在一般溶液状态下,CFX主要是以阴离子的形式存在.BC-NaOH的零电荷点分布如图 8(c)所示,由图 8(c)可知其零电荷点(pHPZC)为6.2.当溶液pH<6.2时,BC-NaOH表面带正电荷,而 pH>6.2时,BC-NaOH 表面则带负电荷.溶液初始 pH值为 2, 4和 6时,CFX带负电荷,而BC-NaOH 表面带正电荷,存在静电引力,因此吸附效率高.溶液初始pH值为8和10时,CFX和BC-NaOH表面均为负电荷,存在静电排斥作用,导致吸附效率下降.以上分析表明,在BC-NaOH吸附CFX的过程中,静电引力起重要作用,这和Temkin 模型相吻合.
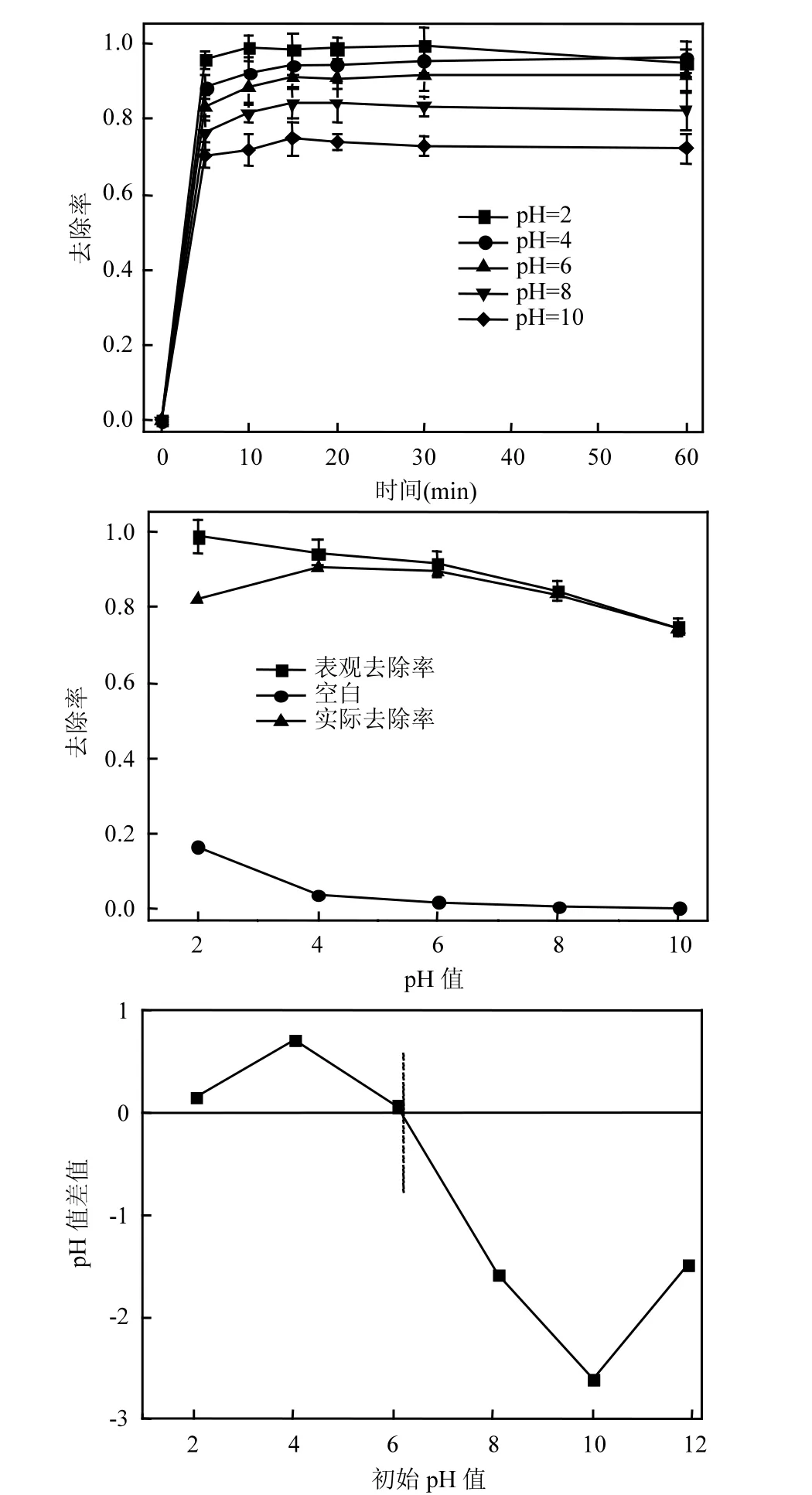
图8 溶液初始pH值对CFX去除的影响和BC-NaOH零电荷点分布曲线Fig.8 Effects of initial solution pH on the removal of cefotaxime and the pHPZC of BC-NaOH
此外,BC-NaOH与CFX间的疏水亲和作用随pH值不同而改变也是影响吸附效率的因素之一[29].生物炭经 NaOH改性后,H/C及(O+N)/C均下降,说明BC-NaOH的极性降低而芳香性增加[17].在酸性介质中,CFX疏水性相对较强,因此与BC-NaOH间的疏水亲和作用较强,吸附率较高.碱性环境下,CFX 的疏水性减弱,导致亲和作用下降,吸附减弱.Wang等采用改性碳纳米管吸附诺氟沙星时发现,碳纳米管表面的疏水位点与诺氟沙星的疏水性之间的强疏水亲和作用,是重要的吸附机理之一[29].
2.5.4 温度的影响 BC-NaOH的投加量为 1.6g/L,CFX浓度为16mg/L,初始pH值为6.0,温度分别为298,313, 323K条件下,考察BC-NaOH对CFX去除效果的影响.由图 9可知,随着温度的升高,吸附平衡时间缩短,吸附效率下降.平衡时间缩短的原因是体系温度升高,分子的运动速率加快,吸附和脱附达到快速平衡.CFX吸附效率的下降说明了 BC-NaOH吸附CFX的过程为放热过程.热力学参数(ΔG0, ΔS0和ΔH0)能更准确的说明吸附过程是吸热反应还是放热反应.计算式为[15]:
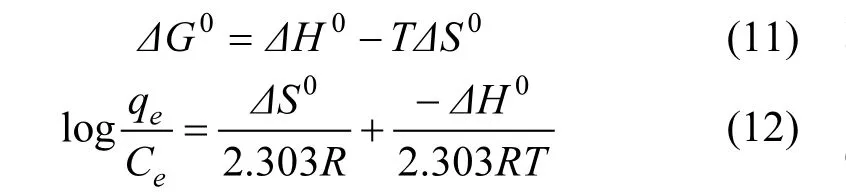
式中:ΔG0, ΔS0和 ΔH0分别为吉布斯自由能(kJ/mol)、熵变(J/mol/K)和焓变(kJ/mol); T为绝对温度,K;R为气体常数 8.314,J/mol/K; qe是平衡吸附量,mg/g;Ce是CFX平衡浓度,mg/L.

图9 溶液温度对去除率的影响Fig.9 Effect of solution temperature on removal efficiency
根据拟合直线的斜率和截距计算热力学参数,结果如表 5所示.ΔH0为-40.91kJ/mol,说明了吸附过程是放热过程;ΔS0为-121.3J/mol/K,表明体系混乱度减小,CFX被BC-NaOH吸附后由水相进入BC-NaOH表面或层间,变得更加有序.3个温度下ΔG0均为负值,说明BC-NaOH吸附CFX的过程为自发反应[26].ΔG0绝对值的大小决定了吸附过程中推动力的大小,由表5 可知, ΔG0298K>ΔG0313K>ΔG0323K,说明 BC-NaOH 吸附CFX的强度随温度升高而降低.

表5 不同温度下的吸附热力学参数Table 5 thermodynamic parameters for the removal of CFX at different temperatures
2.6 吸附机理
BC-NaOH的比表面积、芳香性及疏水性均明显的大于初始生物碳,有利于CFX的吸附.同时,结合BC-NaOH表面形貌的表征及影响CFX吸附因素的分析,说明了BC-NaOH吸附CFX的作用主要有疏水亲和作用和静电引力.酸性环境下 CFX疏水性增强,有利于从极性水分子中转移到BC-NaOH表面疏水区域,增加了CFX的吸附.弱酸性介质中,CFX发生解离,为阴离子形式,羰基氧与醚氧由于富含电子也带部分单位负电荷;BC-NaOH表面带正电荷,因此CFX与BC-NaOH存在较强的静电引力.吸附热力学研究表明 BC-NaOH吸附 CFX能很好地拟合Temkin模型,进一步证实了吸附过程存在较强的静电作用.
3 结论
采用液相浸渍方法制备了 BC-NaOH、BCH2SO4和 BC-NH33种改性生物炭用以吸附水体中CFX.考察其吸附动力学,吸附热力学及吸附影响因素,并揭示了BC-NaOH吸附CFX的机理.具体如下:
3.1 BC-NaOH和其他几种生物炭相比,比表面积增大,极性减弱,芳香性增强,可以提供更多的吸附点位,有利于吸附进行.
3.2 吸附动力学研究表明,BC-NaOH吸附CFX符合伪二级反应动力学且反应速率常数和初始反应速率显著高于其他几种材料.吸附热力学研究表明, BCNaOH吸附CFX符合Temkin模型,说明吸附过程存在静电作用.
3.3 吸附剂浓度、初始CFX浓度、溶液pH值及温度等都影响吸附剂吸附CFX的效果.当吸附剂浓度为 1.6g/L,初始 CFX 浓度为 16mg/L,溶液 pH=6,温度为 298K时,吸附效果较好,且吸附过程为放热自发过程.
3.4 疏水亲和作用及静电引力是 BC-NaOH吸附CFX的主要机理.

