氯掺杂氧化亚铜的制备及光电性能
谢思思,千志科
(黄河交通学院 a.基础教学部;b.机电工程学院,河南 焦作 454150)
Cu2O半导体是一种理想的低成本太阳能电池材料,其光电转换效率的理论值约为20%。因其具有无毒、资源丰富、制备成本低、可吸收大部分可见光、有较高的多数载流子的迁移率以及几微米的少数载流子的扩散长度等特点,在太阳能光伏器件中有很大的潜在价值。但由于氧化亚铜层的阻抗较大,其光电转换效率大大降低。一般情况下,氧化亚铜Cu2O的导电类型为p 型,常温下直接带隙为 1.9~2.38 eV[1]。 通过电化学沉积法在酸性电解液中制备出来的氧化亚铜晶体的导电类型体现为n型,其n型导电类型的原因是由氧空位引入的缺陷能级引起的[2]。 研究表明[3],在酸性条件下通过氯元素的掺杂可明显降低氧化亚铜的表面阻抗,使其具有更好的光电转换能力。在此基础上,本工作采用电化学沉积法在弱酸性溶液中制备氧化亚铜薄膜,通过改变电解液中Cl-含量,来实现Cu2O的不同程度的氯掺杂。利用表面光电压谱和相位谱研究了在外加电场作用下Cl掺杂Cu2O光电化学性能的变化。
1 实验
1.1 实验过程
采用电化学沉积法制备Cu2O薄膜。以导电玻璃ITO(普通玻璃镀一层氧化铟锡)为工作电极,铂片Pt为对电极,饱和甘汞电极(SCE)做参比电极,用实验室自制的支架组成三电极体系,在LK98B型电化学工作站上进行实验。以0.02 mol/L的醋酸铜和0.1 mol/L醋酸钠的混合溶液为电解液,分别加入0、5、7、10 mmol/L的氯化钠进行氯掺杂,用醋酸调节其pH值在5.6~5.8之间,恒温水浴控制溶液温度为40℃。选择电流-时间曲线来控制输入电压为恒压,在恒定电位-0.2 V下沉积2 h。反应结束后,用大量去离子水冲洗残留在Cu2O样品表面上的溶液,室温干燥即可。
1.2 表征
采用X射线衍射仪(XRD,Cu Kα射线,衍射角2θ为20°~90°)表征Cu2O样品的结晶状态及晶体结构。用场发射扫描式电子显微镜FESEM(JSM-7001F,JEOL)来表征样品的表面形貌。采用表面光电压设备(由锁相放大器、斩波器、单色仪自组装,可用于半导体材料表面光电压及相位的测试)测试样品在外加电场作用下的表面光电压谱和相位谱。器件结构为导电玻璃(ITO)/Cu2O/导电玻璃ITO的夹心饼干结构,一侧ITO作为上电极与锁相放大器相连,另一侧ITO(样品衬底)作为下电极接地,入射光作用于上电极。
2 结果与讨论
2.1 Cu2O的晶体结构表征
图1为氯掺杂的Cu2O样品的XRD图谱,ITO的特征峰作为对照。从图1中可知,Cl-浓度低于7 mmol/L时, 特征峰出现在 29.6°、36.4°、42.3°、61.4°、73.6°处,分别对应于 Cu2O 晶体的(110)、(111)、(200)、(220)、(311)晶面,说明在电化学沉积过程中Cu2O实现了结晶,只有 Cu2O 生成。 溶液中 Cl-浓度为 0、5、7、10 mmol/L时(111)晶面与(100)晶面的强度之比值分别为1.90、1.91、2.13、3.81,比值在不断地增加,说明沉积得到的氧化亚铜晶体在(111)面上生长速率较快,在此方向上有优先,并且随着反应溶液中Cl-浓度的增加更加显著。从图1中(d)线可以看到比较微弱的Cu(111)晶面的衍射峰,这说明ITO表面上的样品中有Cu出现。导致Cu单质生成的原因应该是氯离子浓度的增加使得电流密度增大,反应速度加快,ITO表面附近 H+浓度增加,使得Cu2O进一步被还原为铜单质。其反应如下:
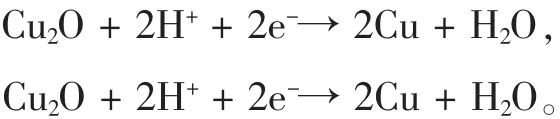

图1氯掺杂的Cu2O薄膜的XRD图谱
图2为氯掺杂的Cu2O薄膜表面形貌。由图2(A)可知,不加添加剂NaCl掺杂的电化学沉积中得到的Cu2O样品表面形貌为类似树枝结构,晶面较复杂,有许多类似针尖的部分;在图2(B)中,经过Cl掺杂后,样品晶体的针尖部分变短,中心部分变大,形貌逐渐向立方体形状转变。当Cl-浓度为5 mmol/L时,晶体的中心部分向四周扩大,基本上为四个橘瓣状的双层结构;当Cl-浓度增加到7 mmol/L时,双层结构继续扩大为类似方形结构,但方形结构不规则,原因是晶粒生长时相互挤压导致形状大小不一;在Cl-浓度为10 mmol/L时,晶粒的尺寸约为12 μm,是7 mmol/L时的2倍,晶体的立方形状也更加明显地呈现出来。从SEM图像的结果综合分析可知,Cl-浓度的增加可引起溶液中总离子浓度增加,也同时增加了晶粒(111)面的优先生长趋势,因此(111)晶面与(100)晶面的强度之比增大,晶体生长过程中更容易形成立方晶粒[4],这与XRD衍射结果一致。因此Cl掺杂使Cu2O晶体的表面形貌产生较大的变化,同时促使晶粒尺寸增大。

图2 氯掺杂的Cu2O薄膜的SEM图谱
2.2 氧化亚铜薄膜的表面光电压分析
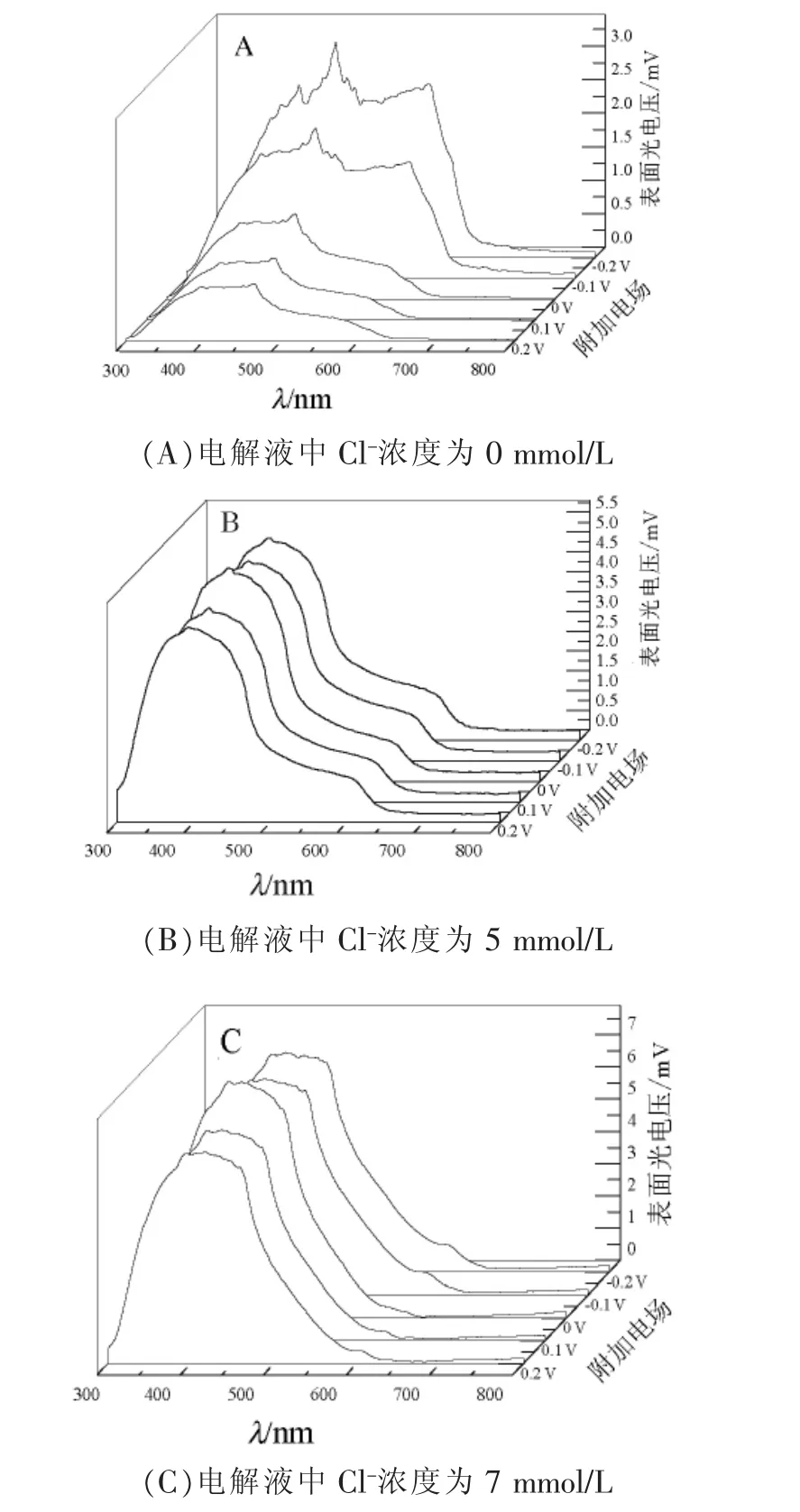
图3 Cu2O薄膜的表面光电压谱
常用表面光电压光谱(SPS)和相位谱(PS)来表征半导体材料的电子结构和光学特性[5]。图3是Cu2O薄膜在附加电场作用下的场致表面光电压谱。当电解液中Cl-浓度为10 mmol/L时有铜单质生成,在此不作讨论。图3A中460 nm处的峰是测试时光源Xe灯的特征谱线,图3B、图3C中由于样品SPS谱强度增加,Xe的衍射峰不太明显。实验制得的所有Cu2O样品的光电压,均有在加正偏压时逐渐降低、在加负偏压时逐渐升高的趋势。在外加电场为负时,所加偏压与Cu2O样品的光生伏特效应的电场方向一致,由Cu2O晶体的体相指向表面,使得SPS幅度得到增加[6]。反之,当附加电场为正时,SPS响应减弱。由此可得实验制备的Cu2O均为n型。
图4是Cu2O样品的场致表面相位谱。由图4(A)可知在外加电场为负时,相位在-100°~-120°之间,由第四象限偏转到第三象限,表明光生电子由于内建电场而分离移动到体相的趋势减弱,即表面处的电子浓度小于空穴浓度。这可能是因为当在ITO与n型Cu2O半导体之间加负偏压时,表面附近形成空穴堆积的反型层,导致表面聚集的电荷类型发生了变化。而在图4(B)和图4(C)中,同样施加负偏压,相位变化不大,均位于第四象限,且随着Cl-浓度增加,相位变化越来越小。根据研究结果[7],Cl掺杂可以使载流子浓度增大 2~3 个数量级,增加电子浓度,使费米能级更接近导带。同样处于负电场作用时,靠近表面的薄层中空穴浓度远小于高电阻区的电离施主或体内的电子浓度,不会影响空间区域的电荷分布,表面层附近也不会具有明显的导电性。Cl掺杂后,多子的浓度明显增加,从而克制了反型层的形成[8],有了图 4(B)和图 4(C)的结果。
图4 Cu2O样品的薄膜场致相位谱
3 结论
在弱酸性电解液下通过电化学沉积法得到的Cu2O导电类型为n型,Cl掺杂对晶体的生长有较大影响,可促进其(111)面的生长。相比于未掺杂的样品,经过Cl掺杂后,载流子浓度的提高抑制了反型层的形成,增强了氧化亚铜的n型导电性。当Cl-浓度过高时部分Cu2+会过度还原成铜单质,与Cu2O薄膜可能会形成肖特基势垒接触。

