锌参与的氨水中醛的电化学烯丙基化反应
梁向晖, 郭伟聪, 黄兴鹏, 孙栋梁, 黄精美
(华南理工大学 化学与化工学院, 广东省功能分子工程重点实验室, 广东 广州 510640)
实验教学作为培养学生综合素质、挖掘创新能力的重要手段,已在国内外众多高校中达成广泛共识[1-3]。随着现代科技发展,一些传统和污染大的化学实验已不能满足现今社会发展和环保需求。具有实时性、综合性、应用性、绿色低碳的化学教学实验是我们追求的特色目标。我院化学学科作为“双一流”建设学科,依托探索性实验项目、产研结合项目及化学学科竞赛等实验教学模式进行教学改革,着力培养并激发学生的科研兴趣,提高大学生实践能力、科研能力和创新创业能力[4]。
以化学学科竞赛为载体,学科竞赛与实验教学相互促进,构成了当今高校培养创新人才的新模式[5-6]。“锌参与的氨水中醛的电化学烯丙基化反应”为综合化学实验项目,不仅可训练学生传统有机实验技能,而且将电化学制备新技术、有机合成方法以及仪器分析等有机结合起来,激发了学生的创新能力和学习积极性,培养了学生化学知识综合应用能力。
1 实验原理
1.1 电有机合成
电有机合成是采用电化学的方法进行有机合成的一门学科。许多合成有机化合物的化学反应中包含着电子的转移,如果将这些反应安排在电解池中进行,这就是有机电合成反应[7-8]。电化学合成方法主要有以下优点:
(1) 电化学合成是通过调节工作电压来控制反应的方向,而且可在电解池中设置隔膜,阴极、阳极两级可以分开;
(2) 电化学反应一般在常温下进行,通过调节电流就可以调节反应速率;
(3) 电化学反应中参与反应的试剂之一是“电子”,可保证产品纯度;
(4) 电化学反应中,由于外界提供了电能,可以使吉布斯自由能ΔGT,p>0的反应进行;
(5) 可更好地选择所要得到的产品,特别是电极上所生成的活泼中间体,是传统合成手段以及光、热化学反应无法比拟的[9-11]。
1.2 反应机理
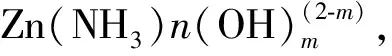
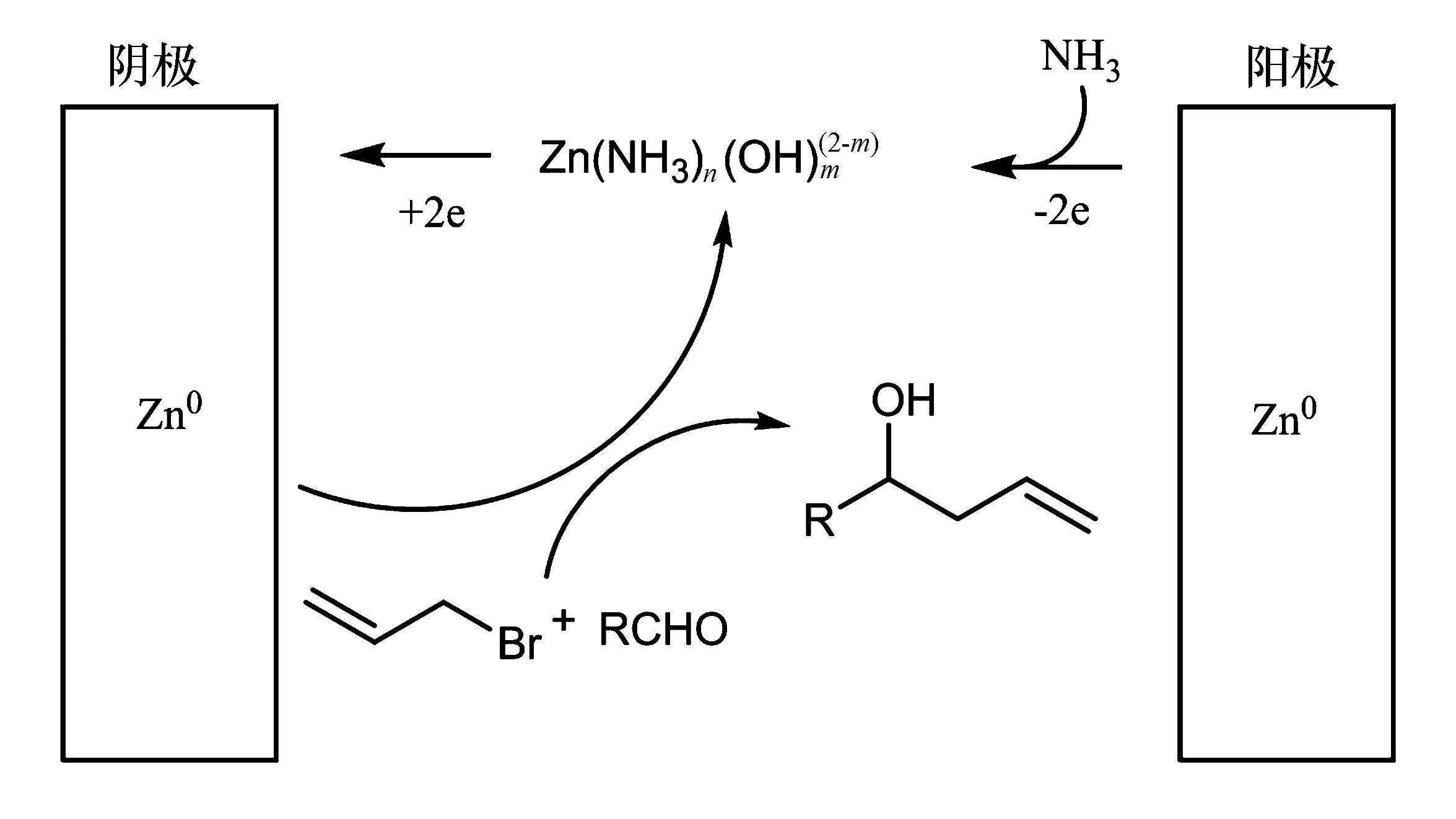
图1 反应机理示意图
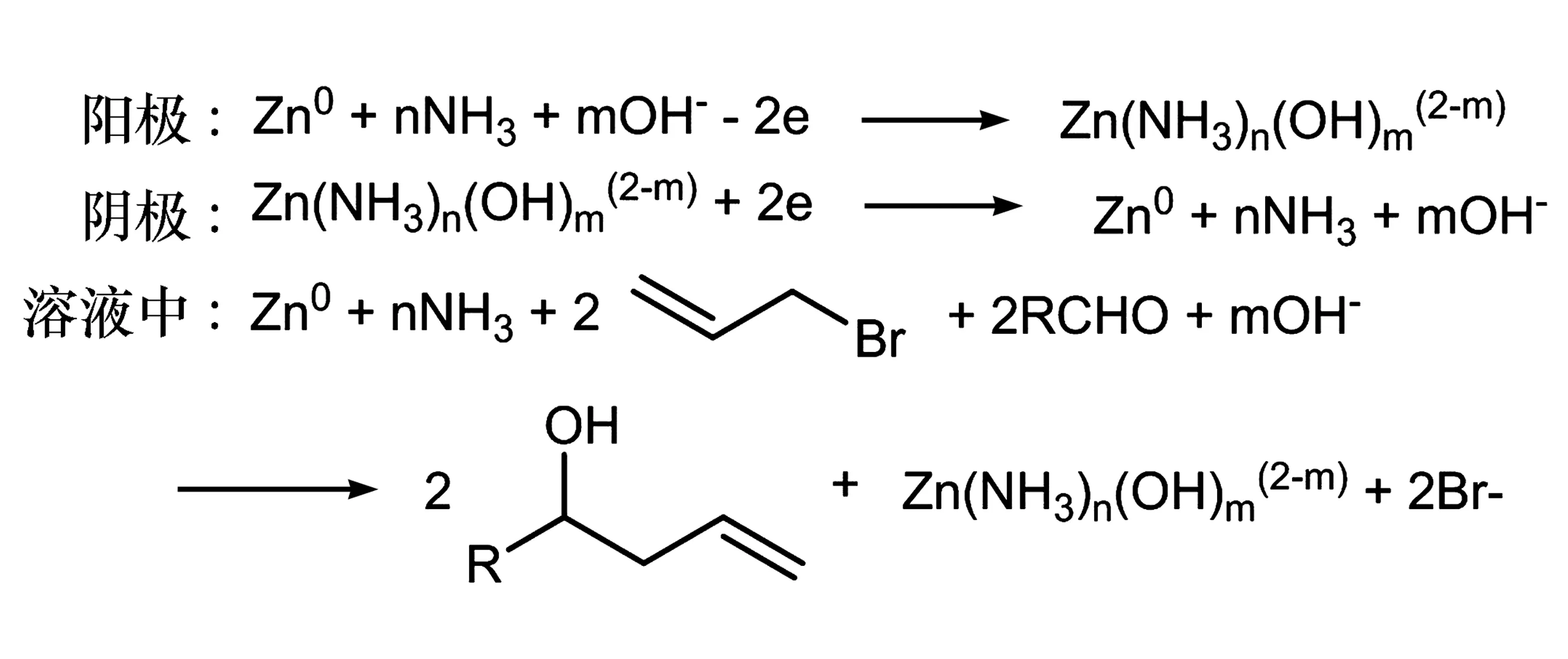
总反应式:

1.3 核磁氢谱图的定量原理
核磁氢谱的定量依据是核磁共振峰的峰面积或峰高与产生该共振峰的质子数成正比。目前核磁定量分析常用的方法是外加内标法,又称绝对测量法,此方法可以直接测量标准物质的含量。相对于传统的定值方法,核磁共振法样品制备简单,可以同时进行定性和定量分析,对样品没有破坏性,无需相关样品的对照物质[12]。在本实验中,采用内标物测定法来测定1-苯基-3-丁烯醇的含量。具体做法:将样品及内标物精确称量,配成一定浓度的溶液,测出核磁氢谱图,然后将内标物及样品的各指定基团上质子产生的共振峰积分值进行比较,即可根据下式算出样品的物质的量。
其中,AS和AR为被测物和内标物的选定信号的积分值,NS和NR为被测物及内标物的指定基团的质子数,WR和MR为内标物的绝对质量及分子量,nS和nR为被测物和内标物的物质的量。
在本实验中,采用硝基甲烷作为内标物,同时选取1-苯基-3-丁烯醇化学位移为4.6处峰作为产品的信号来源,则NR/NS为3。
式中,n为产物的理论的物质的量,W为产物理论质量,M为产物的分子量。
2 实验
2.1 仪器与试剂
仪器:电源以及导线若干,电磁搅拌器,旋转蒸发仪器,紫外灯,电子分析天平,400 MHz核磁共振谱仪,小搅拌子,搅拌子吸取竿,100 mL分液漏斗,50 mL圆底烧瓶,50 mL锥形瓶,100 mL烧杯,10 mL量筒,小漏斗,棉花,5 mL圆底烧瓶,展缸,TLC板,毛细管,滴管移液枪。
试剂:苯甲醛(C6H5CHO)、烯丙基溴(C3H5Br)、乙酸乙酯、石油醚、硝基甲烷、氘代氯仿,上述化学试剂为分析纯;25%氨水、超纯水、饱和氯化钠溶液、稀盐酸、无水硫酸镁、锌片(作为电极)。
2.2 实验步骤
2.2.1 电化学实验步骤
先使用锌片制作2电极(1.5 cm×1.0 cm)。在确认电源开关处于关闭状态后,将2个电极固定在5 mL圆底烧瓶的瓶壁上(2个电极之间间隔大约1 cm),连接电源线路,确保电路畅通;在圆底烧瓶中依次加入搅拌子,1.5 mL、25%的氨水和3.5 mL超纯水,开启搅拌,使氨水和超纯水充分混合;往圆底烧瓶中依次加入51 μL苯甲醛(称量并记录苯甲醛质量)和86 μL烯丙基溴,盖好橡皮塞后,接通电源,调节电流恒定为15 mA(始终注意电源示数是否出现异常值,反应100 min后停止通电;加入约1 mL乙酸乙酯后,继续搅拌3 min;静置后用毛细管取上层有机液点TLC,使用展开剂(乙酸乙酯与石油醚体积比为1∶7),观察反应进程。
使用稀盐酸调节反应瓶中的溶液pH值至中性,再全部转移到分液漏斗中,用乙酸乙酯冲洗电极两遍,将冲洗后的溶液一起合并到分液漏斗中;下层水相用乙酸乙酯萃取2次,每次约10 mL乙酸乙酯;再合并有机相并用约5 mL饱和氯化钠溶液洗涤一遍,萃取并分离出上层有机相,最后将有机相用无水硫酸镁干燥。将干燥后的有机相在带棉花的小漏斗中过滤,收集有机相后在旋转蒸发仪上蒸掉溶剂,称出粗产物质量(注意产物量少、无法倒出,要先称出空瓶质量,再加入萃取得到的有机相去旋蒸,利用差重法得到粗产物质量)。
加入内标(硝基甲烷)后做1H-NMR,并算出核磁产率。
2.2.2 对照实验步骤
在5 mL的圆底烧瓶中加入1.5 mL、25%的氨水和3.5 mL的超纯水,开启搅拌,使氨水和超纯水充分混合,在搅拌下依次加入51 μL苯甲醛(称量并记录苯甲醛质量)、86 μL、1.0 mmol的烯丙基溴和81 mg、1.2 mmol的市售锌粉;反应100 min后停止反应,后面处理按2.2.1的步骤进行操作。
2.2.3 产物的核磁产率计算
加入30 μL硝基甲烷(内标)于粗产物中,再加入适量氘代氯仿作为溶剂,溶解均匀,将溶液转移入核磁管,使用超导傅里叶核磁共振谱仪测定核磁氢谱,计算产率。
2.2.4 注意事项
(1) 开封已久的锌片表面可能会有氧化膜,需先用细砂纸打磨光滑后使用;苯甲醛容易被氧化成苯甲酸,使用前先减压蒸馏纯化,以除去苯甲酸。
(2) 两电极片之间间隔不能过近,否则在反应过程中阴极片上生成的锌粒堆积,可能会造成短路。
(3) 因为本反应是非均相反应,反应过程中需要保持剧烈搅拌,反应液形成漩涡,以使水相中反应物充分混合。搅拌子可能会在搅拌过程中卡入电极底部,若出现此状况需立即处理,使搅拌子正常运作。
(4) 使用乙酸乙酯洗涤电极时,尽量防止电极片上的锌粒掉落入洗涤液中。
(5) 核磁氢谱图定量时,应尽量选用只含单个氢原子且该氢原子共振峰附近无明显干扰峰的基团。
3 结果与讨论
3.1 1-苯基-3-丁烯醇的薄层色谱示意图
1-苯基-3-丁烯醇的薄层色谱点板示意图见图2。
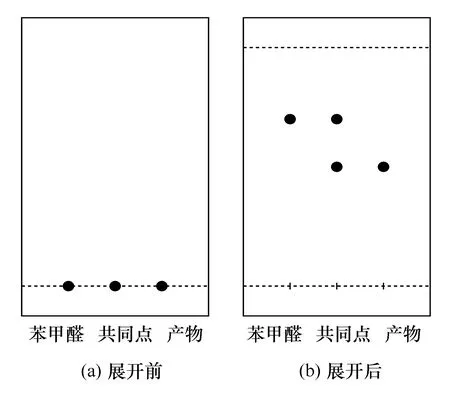
图2 TLC点板示意图
粗产品核磁氢谱图见图3。
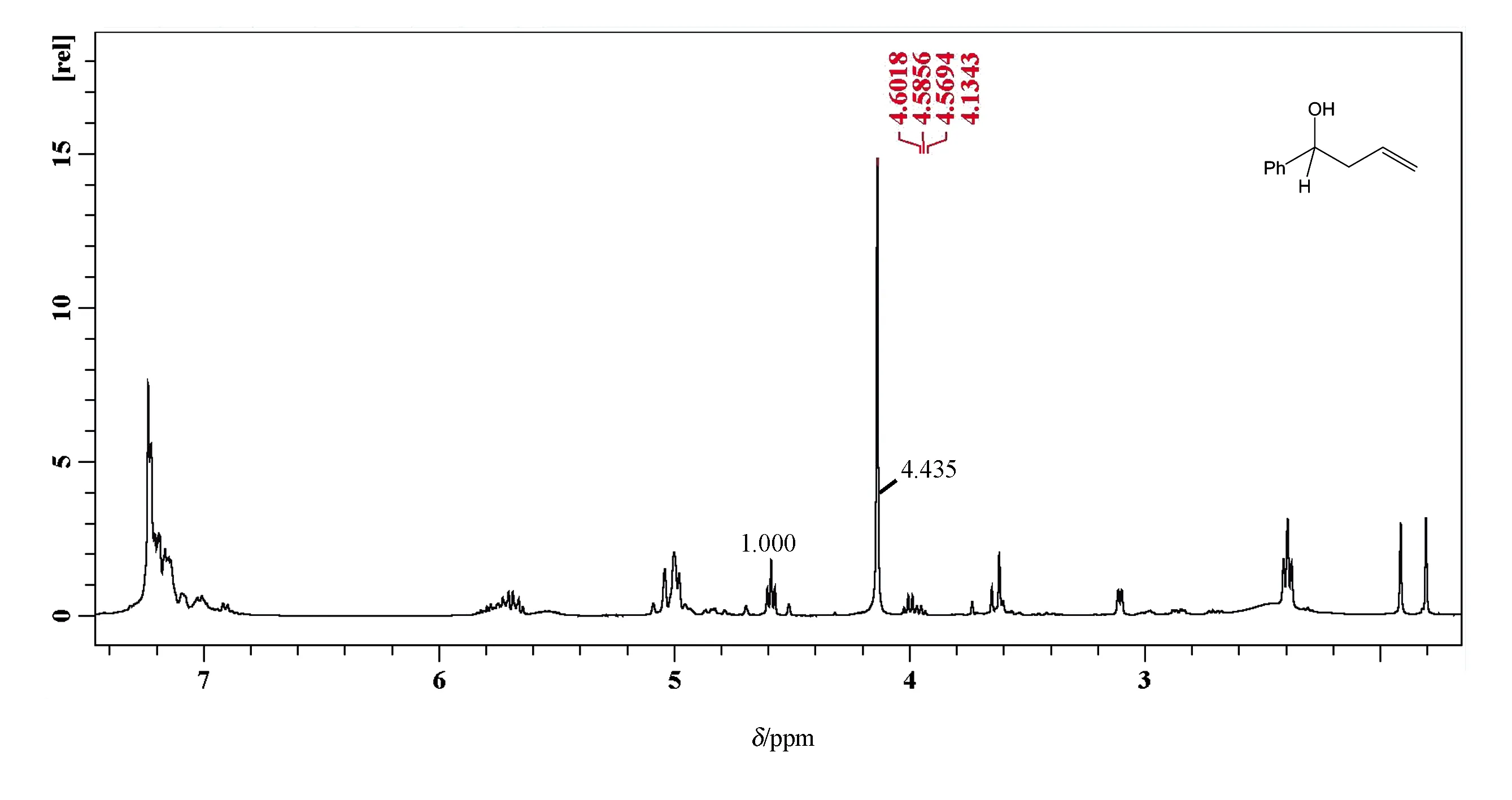
图3 粗产品核磁氢谱图
3.2 电化学实验产率
在电流为15 mA、反应时间为100 min、投料比为1∶3.5 、浓氨水与超纯水比例为1.7 mL∶3.3 mL的反应条件下,得到产率为61.2%。
3.3 对照实验产率
对照实验得到产率为27.0%。可见,相比较于电化学条件,使用传统方法得到的产率较低,不能很好地推广应用。而且耗费锌粉较多,后处理难度加大。
4 结语
将电化学实验引进本科实验教学之中,可以引导学生思考和对比电化学方法与传统合成方法的优缺点,可以锻炼学生的发现和思考问题的能力。相对于传统的合成方法,电化学方法制备1-苯基-3-丁烯醇能
明显加快反应速度,提高效率,而且电化学方法后处理步骤简单,作为阴极的锌片能够重复利用,实现节能环保。该反应为微量反应实验,操作难度加大,既可以锻炼学生操作能力,又可以减少反应废液和节约成本。实验采用内标法,通过核磁氢谱图中内标物与产品特征峰的峰面积比来确定产物的物质的量,具有逻辑性和科学性。将科研转化实验教学模式,科研反哺教学,实现创新人才培养的多元化模式。
[1] 王芳,李滨,宋瑛琳.国外高校实验教学经验及启示[J]. 实验室科学,2012,15(5):1-3.
[2] 江捷.英国高校实验教学的分析与启示[J]. 实验技术与管理,2008,25(1):110-111,143.
[3] 于化东.加强实践教学环节 提高大学生创新实践能力[J].中国高等教育,2010(21):23-25.
[4] 禹奇才,张俊平,张灵,等.创新性应用型人才:地方重点建设高校培养目标定位[J]. 中国高等教育,2010(22): 42-43.
[5] 李金昌,林家莲.实践教学与学科竞赛相结合,促进创新人才培养[J]. 实验技术与管理,2011, 28(11):1-3, 16.
[6] 赵小强,唐黎.大开放实验室环境及体系学科竞赛机制的构建与实践[J]. 实验室科学,2015,18(2):210-213.
[7] 傅献彩,沈文霞,姚天扬, 等.物理化学:下册[M].5版. 北京:高等教育出版社,2006:145-148.
[8] 高占先.有机化学实验[M].4版. 北京:高等教育出版社,2004.
[9] Huang J M, Yi D. Zn-mediated electrochemical allylation of aldehydes in aqueous ammonia[J]. The Royal Society of Chemistry, 2009(46):3943-3945.
[10] 董毅.电化学条件下氨水中锌参与的羰基化合物的烯丙基化反应[D].广州:华南理工大学,2010.
[11] 任海锐.电化学水相条件下锌催化的羰基化合物的烯丙基化反应[D].广州:华南理工大学,2010.
[12] 张琪,李晓东,杨化新.核磁共振技术在药品标准领域中的应用进展[J].药物分析杂志,2012,32(3):545.

