培美曲塞与多西他赛治疗老年晚期肺腺癌病人的疗效比较
肺癌是全球重大健康问题之一,其在全球癌症统计数据中是诊断率最高的癌症,占癌症发病率的13%[1]。尽管新药和新治疗理念层出不穷,但肺癌5年生存率依旧徘徊在15%左右[2]。非小细胞肺癌(NSCLC)占肺癌病理类型的80%~85%,其中腺癌已取代鳞癌,成为最常见的肺癌组织类型,有效改善此类病人的总生存期(overall survival,OS),可有望改善目前肺癌病人的生存现状[3]。 目前,第三代含铂双药联合化疗是针对晚期NSCLC病人标准一线化疗方案,但大多数老年NSCLC病人合并有心脑血管以及内分泌系统疾病,加之机体储备功能下降,对化疗的耐受性往往较差。本文回顾性分析我院收治的80例老年晚期肺腺癌病人的临床资料,比较培美曲塞联合顺铂与多西他赛联合顺铂治疗老年晚期肺腺癌病人的效果。
1 资料与方法
1.1 临床资料 收集2013年6月至2017年1月在我院治疗的80例老年晚期肺腺癌病人的临床资料,根据治疗方案将病人分为培美曲塞组41例,年龄61~82岁,中位年龄73.3岁;多西他赛组39例,年龄60~85岁,中位年龄74.8岁。所有病人经细胞学检测确诊为ⅢB~Ⅳ期的肺腺癌,PS评分均≤2分,预计生存期在3个月以上,化疗前检测肝肾功能及血常规均在正常范围,重要脏器无严重器质性病变,可耐受化疗。参与研究的所有病人均签署知情同意书。2组病人在年龄、性别上差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法 培美曲塞组:病人于接受培美曲塞化疗前1周开始口服叶酸片,400μg/d,一直持续到化疗结束;化疗前1周同时给予维生素B121000μg/次肌肉注射,每21 d注射1次;化疗前1 d、当天以及第2天予以口服地塞米松4 mg,2次/d,预防皮疹及过敏的发生;给予培美曲塞500 mg/m2,第1天静滴;顺铂70 mg/m2,第1天静滴;每21 d为1个周期。多西他赛组:化疗前1 d、当天以及第2天予以口服地塞米松8 mg,2次/d;多西他赛75 mg/m2,第1天静滴;顺铂70 mg/m2,第1天静滴;每 21 d为 1 个周期。化疗过程中给予预防止吐等措施,化疗结束24 h后若白细胞降低Ⅱ度以上,则给予升白治疗。复查血象1周1次,每次化疗前复查肿瘤标志物及生化指标,2个周期后行影像学检查评价疗效。
1.3 评价标准 疗效评估依据世界卫生组织(WHO)实体瘤疗效评价标准 RECIST 1.1进行。完全缓解(CR):所有可测病灶消失,肿瘤标志物降到正常范围,无新病灶出现,维持至少4周;部分缓解(PR):病灶缩小≥30%,维持至少4周;疾病稳定(SD):病灶改变介于PR和疾病进展(PD)之间;PD:原有病灶增大20%或出现新病灶。治疗有效=CR+PR,无效=SD+PD。所有病人化疗2个周期后进行疗效评价,检测血清肿瘤标志物和行胸腹增强CT,按RECIST标准继续下一周期治疗,病人出现PD则选取其他化疗方案,或联合放疗以及最佳支持治疗。无进展生存期(PFS)指病人开始化疗的日期至肿瘤进展或最后一次的随访日期。
1.4 统计分析方法 采用SPSS 19.0统计学软件进行统计分析,计数资料的比较采用χ2检验,计量资料比较应用t检验。以P<0.05为差异具有统计学意义。
2 结果
2.1 疗效及生存情况 2组的总有效率(RR)、疾病控制率(DCR)比较差异无统计学意义(P>0.05)。所有病人的随访时间为6~24个月,中位随访时间为10个月。2组病人的中位疾病进展时间(TTP)、中位生存期(MST)及1年生存率比较差异统计学意义(P>0.05)。见表1。

表1 2组临床疗效比较
2.2 不良反应 培美曲塞组恶心呕吐、便秘、腹泻、骨髓抑制(贫血、粒细胞减少)、疲劳乏力以及脱发不良反应发生率较多西他赛组低,差异具有统计学意义(P<0.05),其他不良反应发生率2组比较差异无统计学意义(P>0.05)。
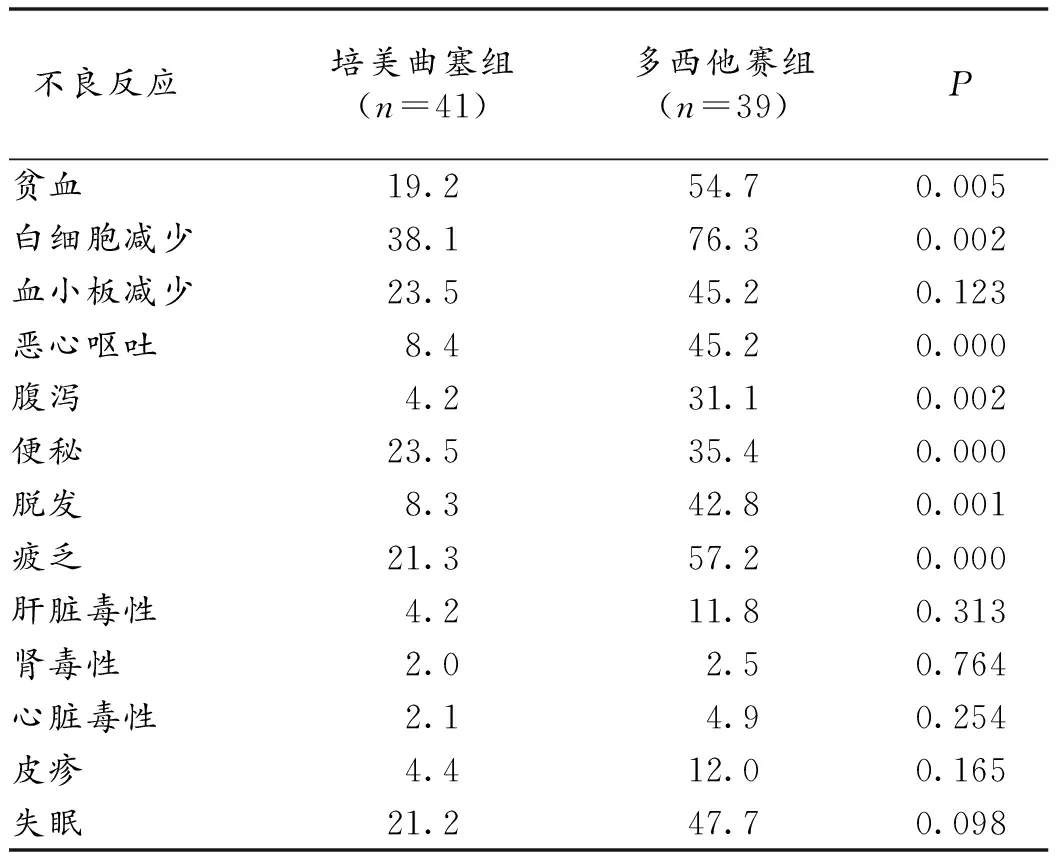
表2 2组不良反应比较(%)
3 讨论
NSCLC易远处转移以及复发,确诊时大概2/3的病人已处于中晚期[6],往往失去根治性手术机会,尤其是老年病人。由于老年人生理功能的特殊性,肝脏储备、肾脏清除力以及肺功能均降低,造血功能减退,合并其他脏器疾病,致使老年肺癌病人化疗耐受性降低。因此,在考虑化疗的治疗效果同时更要权衡病人对不良反应的耐受性。
培美曲塞是一种多靶点抗叶酸药,可以抑制甘氨酰胺核苷酸甲基转移酶、二氢叶酸还原酶以及胸苷酸合成酶等叶酸依赖性酶的活性,减少胸腺嘧啶和嘌呤等核苷的合成,阻碍肿瘤细胞 DNA以及RNA的合成,发挥抗肿瘤作用[8]。培美曲塞有低毒、高效、广泛抗瘤作用,美国FDA于2004年批准其用于晚期NSCLC的二线治疗[9]。一项Ⅲ期随机对照研究表明,培美曲塞和多西他赛针对不同的组织学类型,疗效也有差异,经培美曲塞治疗非鳞NSCLC病人的PFS更高(9.3月比8月),而对于鳞癌病人则经多西他赛治疗后病人的PFS较高(6.2月比7.4月)[11]。周元东等[12]的临床试验表明培美曲塞对于晚期非鳞NSCLC病人具有更好的疗效。铂类是调控细胞周期的非特异性药物,有一定细胞毒性,具有损伤癌细胞膜结构、抑制癌细胞DNA复制的作用,其广谱抗癌作用较强,与培美曲塞或多西他赛联合应用效果较好。
本研究结果表明2组RR、DCR、TTP、MST以及1年生存率比较差异无统计学意义。说明培美曲塞联合顺铂与多西他赛联合顺铂治疗老年晚期肺腺癌的效果相近。但培美曲塞组病人的恶心呕吐、便秘、腹泻、骨髓抑制、疲劳乏力以及脱发不良反应发生率较多西他赛组低。培美曲塞是通过破坏肿瘤细胞叶酸依赖性的正常代谢,从而抑制肿瘤细胞的复制,而多西他赛可以加强微管蛋白聚合同时抑制微管解聚,形成稳定的非功能性微管束,以破坏肿瘤细胞的有丝分裂。在药代动力学方面,培美曲塞以原药形式经肾脏排泄,而多西他赛在肝中代谢,主要经胆道从肠道排出。由于2种药物的作用机制、药代动力学的差异,造成2组的不良反应有一定的差异,但因本研究病例数有限,仍需大样本对照研究进一步明确作用。
[参考文献]
[1] Torre LA, Bray F, Siegel RL, et al. Global cancer statistics, 2012[J]. CA Cancer J Clin, 2015, 65(2):87-108.
[2] Miller KD, Siegel RL, Lin CC, et al. Cancer treatment and survivorship statistics, 2016[J]. CA Cancer J Clin, 2016, 66(4):271-289.
[3] Cheng TD, Cramb SM, Baade PD, et al. The International Epidemiology of Lung Cancer: Latest Trends, Disparities, and Tumor Characteristics[J]. J Thorac Oncol, 2016, 11(10):1653-1671.
[4] Loo BW. Non-Small Cell Lung Cancer, Version 2.2013 Featured Updates to the NCCN Guidelines[J]. JNCCN, 2013, 11(6):645-653.
[5] Kurata T, Iwamoto T, Kawahara Y, et al. Corrigendum to “Characteristics of pemetrexed transport by renal basolateral organic anion transporter hOAT3” [Drug Metab Pharmacokinet 29 (2) (2014) 148-153][J]. Drug Metab Pharmacokinet, 2016, 31(3):260.
[6] Joshi MB, Shirota Y, Danerberg KD, et al. High gene expression of TS1, GSTP1, and ERCCI are risk factors for survival in patients treated with trim odality therapy for esophageal cancer [J]. Clin Cancer Res, 2005, 11(6): 2215-2221.
[7] Peterson P, Park K, Fossella F, et al. 6521 POSTER is pemetrexed more effective in patients with non-squamous histology? A retrospective analysis of a phase III trial of pemetrexed vs docetaxel in previously treated patients with advanced non-small cell lung cancer (NSCLC)[J]. EJC Supplements, 2007, 5(4):363-364.
[8] 周元东, 顾洪兵. 培美曲塞在晚期非鳞非小细胞肺癌三线及以上治疗中的临床观察[J]. 现代肿瘤医学, 2017, 25(3):374-376.

