RORα基因 rs782931、rs11639084 和 rs7172342位点多态性与四川汉族人群精神分裂症的关联性研究*
刘志容,陈 璐,彭顺香,吴晓蓉,钱琦琪,张录顺,程 丽
1.成都市第二人民医院 普外三科(成都 610017);2.成都医学院 生物医学系(成都 610500);3.成都医学院 检验医学院(成都 610500);4.发育与再生四川省重点实验室(成都 610500);5.成都医学院 基础医学院(成都 610500)
精神分裂症(schizophrenia,SCZ)作为世界上致残率最高的疾病之一,已经成为一个严重的公共卫生问题。SCZ是一组原因未明的严重精神疾病,其临床表现症状多样,常有感觉、思维、情感和行为等多方面障碍。SCZ严重损害全世界0.5%~1.0%人口的身体健康,在中国成年人中终生患病率约1.0%,但其发病机制至今尚不清楚。由于SCZ具有高度的遗传性,其遗传机制越来越受到人们的关注[1-2]。
昼夜节律系统对于人类行为和生理节律的正常调节至关重要。昼夜节律基因突变可影响正常神经生理,与自闭症和抑郁症等疾病的病理生理过程密切相关[3-4]。既往研究[5-7]显示,昼夜节律基因RORα多态性位点(rs782931、rs11639084和rs7172342)与双相情感障碍及SCZ的消极和精神错乱症状相关。但上述3个RORα多态性位点与四川汉族SCZ患者之间的关系尚未见文献报道。因此,本研究采用临床病例对照方法,探讨RORα多态性位点与四川汉族人群SCZ发病风险的相关性。
1 资料与方法
1.1 临床资料
选取2015-2016年四川大学华西医院连续招募的427例四川汉族人群为研究对象。纳入标准:1)根据《精神疾病诊断与统计手册》第四版(DSM-IV)精神分裂症的诊断标准,经2名精神科主任医师同时诊断为精神分裂症;2)除患SCZ,没有任何生理疾病或其他精神疾病;3)四川汉族。纳入143例SCZ患者作为病例组,284例健康人群作为对照组。纳入标准:1)没有严重的身体疾病及个人、家庭精神疾病史;2)四川汉族。
1.2 基因分型
用天根DNA 提取试剂盒从志愿者血样中提取基因组DNA,通过限制性片段长度多态性聚合酶链反应技术分析RORαrs782931、rs11639084和rs7172342位点的基因型。引物序列、扩增条件和限制酶如表1所示。酶切产物通过非变性聚丙烯酰胺凝胶垂直电泳和硝酸银染色法对其进行肉眼分型。为保证分型结果的准确性,随机选取10%的样本进行测序验证。

表1 扩增引物序列及扩增反应条件
1.3 统计学方法
采用SPSS 17.0统计软件进行数据处理。病例组和对照组基因的基因型和等位基因表达情况采用例数(%)描述,Hard-Wenborger平衡分析采用2检验。比值比(OR)和95%置信区间(CI)来评估特定等位基因或基因型与疾病的相对风险,检验水准ɑ除特别说明外均设定为0.05。
2 结果
所有纳入人群的基因型和等位基因频率结果显示,对照组所有基因型均符合Hard-Wenborger平衡(rs11639084P=0.27; rs7172342P=0.09;rs782931,P=0.19)。等位基因频率分布在病例组和对照组之间,差异无统计学意义(P>0.05)(表2)。rs11639084 CT基因型明显增加SCZ的患病风险(CT vs. TT, OR= 3.91, 95% CI: 2.31~6.63,P<0.001),而rs782931 GG基因型则降低SCZ的患病风险(GG vs.AA, OR= 0.07, 95 % CI: 0.01~0.56,P<0.001)(表3)。rs7172342多态性在病例组患者与对照组健康人群间比较,差异无统计学意义(P>0.05)(表2,表3)。
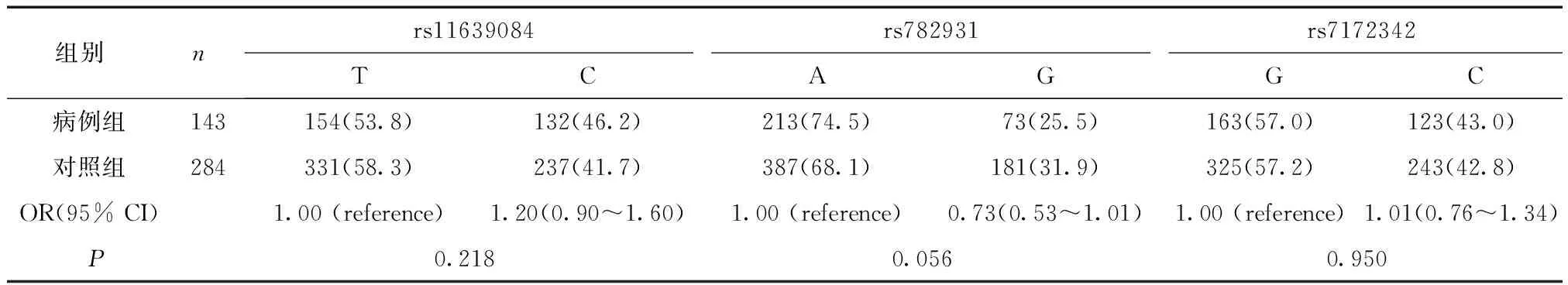
表2 两组rs782931、rs11639084和rs7172342多态性等位基因频率的比较[n(%)]
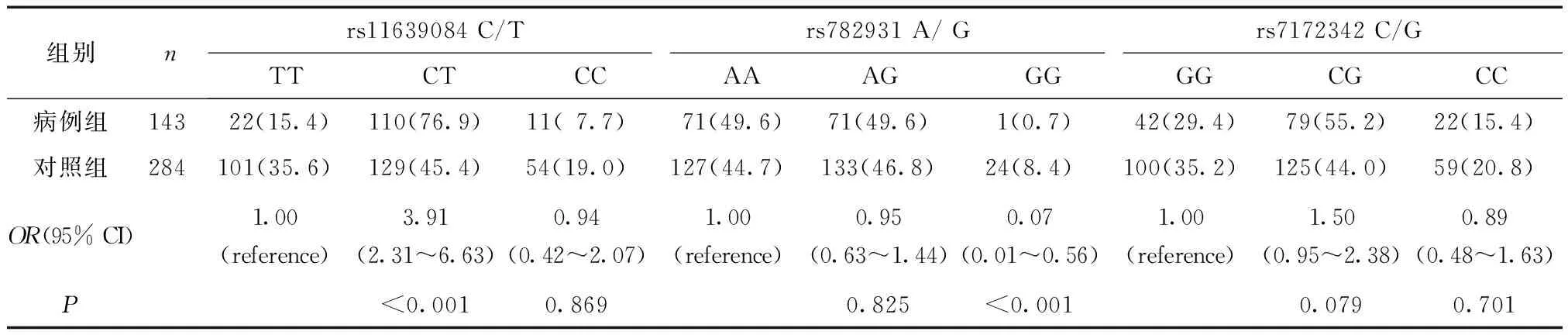
表3 两组rs782931、rs11639084和rs7172342多态性基因型频率的比较[n(%)]
3 讨论
维甲酸相关孤儿受体亚家族包含RORα、RORβ和RORγ,RORα是进化相关转录因子之一,属于类固醇激素受体超家族[8]。维甲酸相关孤儿受体亚家族广泛分布于机体的各个组织,包括脑、睾丸、肾脏、脂肪和肝脏,尤其在丘脑和小脑中表达量最高[9-10]。
RORα是多种生物进程的关键调控基因,参与各种生理过程,在调节细胞周期、激素分泌和控制体温[11],维持睡眠/觉醒周期、内分泌、生理和行为功能等方面起着关键作用[12]。既往研究[12]报道,作为生物节律的关键基因之一,RORα多态性与SCZ、双相情感障碍、抑郁、癫痫以及自闭症等疾病的发病进程相关。Etain等[6]研究结果显示,RORαrs782931与BD存在显著相关,RORα多态性影响了携带者的生理表型,降低了适应外部刺激的能力。Lai等[5]研究发现,RORαrs11639084和BD之间存在显著关联,提示RORαrs11639084促进BD的发生。Fanous等[7]分析了2 454例欧洲无症状型SCZ患者的心理健康量表评分与RORα多态性的关系,结果表明,RORαrs7172342与SCZ症状表型无关,该结果与我们在汉族人群中的调查结果一致。
综上所述,本研究表明RORαrs782931和RORαrs11639084多态性与SCZ发病风险存在相关性,这两个多态性位点可能参与了SCZ的发病进程,但该结果有待在更大样本量和遗传/环境交互分析研究中进一步证明。
[1]Xing J, Kimura H, Wang C,etal. Resequencing and Association Analysis of Six PSD-95-Related Genes as Possible Susceptibility Genes for Schizophrenia and Autism Spectrum Disorders[J]. Sci Rep, 2016, 6: 27491.
[2]Pouget J G, Goncalves V F,Schizophrenia Working Group of the Psychiatric Genomics Consortium ,etal. Genome-Wide Association Studies Suggest Limited Immune Gene Enrichment in Schizophrenia Compared to 5 Autoimmune Diseases[J]. Schizophr Bull, 2016, 42(5): 1176-1184.
[3]Sayad A, Noroozi R, Omrani M D,etal. Retinoic acid-related orphan receptor alpha (RORA) variants are associated with autism spectrum disorder[J]. Metab Brain Dis, 2017, 32(5): 1595-1601.
[4]Maglione J E, Nievergelt C M, Parimi N,etal. Associations of PER3 and RORA Circadian Gene Polymorphisms and Depressive Symptoms in Older Adults[J]. Am J Geriatr Psychiatry, 2015, 23(10): 1075-1087.
[5]Lai Y C, Kao C F, Lu M L,etal. Investigation of associations between NR1D1, RORA and RORB genes and bipolar disorder[J]. PLoS One, 2015, 10(3): e0121245.
[6]Etain B, Jamain S, Milhiet V,etal. Association between circadian genes, bipolar disorders and chronotypes[J]. Chronobiol Int, 2014, 31(7): 807-814.
[7]Fanous A H, Zhou B, Aggen S H,etal. Genome-wide association study of clinical dimensions of schizophrenia: polygenic effect on disorganized symptoms[J]. Am J Psychiatry, 2012, 169(12): 1309-1317.
[8]Jetten A M. Recent advances in the mechanisms of action and physiological functions of the retinoid-related orphan receptors (RORs)[J]. Curr Drug Targets Inflamm Allergy, 2004, 3(4): 395-412.
[9]Nakagawa Y, O'Leary D D. Dynamic patterned expression of orphan nuclear receptor genes RORalpha and RORbeta in developing mouse forebrain[J]. Dev Neurosci, 2003, 25(2/4): 234-244.
[10] Matysiak-Scholze U, Nehls M. The structural integrity of ROR alpha isoforms is mutated in staggerer mice: cerebellar coexpression of ROR alpha1 and ROR alpha4[J]. Genomics, 1997, 43(1): 78-84.
[11] Acevedo N, Sääf A, Söderhäll C,etal. Interaction between retinoid acid receptor-related orphan receptor alpha (RORA) and neuropeptide S receptor 1 (NPSR1) in asthma[J]. PLoS One, 2013, 8(4): e60111.
[12] Gooley J J. Circadian regulation of lipid metabolism[J]. Proc Nutr Soc, 2016, 75(4): 440-450.

