人源性乙酰胆碱受体α亚基胞外肽段的原核表达与血清学诊断研究
许胜杰,孙卫国,陈玉萍,王中魁,陶晓勇,王卫
解放军第三〇九医院 a.神经内科;b.全军结核病防治重点实验室,结核病诊疗新技术北京市重点实验室;北京 100091
重症肌无力(myastheniagravis,MG)是一种自身免疫性疾病,机制为血清中大量生成的乙酰胆碱受体(acetylcholine receptor,AchR)抗体与AchR结合,导致AchR生理功能低下,引发肌肉疲乏无力症状[1]。目前在我国人群中MG发病率较高,早发现及时治疗对改善预后具有重要意义。研究表明,血清中AchR抗体滴度与MG的病情密切相关,通过检测患者血清中AchR抗体水平可以对MG患者进行初步临床诊断和病情评估。神经肌肉接头处突触后膜的AchR是一个由4种亚基构成的五聚体跨膜蛋白,其中α亚基上存在众多抗原表位,AchR特异性T细胞及B细胞表位几乎均存在于α亚基上,α亚基有望作为抗原用来检测MG患者血清AchR抗体[2]。α亚基是一个具有4个跨膜区域的跨膜蛋白,其胞外域可用于免疫吸附、免疫动物制备实验性重症肌无力动物模型。我们构建了AchR的α亚基胞外氨基酸即第1~221位氨基酸(aa)序列的融合表达载体pETNusA-AchR-α,原核表达获得融合蛋白NusAAchR-α,纯化重组蛋白后进行血清学鉴定,对重组蛋白用于MG患者血清学诊断的价值进行评估,探讨开发临床检测MG试剂盒的可行性。
1 材料与方法
1.1 材料
临床阳性血清来自本院神经内科住院MG患者200例;健康人血清来自本院体检中心60例;大肠杆菌BL21(DE3)、质粒pET-NusA由本室保存;全基因和引物由华大基因公司合成;限制性内切酶HindⅢ和XhoⅠ、T4DNA连接酶购自NEB公司;TaqDNA聚合酶和dNTP购自天根生化生物公司;HRP酶标羊抗人IgG购自华美生物技术公司;琼脂糖为Spain公司产品;IPTG为Merck公司产品;蛋白质相对分子质量marker为Sigma公司产品;其他试剂为进口或国产分析纯产品。
在这个例句中,根据句义“the man to help you”可以理解为“the man who helps you”。因此,the man与help构成了主谓关系。
1.2 全基因与引物合成
全合成α亚基胞外氨基酸序列对应的核酸序列(GenBank:M64695),在上、下游 5′和 3′端分别引入HindⅢ酶切位点(AAGCTT)和XhoⅠ酶切位点(CTCGAG),在 3′端引入原核终止密码子TAA。合成全序列为:
aagcttTCCGAACATGAGACCCGTCTGGTGGCAAAGCTATTTAA AGACTACAGCAGCGTGGTGCGGCCAGTGGAAGACCACCGCCAGG TCGTGGAGGTCACCGTGGGCCTGCAGCTGATACAGCTCATCAAT GTGGATGAAGTAAATCAGATCGTGACAACCAATGTGCGTCTGAA ACAGCAATGGGTGGATTACAACCTAAAATGGAATCCAGATGACT ATGGCGGTGTGAAAAAAATTCACATTCCTTCAGAAAAGATCTGG CGCCCAGACCTTGTTCTCTATAACAATGCAGATGGTGACTTTGC TATTGTCAAGTTCACCAAAGTGCTCCTGCAGTACACTGGCCACA TCACGTGGACACCTCCAGCCATCTTTAAAAGCTACTGTGAGATC ATCGTCACCCACTTTCCCTTTGATGAACAGAACTGCAGCATGAA GCTGGGCACCTGGACCTACGACGGCTCTGTCGTGGCCATCAACC CGGAAAGCGACCAGCCAGACCTGAGCAACTTCATGGAGAGCGCC CCGACACCCCCTACCTGGACATCACCTACCACTTCGTCATGCAG CGCCTGTAActcgag
合成的阳性鉴定引物为:
正向 5′-CCCaagcttTCCGAACATGAGACCCGTCT-3′
反向 5′-CCGctcgagTTACAGGCGCTGCATGACGAAGTGG-3′
1.3 pET-NusA-AchR-α重组质粒的构建
合成的序列及表达载体pET-NusA分别用HindⅢ和XhoⅠ双酶切后切胶回收,回收后的产物按浓度比3∶1过夜连接,连接产物转化感受态大肠杆菌BL21(DE3),筛选PCR阳性菌落进行测序,获得工程菌pET-NusA-AchR-α。
1.4 NusA-AchR-α融合蛋白的原核表达
将阳性工程菌株转接至含卡那霉素的LB培养基中,于37℃振荡活化,扩大培养中检测细菌菌液D600nm值为0.4时加入IPTG(终浓度0.3mmol/L),37℃继续诱导7h,离心收集菌体,在冰浴状态下进行超声波破碎,高速离心(12000r/min,30min),取上清和沉淀进行SDS-PAGE分析。
1.5 NusA-AchR-α融合蛋白的纯化
取超声波破碎后上清,加入咪唑至终浓度为10mmol/L,充分混匀,通过镍离子螯合的亲和层析柱对目的蛋白进行亲和纯化,分别以30mmol/L咪唑除去菌体自身蛋白、150mmol/L咪唑洗脱收集目的融合蛋白,通过12%SDS-PAGE分析纯化后目的蛋白的纯度。
1.6 NusA-AchR-α融合蛋白的免疫印迹与ELISA分析
取NusA-AchR-α融合蛋白冻干粉末,用PBS缓冲液稀释成1mg/mL的母液,吸取2μL加入上样缓冲液煮沸8min,经12%SDS-PAGE后转移到硝酸纤维素膜上,用5%的脱脂奶粉封闭后,依次以确诊阳性MG患者血清、HRP标记的羊抗人IgG孵育,漂洗干净,通过ECL进行暗室自动曝光显影,分析重组蛋白的抗原性。
用碳酸钠溶液将融合蛋白稀释至4μg/mL备用,酶标板包被过夜后,37℃封闭2h,用PBST充分洗板5次,确诊MG患者血清和健康人血清(1∶200)于37℃孵育1h,重新洗板若干次,每孔中加入用PBS稀释至1∶1000的HRP标记的羊抗人IgG100 μL,37℃振荡孵育1h,再洗板 5次,加入TMB显色液反应30min显色,终止反应,酶标仪检测D450nm值,结果判定以待测样本的D450nm值与阴性对照的D450nm值之比≥210(P/N≥210)为阳性,显示阳性结果的最大抗体稀释度为血清效价。
2 结果
2.1 pET-NusA-AchR-α表达载体的构建
通过全基因合成的方法获得AchRα胞外肽段核酸全序列,克隆到载体pET-NusA中,以合成的引物通过菌落PCR筛选阳性克隆进行测序保存。PCR产物的1%琼脂糖电泳结果见图1,在约660bp处有单一的条带,和预期结果一致。
2.2 NusA-AchR-α融合蛋白的表达与纯化
NusA-AchR-α融合蛋白的相对分子质量约为80000(图2),与预期一致,目的蛋白的表达量占细菌总蛋白的25%~35%。SDS-PAGE分析表明重组蛋白主要表达于上清中,这同理论结果相同。前期实验中,我们尝试将AchRα亚基胞外段用pET-22b载体进行非融合表达,但没有获得成功。
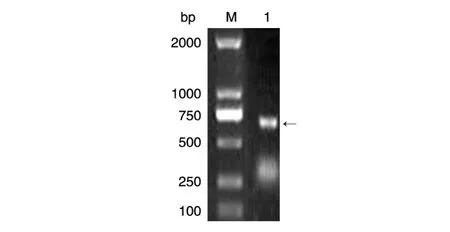
图1 AchRα胞外肽段核酸PCR产物的凝胶电泳鉴定
对重组 NusA-AchR-α表达后的上清液进行亲和柱纯化,SDS-PAGE分析纯化结果,重组蛋白纯度可达90%以上(图3)。
2.3 NusA-AchR-α融合蛋白的Western印迹鉴定
以确诊的MG患者血清为一抗与NC膜进行孵育,Western印迹表明融合蛋白NusA-AchR-α与MG患者血清结合,在胶片上显示出条带(图4)。而对照的NusA蛋白在对应位置没有出现条带。实验说明,纯化后的重组蛋白NusA-AchR-α相对于MG患者血清具有强的抗原性及特异性。
2.4 融合蛋白NusA-AchR-α的ELISA鉴定
收集200份MG患者血清和100份健康人血清对纯化的NusA-AchR-α重组蛋白进行ELISA分析,发现常规ELISA最佳重组抗原包被浓度为4μg/mL,96孔包被板背景较深,非特异结合较强,其中MG患者检出120例,检出率为60%;健康人血清检出5例,特异度为95%。
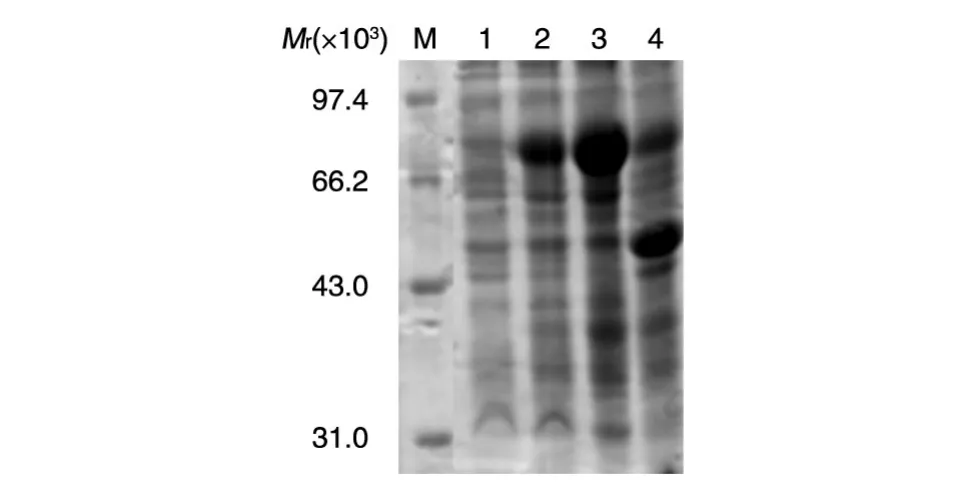
图2 pET-NusA-AchR-α原核表达产物的SDS-PAGE
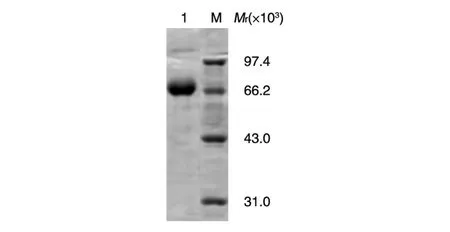
图3 NusA-AchR-α亲和纯化的SDS-PAGE分析
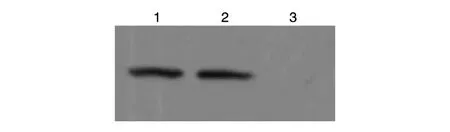
图4 NusA-AchR-α和MG患者血清的Western印迹抗原性分析
3 讨论
在MG患者发病过程中有多种抗体参与[3],我院神经内科研究发现MG患者的患病程度与Titin抗体浓度呈正相关[4]。刘岚剑等[5]研究发现,MG患者血清AchR抗体和Titin抗体阳性率均明显高于对照组,AchR抗体与Titin抗体检测重症肌无力的敏感度分别为76.3%和52.5%,2种抗体并联后敏感度可提高到86.3%。通过检测患者血清AchR抗体水平,可以初步预判MG症状,目前国内市场还没有血清学检测MG疾病的试剂,临床检测主要依赖国外进口试剂盒。为了对AchR抗体进行血清学检测,我们尝试对AchR的α亚基胞外段进行体外重组。同时,参考NusA蛋白标签系统能显著提高外源蛋白的可溶性表达功能,并且NusA标签还能使目的蛋白仍保持正确折叠和生物学活性的作用,将AchR-α与NusA进行融合表达,获得了重组NusA-AchR-α的可溶性表达,在后期的ELISA实验中,由于显色背景较深,阳性检出率不是很理想,但相对于对照血清而言还是能初步进行甄别。后期实验我们将对AchR序列进行抗原优化以提高特异性。本实验为开发MG临床血清学诊断研究做了初步尝试,也能为今后开发血清学检测试剂盒提供参考。

