他克莫司对γ干扰素刺激HaCaT细胞分泌趋化因子CXCL9和CXCL10的影响及机制研究
杨赛琳 许文 林福全 周妙妮 许爱娥
310009杭州,浙江中医药大学附属杭州第三医院皮肤科
白癜风是以Th1型细胞为主介导的疾病,γ干扰素(IFN-γ)是Th1淋巴细胞分泌的重要细胞因子之一,IFN-γ与受体结合后,促发Janus激酶信号转导和转录激活物(JAK-STAT)级联反应,促动JAKS和STAT磷酸化,诱导趋化因子表达[1]。趋化因子受体3及其配体CXCL9和CXCL10被认为是在白癜风等自身免疫和炎症过程中促进T细胞迁移最相关的趋化因子轴之一[2]。CXCL9、CXCL10等在白癜风发生发展中起关键作用[3-5]。在白癜风患者血清中CXCL9和CXCL10比健康人高,血清CXCL10可能是监测疾病活动和指导进展期白癜风治疗的新型生物标志物[6]。与健康人相比,在白癜风患者病灶周围皮肤中CXCL10和IFN-γ表达增加[2]。他克莫司(tacrolimus)是一种免疫调节剂,临床上已证明其治疗白癜风有效[7]。Tu等[1]研究表明,他克莫司对HaCaT细胞IFN-γ相关细胞因子产生影响。他克莫司下调IFN-γ诱导的IFN-γ受体α、磷酸化Janus激酶2(pJAK2)、磷酸化信号转导和转录激活因子1(pSTAT-1)和CXCL8表达。尚未见他克莫司对HaCaT细胞中IFN-γ诱导的趋化因子CXCL9、CXCL10及Janus激酶1信号途径的影响。本研究采用实时荧光定量PCR及Western印迹法检测他克莫司对IFN-γ刺激HaCaT细胞分泌CXCL9、CXCL10及相关信号途径关键蛋白的影响,为他克莫司治疗白癜风作用机制的研究提供依据。
一、材料
他克莫司由海正药业杭州有限公司生产(批号TAB0160901,纯度99.1%),rhIFN-γ为美国Perpotech公司产品,人角质形成细胞株HaCaT购于上海博谷生物科技有限公司,MTT、胎牛血清为美国Gbico公司产品,反转录PCR试剂盒为美国罗氏公司产品,CXCL9、CXCL10引物由广州复能公司设计合成。CXCL9、CXCL10抗体、ELISA试剂盒为美国Abcam公司产品,蛋白提取试剂盒、蛋白MARK为美国Fermentes公司产品。
二、方法
1.MTT法:取对数生长期HaCaT细胞,按1×105/ml浓度接种入96孔板,每孔100 μl。用二甲基亚砜(DMSO)配制他克莫司成1 kg/L溶液,用培养液稀释至1、10、20、40、60、80、100、120 mg/L,处理细胞,与空白对照组同置37℃、5%CO2条件下培养4 h。加入MTT溶液(5 g/L)10 μl/孔,4 h后弃上清液,加入DMSO 100 μl/孔,振荡10 min,置酶标仪于490 nm波长测吸光度(A值)。每组设3个复孔。细胞存活率=实验组A490/对照组A490×100%。
2.荧光定量PCR检测CXCL9、CXCL10 mRNA表达:分为空白对照组、IFN-γ组、他克莫司组及他克莫司+IFN-γ组。根据MTT结果选择20 mg/L他克莫司预处理HaCaT细胞4 h,用500 U/ml IFN-γ刺激细胞12 h,荧光定量PCR测定4组细胞内CXCL9、CXCL10 mRNA含量,严格按试剂盒步骤操作。
3.Western印迹法检测 CXCL9、CXCL10、p-JAK1、p-STAT1蛋白表达:分组同荧光定量PCR检测。20 mg/L他克莫司处理4 h,500 U/ml IFN-γ处理48 h。收集细胞,蛋白裂解液裂解,离心后收集上清液提取细胞总蛋白,测定蛋白浓度,每组各取50 μg总蛋白样品,经十二烷基硫酸钠-聚丙烯酰胺凝胶电泳后,电转移至二氟乙烯膜,5%牛血清白蛋白室温4℃封闭1 h,一抗(1∶1 000)4℃孵育过夜,洗膜后与辣根过氧化物酶标记二抗IgG抗体室温孵育1 h,与ECL显色剂以1∶1比例混合后孵育1 min,用保鲜膜包被后转X线片曝光3 min。以β肌动蛋白及磷酸化总蛋白为内参照。重复3次,Bio-Rad凝胶成像分析系统分析目的蛋白表达情况。
4.ELISA法检测HaCaT细胞上清液中CXCL9、CXCL10蛋白。分组处理同荧光定量PCR检测。实验严格按照试剂盒说明书操作。
5.统计方法:采用SPSS17.0统计分析软件,计量资料采用±s,两组间比较采用两独立样本t检验,多组样本采用单因素方差分析,P<0.05为差异有统计学意义。
三、结果
1.不同浓度他克莫司对HaCaT细胞增殖的影响:0、1、10、20、40、60、80、100、120 mg/L他克莫司处理4 h后,HaCaT细胞存活率分别为100%、85%、96%、90%、67%、13%、13%、12%、13%。与空白对照组比较,40~120 mg/L他克莫司对HaCaT细胞增殖有明显抑制作用(均P<0.05);0~20 mg/L他克莫司对HaCaT细胞增殖无显著影响(P>0.05)。
2.他克莫司对HaCaT细胞CXCL9、CXCL10 mRNA表达的影响:与空白对照组比较,IFN-γ组能明显增加CXCL9、CXCL10 mRNA表达,差异均有统计学意义(P<0.01)。与IFN-γ组比较,20 mg/L他克莫司能明显抑制IFN-γ刺激后细胞CXCL9、CXCL10 mRNA的表达,差异均有统计学意义(P<0.01)。见表1。
3.他克莫司对HaCaT细胞CXCL9、CXCL10及p-JAK1、p-STAT1蛋白表达的影响:见表2、图1。与空白对照组比较,IFN-γ组明显增加CXCL9、CXCL10及p-JAK1、p-STAT1蛋白表达,差异均有统计学意义(P<0.05)。与IFN-γ组比较,20 mg/L他克莫司明显抑制IFN-γ刺激后细胞CXCL9、CXCL10、p-JAK1、p-STAT1蛋白表达,差异有统计学意义(P<0.01)。
4.他克莫司对HaCaT细胞培养上清液CXCL9、CXCL10蛋白含量的影响:见表2。与空白对照组比较,IFN-γ组明显增加细胞培养上清液CXCL9、CXCL10蛋白的含量,差异均有统计学意义(P<0.01)。与IFN-γ组比较,20 mg/L他克莫司能明显抑制IFN-γ刺激后细胞培养上清液CXCL9、CXCL10蛋白含量,差异均有统计学意义(P<0.01)。
表1 20 mg/L他克莫司处理对500 U/ml γ干扰素刺激HaCaT细胞CXCL9、CXCL10 mRNA表达的影响(±s)
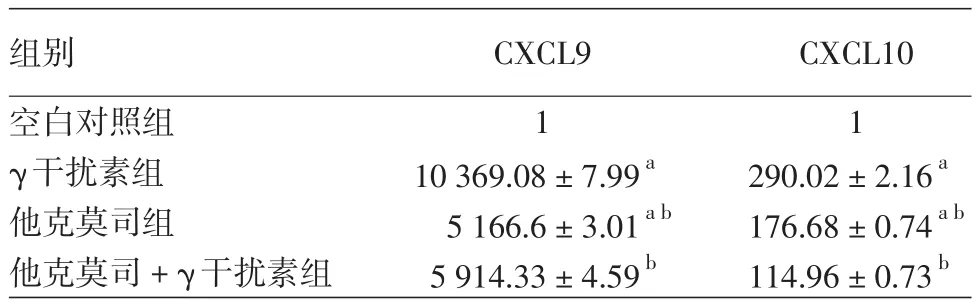
表1 20 mg/L他克莫司处理对500 U/ml γ干扰素刺激HaCaT细胞CXCL9、CXCL10 mRNA表达的影响(±s)
注:n=3。各组与空白对照组比较,aP<0.01。各组与γ干扰素组比较,bP<0.01
组别空白对照组γ干扰素组他克莫司组他克莫司+γ干扰素组CXCL9 1 10 369.08±7.99a5 166.6±3.01a b5 914.33±4.59bCXCL10 1 290.02±2.16a176.68±0.74a b114.96±0.73b
四、讨论
白癜风的治疗是一个挑战。糖皮质激素是最常用的药物,但长期大量使用会引起皮肤萎缩、毛细血管扩张、多毛症和痤疮等。他克莫司治疗白癜风,尤其是面颈部白癜风疗效好,安全性高,长期使用不会有外用糖皮质激素的不良反应[8]。Lan等[9]认为,他克莫司可通过刺激角质形成细胞释放干细胞生长因子,从而促进黑素细胞增殖。Kang等[10]发现,他克莫司可通过刺激酪氨酸酶活性和表达来促进黑素细胞色素生成和迁移。
本研究结果显示,IFN-γ对CXCL9和CXCL10基因表达的影响不同,CXCL9的表达量丰度比CXCL10高,该结果与文献报道一致。20 mg/L他克莫司能抑制HaCaT细胞中IFN-γ诱导的CXCL9、CXCL10的基因表达。CXCL9基因相对表达量减少43%,CXCL10基因相对表达量减少60%,表明他克莫司对CXCL10基因表达的抑制作用更强,具体原因有待进一步研究。20 mg/L他克莫司能抑制HaCaT细胞中JAK1及STAT1磷酸化;能抑制HaCaT细胞内与培养上清液中IFN-γ诱导的CXCL9、CXCL10蛋白表达。本研究为进一步阐明他克莫司治疗白癜风的作用机制及他克莫司的临床应用提供了一定实验依据。
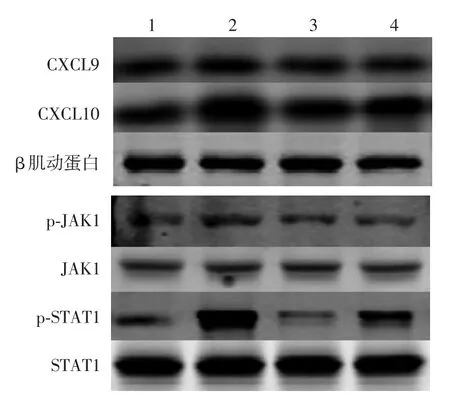
图1 20 mg/L他克莫司对HaCaT细胞CXCL9、CXCL10、p-JAK1、p-STAT1蛋白表达的影响 1:空白对照组;2:500 U/ml γ干扰素组;3:他克莫司组;4:他克莫司+γ干扰素组
表2 20 mg/L他克莫司对HaCaT细胞及其培养上清液CXCL9、CXCL10蛋白表达的影响(灰度值,±s)
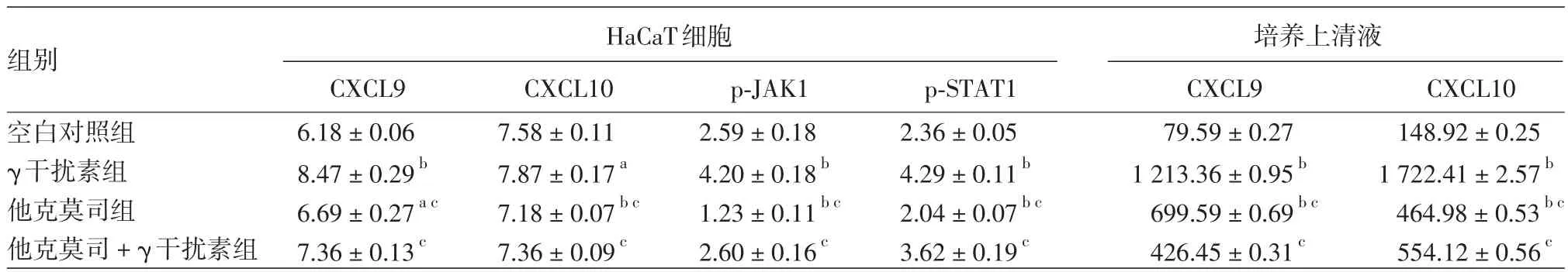
表2 20 mg/L他克莫司对HaCaT细胞及其培养上清液CXCL9、CXCL10蛋白表达的影响(灰度值,±s)
注:n=3。各组与空白对照组比较,aP<0.05,bP<0.01;各组与γ干扰素组比较,cP<0.01
组别HaCaT细胞空白对照组γ干扰素组他克莫司组他克莫司+γ干扰素组CXCL9 6.18±0.06 8.47±0.29b6.69±0.27a c7.36±0.13cCXCL10 7.58±0.11 7.87±0.17a7.18±0.07b c7.36±0.09cp-JAK1 2.59±0.18 4.20±0.18b1.23±0.11b c2.60±0.16cp-STAT1 2.36±0.05 4.29±0.11b2.04±0.07b c3.62±0.19c培养上清液CXCL9 79.59±0.27 1 213.36±0.95b699.59±0.69b c426.45±0.31cCXCL10 148.92±0.25 1 722.41±2.57b464.98±0.53b c554.12±0.56c

