梅毒IgA快速检测试剂诊断早期现症梅毒的应用性评估
韩燕 魏万惠 尹跃平 David Anderson 王红春 Mary L Garcia Huy Van 朱小宇 陈凯 陈祥生
210042南京,中国医学科学院 北京协和医学院 皮肤病研究所 中国疾病预防控制中心性病控制中心参比实验室(韩燕、魏万惠、尹跃平、王红春、朱小宇、陈凯),性病控制中心(陈祥生);Burnet Institute(David Anderson、Mary L Garcia、Huy Van)
梅毒螺旋体在母体内通过胎盘途径感染胎儿,可引起早产、死产。加强孕妇的梅毒筛查,是减少梅毒垂直传播的关键[1-3]。目前,梅毒的快速检测试剂(POC,point-of-care)主要检测梅毒的特异性抗体,不能够有效区分现症和既往梅毒感染,还需要快速血浆反应素环状卡片试验(RPR)/甲苯胺红不加热血清试验(TRUST)的辅助,限制了快速检测方法的应用。澳大利亚Burnet研究所研发了一种可快速鉴定患者是否为早期现症梅毒的POC试剂(prototype IgA rapid test),前期Burnet研究所利用墨尔本参比实验室提供的100份血浆标本检测,显示该试剂对现症梅毒患者血浆(RPR滴度≥1∶8)检测的灵敏度为91%,对既往梅毒患者血浆[梅毒螺旋体血球凝集试验(TPHA)阴性,RPR阴性]的检测特异性为80%。在本研究中,我们对该快速检测试剂进行了扩大样本量的实验室评估。
一、对象和方法
1.标本:血清标本来自中国医学科学院皮肤病研究所参比实验室。由于库存标本缺少患者主诉相关信息,我们主要依靠IgM酶联免疫吸附实验(IgM-ELISA)、IgA-ELISA检测的结果进行未感染梅毒、既往感染梅毒和早期现症梅毒的分组。本研究通过中国医学科学院皮肤病研究所医学伦理委员会批准(2016-临快审-016)。
2.试剂:TPHA试剂、RPR试剂(英国Omega Diagnostics公司);IgA-POC及IgA-ELISA试剂均由Burnet研究所提供,其制备IgA快速检测试纸条中所使用的IgA抗原梅毒重组抗原购自美国Meridian Life Sciences公司;IgM-ELISA试剂(德国DRG公司)。
3.分组:标本管理员根据标本库原先记录的检测结果进行标本抽样,完成抽样后,所有标本经TPHA和RPR检测,并利用IgM-ELISA发现TPHA和RPR检测漏检的早期梅毒感染者。未感染组:IgM-ELISA检测阴性或TPHA检测阴性且RPR检测阴性;既往感染组:TPHA检测阳性、RPR检测阴性且IgM-ELISA阴性;早期现症组:IgM-ELISA检测阳性或TPHA检测阳性、RPR检测阳性且滴度大于1∶8。为保证检测人员对TPHA和RPR结果的盲法,在完成分组标本的筛选后,对标本二次编号,号码按照随机数生成器产生,然后按序排列。实验人员在后续过程中对所有标本前期的检测结果及分组信息未知。
4.IgA-POC检测:冻存标本室温孵育至室温后,10 000×g离心5 min,加入5 μl血清标本至检测板的A孔,然后加入1滴磷酸盐缓冲液(PBS),10 min后再加入4滴PBS至B孔,20 min后观察,质控线出现粉红色条带时检测有效,检测线出现粉红色条带为阳性。
5.IgA-ELISA检测:在96孔板中包被IgA抗原作为IgA-ELISA的检测板。在酶标板孔中加入100 μl标本,37 ℃孵育1 h,洗板6次后加入100 μl抗人IgA辣根过氧化酶溶液继续37℃孵育1 h,洗板6次后加入3,3′,5,5′-四甲基联苯胺(TMB)底物100 μl,11 min后加入100 μl终止液,利用酶标仪检测吸光度(A值)。利用阴性质控及空白质控计算灰区值(cutoff),cutoff=(A阴性-A空白)× 0.9。每批实验单独计算cutoff值,检测的吸光度大于或等于cutoff值则判为阳性,小于cutoff值判为阴性。
6.统计学分析:采用SPSS 20进行统计分析。IgA-POC与IgM-ELISA方法灵敏度和特异性比较采用Z检验,IgAPOC与IgA-ELISA方法的比较采用配对资料McNemar检测,以P<0.05为差异有统计学意义。
二、结果
1.基本情况:抽取库存标本458份,男性标本241例,女性标本215例,2份标本缺少性别信息;年龄(38.2±12.3)岁。未感染梅毒148份、既往感染梅毒147份、早期现症梅毒163份(表1)。现症梅毒组有9例RPR阴性、IgM-ELISA阳性,其余154例RPR滴度在1∶8至1∶256之间,其中1∶16、1∶32及1∶64这3个滴度标本占全部标本80%左右。
2.IgA-POC与IgM-ELISA、IgA-ELISA检测结果比较:3份标本(0.65%)未出现质控线,没有纳入最终IgA评估,455份血清用于检测,结果见表2。IgM-ELISA试剂检测结果出现在灰区16份,占总标本的3.52%(16/455)。IgA-POC对早期现症感染诊断的灵敏度(92.64%)高于IgM-ELISA(Z=6.88,P<0.05);对既往感染排除诊断的特异性(72.22%)低于IgMELISA(Z=6.18,P<0.05);对未感染排除诊断的特异性(97.97%)与IgM-ELISA相比差异无统计学意义(Z=1.16,P=0.25)。IgA-POC对非早期现症梅毒排除诊断的特异性为85.27%,约登指数为64.86%;IgM-ELISA的特异性为99.32%,约登指数为58.83%。
IgA-ELISA与IgA-POC的检测能力差异有统计学意义(McNemarχ2=11.70,P=0.00)(表3)。IgA-POC对早期现症感染诊断的灵敏度及对既往感染排除诊断的特异性与IgAELISA差异无统计学意义(Z值分别为0.21、0.26,P>0.05),但对未感染排除诊断的特异性高于IgA-ELISA(Z=4.68,P<0.05);对非早期现症梅毒排除诊断的特异性为75.34%,低于IgA-POC的97.97%,约登指数为45.48%。
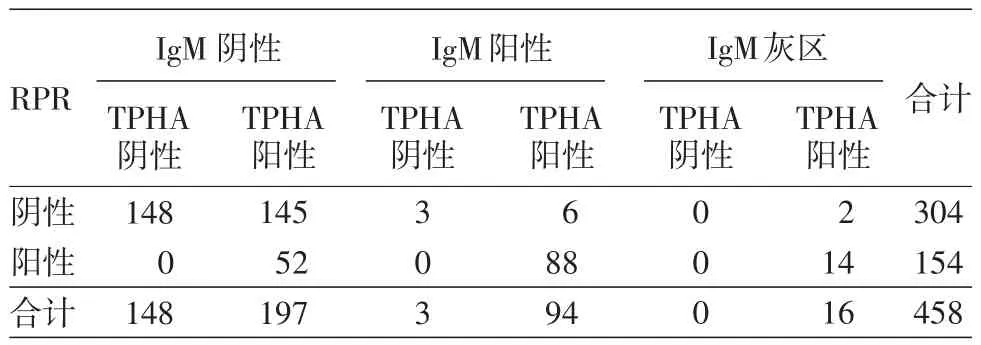
表1 458份血清标本IgM-ELISA、梅毒螺旋体血球凝集试验(TPHA)和快速血浆反应素环状卡片试验(RPR)结果
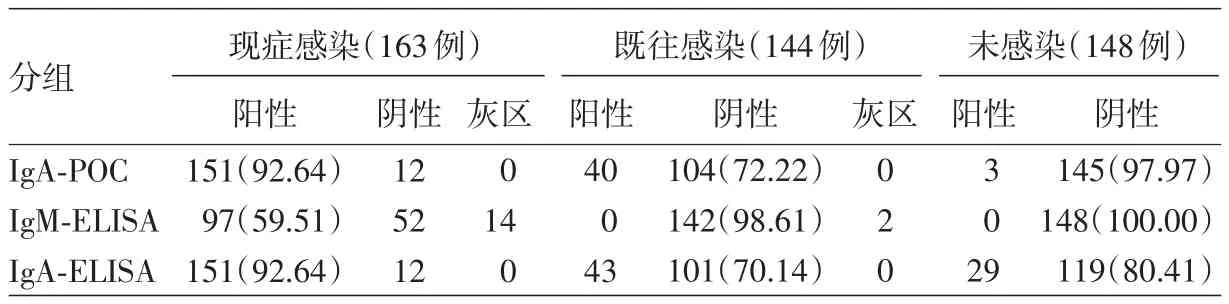
表2 IgA快速检测试剂(IgA-POC)、IgM-ELISA、IgA-ELISA对不同感染状态的梅毒血清标本的检测结果比较[例(%)]
三、讨论
梅毒特异性IgM和IgA可随着感染的时间及治疗而逐渐消失[4],且分子量比较大难以通过胎盘屏障[5],因此IgM和IgA抗体的检测可用于梅毒的早期诊断。本研究利用库存标本对梅毒IgA-POC进行了早期现症梅毒诊断的应用性评估,结果显示,该试剂对早期现症梅毒的发现能力达93%,对未感染梅毒和既往感染梅毒的排除率分别达98%和72%。目前IgA-POC尚处于研发阶段,对现症梅毒诊断特异性和灵敏度尚不能与美国Chembio公司梅毒双检的方法相媲美[6],但基本符合WHO对于新开发的POC试剂要求(临床灵敏度和特异性均大于80%)。由于该检测方法简便易行,所需实验室条件和设备要求不高,因此可以在实验室条件简陋的诊所或现场调查中推广。
由于IgM在感染者体内消失得较快,IgM-ELISA对早期现症感染的检测灵敏性低,应用该方法进行现症梅毒筛查时常会出现漏诊[7],因此IgA检测是对IgM检测诊断早期梅毒的有效补充。而本研究通过对IgA-POC与IgA-ELISA的比较发现,IgA-POC检测未感染排除诊断的特异性高于IgAELISA,这可能与两种方法的操作过程有关:IgA-POC抗原包被过程是通过胶体金划线仪将抗原划至硝酸纤维膜上,而IgA-ELISA主要通过排枪移液器吸附至96孔板;IgA-POC的检测为两步法,而IgA-ELISA涉及的步骤较为繁琐,没有实现自动化,增加了人为因素的干扰。
本研究使用的是库存标本,缺少临床诊断相关信息,因此可能存在错误分组的情况,影响对该试剂的灵敏度和特异性的计算,需要进一步开展多中心临床标本评估。

表3 IgA-ELISA与IgA快速检测试剂(IgA-POC)检测结果比较

