超高效液相色谱-三重四极杆质谱法同时检测人尿中12种单羟基多环芳烃代谢物
付 慧, 胡小键, 陈 曦, 林少彬
(中国疾病预防控制中心环境与健康相关产品安全所, 北京 100021)
多环芳烃(PAHs)作为一类广泛存在的环境致癌性化合物,受到国内外研究者的普遍关注。人类主要通过摄入含有PAH的食物或者吸入带有PAH的空气而受到污染[1-4]。进入体内的PAH在肝脏内分两步转化为结合态羟基多环芳烃(OH-PAH),而后经尿液或粪便排出体外。由于PAH在体内代谢期较短,因而测定尿中OH-PAH可反映近期PAH暴露情况[5]。以往的研究结果表明,应该选择多个PAH代谢物(尤其是致癌性多环芳烃如苯并[a]蒽、苯并[a]芘等)作为生物标志物,来联合评价人体的PAHs暴露。由于高环数多环芳烃主要经粪便排泄,在尿中的浓度很低[6,7],需要有更灵敏的方法对尿中多种OH-PAHs代谢物进行同时测定,以期发现适于联合评价PAHs内暴露水平的OH-PAHs。
目前,测定尿中多环芳烃代谢物的方法主要有气相色谱-质谱联用法[5,9-13]、液相色谱法[14-18]和液相色谱-质谱联用法[19-26]。美国疾病控制与预防中心(CDC)采用气相色谱-串联质谱(GC-MS/MS)法测定尿中24种OH-PAH,尿液样品经液液萃取后再浓缩100倍,衍生化后进行仪器分析[5]。该方法作为标准操作方法用于美国生物监测项目中尿液的测定,方法具有较高的灵敏度(检出限达0.01 μg/L),但是前处理繁琐,使用有机溶剂较多,大批量样品测定时效率低下。高效液相色谱-荧光检测法[14,16,17]具有选择性强、分析时间短、检出限低和重现性好等优点,但对荧光强度较弱的化合物则无法测定。液相色谱-质谱联用法省略了气相色谱-质谱联用法繁琐的前处理过程,且多反应监测模式(MRM)的应用避免了分析过程中基质的杂质干扰,使检出限明显降低。目前,国内对于多环芳烃的职业暴露研究多于非职业暴露,且可以测定的生物标志物少,这与分析手段不够先进,检出限高有关。全面了解不同地区PAHs的人体内暴露水平,将为政府职能部门提供可靠的基础数据,为PAHs污染防控提供建议。因此发展快速灵敏、实用的分析检测方法仍是分析化学工作者努力的方向。

1 实验部分
1.1 仪器、试剂与材料
API4000三重四极杆质谱仪(ESI源,美国Applied Biosystems公司), Acquity UPLC I-Class系统(美国Waters公司),纯水机(美国Barnstead公司), Mettler AE 163十万分之一电子天平(瑞士Mettler公司), C18固相萃取柱(3 mL/500 mg)(美国Supelco公司), 0.2 μm GHP针头过滤器(美国Waters公司)。

甲醇(HPLC级,美国Fisher公司),无水醋酸铵、冰醋酸(分析纯,国药集团),β-葡萄糖苷酸酶、芳基硫酸酯酶(美国Sigma-Aldrich公司),人工尿样(湖州英创生物科技公司)。
人体尿液实际样品采自淮河流域的100名志愿者。
1.2 标准溶液配制
OH-PAHs标准溶液:准确称取一定量的目标化合物的标准品,以甲醇为溶剂配成质量浓度约为1.00 g/L的单标储备液;12种单标储备液各取一定体积混合后,用甲醇定容,配制成各组分质量浓度均为100 mg/L的混合标准中间液。用甲醇逐级稀释得到使用液。

饱和醋酸-醋酸铵缓冲溶液:准确称取740.0 g无水醋酸铵,加入500 mL水,用超声波振荡器振荡溶解,用冰醋酸调pH至5.0。水解酶溶液:按照每个样品使用3 000 Uβ-葡萄糖苷酸酶、70 U芳基硫酸酯酶的量,根据所购β-葡萄糖苷酸酶、芳基硫酸酯酶的含量,计算实验所需水解酶的量,准确称取(3 000×(n+3)/A) gβ-葡萄糖苷酸酶和(70×(n+3)/B) g芳基硫酸酯酶(n为样品数,通常多加3份样品的量;A、B分别为两种酶的比活力,U/g),用饱和醋酸-醋酸铵缓冲溶液控温超声溶解并定容至10×(n+3) mL,现用现配。
1.3 实验方法
1.3.1样品前处理
将冰冻尿样放置至室温,准确移取10.0 mL尿样于25.0 mL玻璃试管中,分别加入100 μL 200 μg/L的内标溶液和10.0 mL的水解酶溶液,充分混匀后置于37 ℃恒温箱中避光水解16 h,得水解液。依次用5.0 mL甲醇、5.0 mL水活化C18固相萃取柱,将水解液通过C18固相萃取柱富集,用1.0 mL水淋洗小柱,氮气吹干40 min,然后用1.0 mL甲醇以0.25 mL/min进行洗脱,收集洗脱液,用甲醇定容至1.0 mL,混匀,0.2 μm GHP针头过滤器过滤后,待测。
1.3.2色谱条件
Acquity UPLC®HSS T3色谱柱(100 mm×2.1 mm, 1.8 μm);柱温:25 ℃;进样量3.00 μL;流速0.25 mL/min;流动相:甲醇(A)和水(B);梯度洗脱程序:0~22 min, 55%A~85%A; 22~25 min, 85%A~55%A。
1.3.3质谱条件
ESI离子源,负离子多反应监测(MRM);雾化气:高纯氮气;碰撞气(CAD): 83 kPa;气帘气(CUR): 138 kPa;雾化气(GS1): 172 kPa;辅助气(GS2): 241 kPa;喷雾电压(IS): -4 000 V;离子源温度(TEM): 450 ℃;扫描时间:100 ms;其他质谱参数见表1。
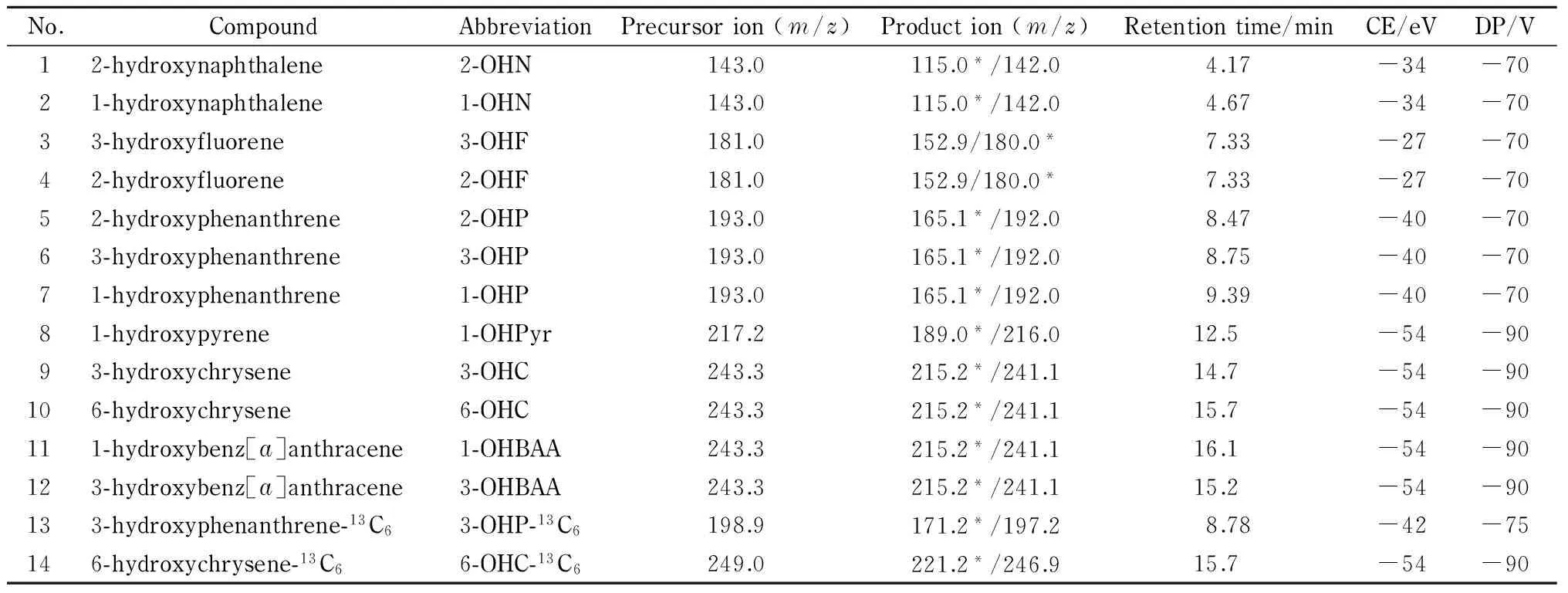
表 1 12种OH-PAHs和2种同位素内标的保留时间、监测离子、碰撞电压(CE)和去簇电压(DP)
* Quantitative ion.
2 结果与讨论
2.1 质谱条件的选择
用甲醇将14种物质的标准储备液分别稀释成100 μg/L的标准使用液,采用流动注射方式,以10 μL/min的流速进样,在正离子和负离子模式下进行全扫描,以选择适当的电离方式和分子离子峰。结果表明,在负离子模式下,目标化合物全扫描的分子离子[M-H]-最理想;以目标化合物的[M-H]-为母离子进行子离子扫描,选择丰度最高、干扰较少的两个子离子,优化CE和DP;用100 μg/L混合标准溶液,在负离子模式下,以MRM方式优化CUR、CAD、GS1、GS2、IS、TEM等参数,结果见表1。
2.2 色谱条件的优化
比较了14种物质在Acquity UPLC®BEH C18色谱柱(100 mm×2.1 mm, 1.7 μm)和Acquity UPLC®HSS T3色谱柱(100 mm×2.1 mm, 1.8 μm)上的保留行为。结果显示,在C18色谱柱上3-OHP和2-OHP不能完全分离,3-OHC和3-OHBAA无法完全分离;在T3色谱柱上,只有2-OHF和3-OHF无法完全分离,其他化合物均得到较好分离,目标化合物的响应值较高,各物质峰形尖锐、对称,峰形较好。另外,比较了甲醇-水、乙腈-水、0.05%(v/v)氨水乙腈-水、0.1%(v/v)氨水乙腈-水和0.2%(v/v)氨水-乙腈流动相对14种物质离子化程度的影响。结果表明,使用甲醇-水溶液体系时选择离子的色谱峰形和灵敏度均优于其他溶液体系。方法选用Acquity UPLC®HSS T3色谱柱(100 mm×2.1 mm, 1.8 μm),用甲醇-水流动相进行梯度洗脱,尿中目标化合物的MRM色谱图见图1。将14个目标化合物单标溶液在最佳仪器条件下分别进样以确定各目标化合物的保留时间,见表1。
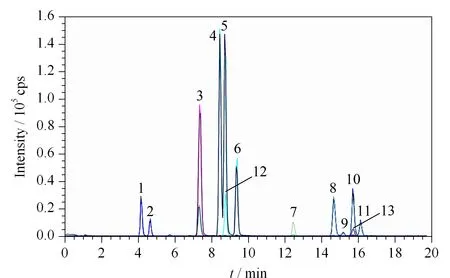
图 1 14种OH-PAHs的MRM色谱图Fig. 1 MRM chromatogram of the fourteen OH-PAHs Peak identifications: 1. 2-OHN; 2. 1-OHN; 3. 3-OHF & 2-OHF; 4. 2-OHP; 5. 3-OHP; 6. 1-OHP; 7. 1-OHPyr; 8. 3-OHC; 9. 3-OHBAA; 10. 6-OHC; 11. 1-OHBAA; 12. 3-OHP-13C6; 13. 6-OHC-13C6.
2.3 前处理条件的优化
2.3.1淋洗溶剂及用量的选择
为了减小尿样基体的干扰,提高实验的灵敏度,实验在水解液通过固相萃取柱富集后,加入了淋洗步骤。考察了不同配比的甲醇-水、乙腈-水和纯水淋洗对目标化合物回收率的影响。结果表明,纯水淋洗效果较好,因此实验采用1.0 mL纯水进行淋洗。
2.3.2浓缩方式的选择
实验比较了浓缩和直接洗脱进样对实验结果的影响。取2份平行尿样,分别加入等量的标准品,37 ℃恒温避光酶解16 h,将酶解液通过固相萃取小柱富集、淋洗后,一份用1.0 mL甲醇进行洗脱、定容至1.0 mL后待测;另一份用5.0 mL甲醇洗脱,真空浓缩仪35 ℃浓缩至干后,1.0 mL甲醇溶解定容后待测。结果表明,直接洗脱进样所测样品的峰面积明显高于浓缩后测定样品。采用真空浓缩方式进行样品浓缩时,1-OHN和2-OHN两种物质损失较为严重;用1.0 mL甲醇进行洗脱,定容至1.0 mL后测定,既省去了浓缩步骤,又可以达到良好的实验效果。
2.4 方法学考察
2.4.1线性范围和检出限
本方法采用内标法定量。向人工尿样中加入系列混合标准溶液和内标溶液,配制成质量浓度分别为0、0.04、0.10、0.40、1.00、2.00、10.0、20.0 μg/L,内标质量浓度为2.00 μg/L的标准工作曲线。经过与样品相同的前处理后,在优化的实验条件下测定。2-OHN、1-OHN、3-OHF、2-OHF、3-OHP、2-OHP和1-OHP以3-OHP-13C6为内标,1-OHPyr、3-OHC、6-OHC、1-OHBAA、3-OHBAA以6-OHC-13C6为内标,进行定量计算。以被测组分质量浓度为横坐标(x, μg/L),被测组分定量离子峰面积与内标物定量离子峰面积比为纵坐标(y),进行线性回归分析,得到12种目标化合物的线性方程和相关系数。采用空白样品中添加目标物的方法,以3倍信噪比(S/N)对应的质量浓度确定检出限(LOD), 10倍信噪比(S/N)对应的质量浓度确定定量限(LOQ)。12种目标化合物在0.04~20.0 μg/L范围内线性关系良好,相关系数>0.99,方法检出限为0.01~0.41 μg/L,定量限为0.04~1.35 μg/L。线性方程和检出限见表2。
2.4.2回收率和精密度
取一实际尿样,分别在高、中、低3个浓度水平下加标,每个加标样品做6个平行样。采用1.3.1节样品前处理方法处理加标样品,在最佳仪器条件下,依次进样,将测试样各组分的峰面积代入工作曲线的线性回归方程,计算各组分的浓度。同样条件处理样品3批,进行测定。计算准确度、批内精密度和批间精密度。准确度以加标回收率表示,批内和批间精密度以相对标准偏差(RSD)表示。样品平均回收率和精密度见表3。
2.5 实际样品测定
采用本实验条件和方法,对淮河流域某区域的100份人体尿样进行了检测,以期了解该地区不同人群的PAHs内暴露水平。结果显示,OH-PAHs的检出率为98%,检出率由高到低,分别为2-OHP、3-OHP、2-OHN、1-OHN、1-OHP和3-OHF & 2-OHF,其余物质未检出。以2-OHN为例,其检出率为40%,检出范围为0.10~3.62 μg/L,四分位距为0.23 μg/L,结果详见表4。
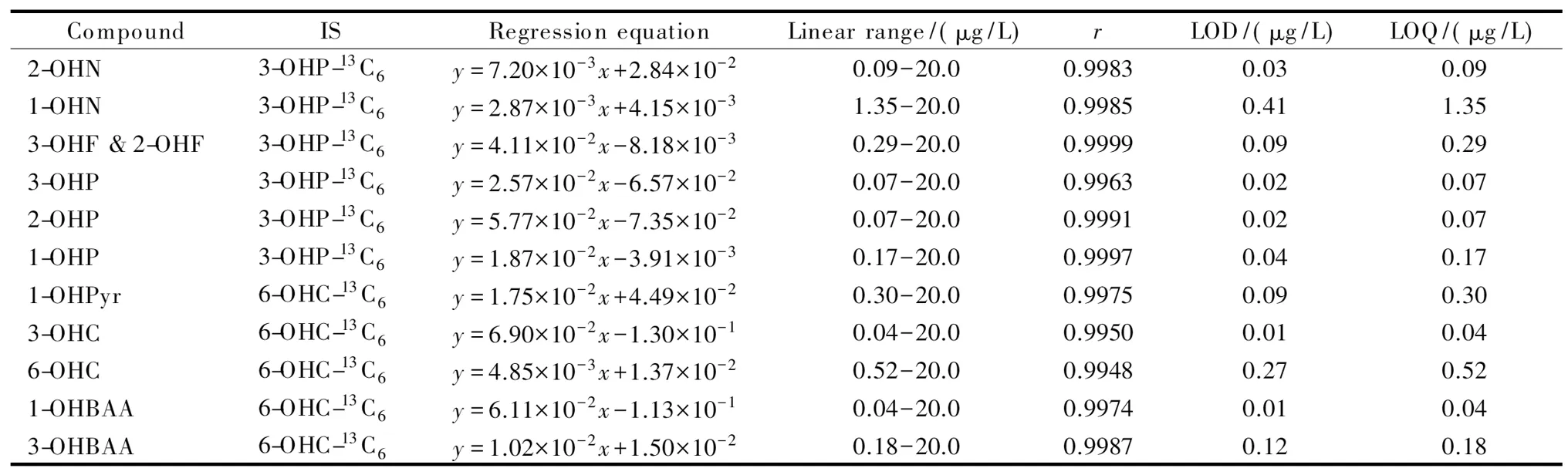
表 2 12种OH-PAHs的定量内标、回归方程、线性范围、相关系数(r)、检出限和定量限
y: peak area ratio of quantitative ions of the measured component to the internal standard;x: mass concentration of the measured component, μg/L.
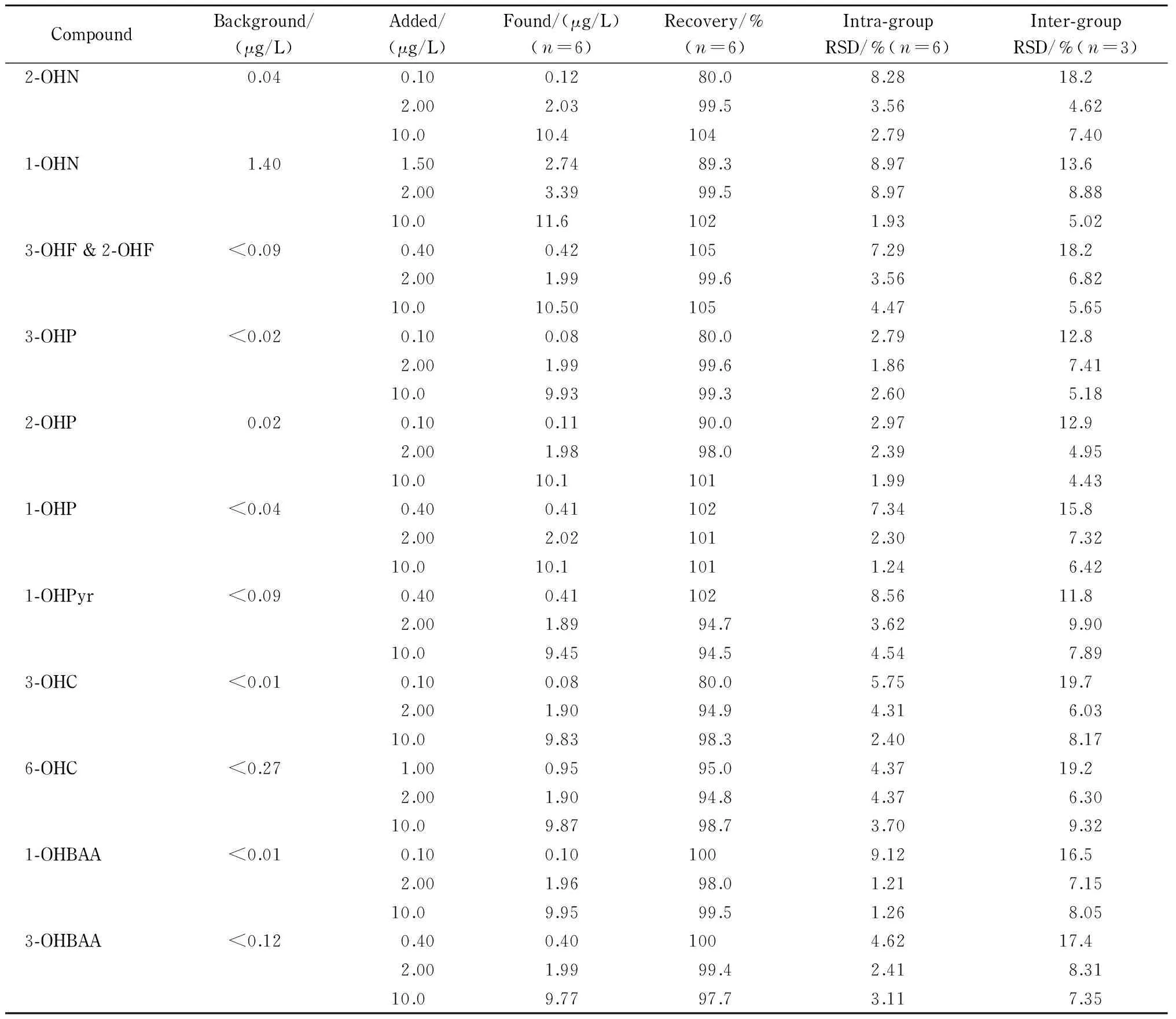
表 3 12种OH-PAHs在尿中3个水平下的加标回收率和精密度(n=6)
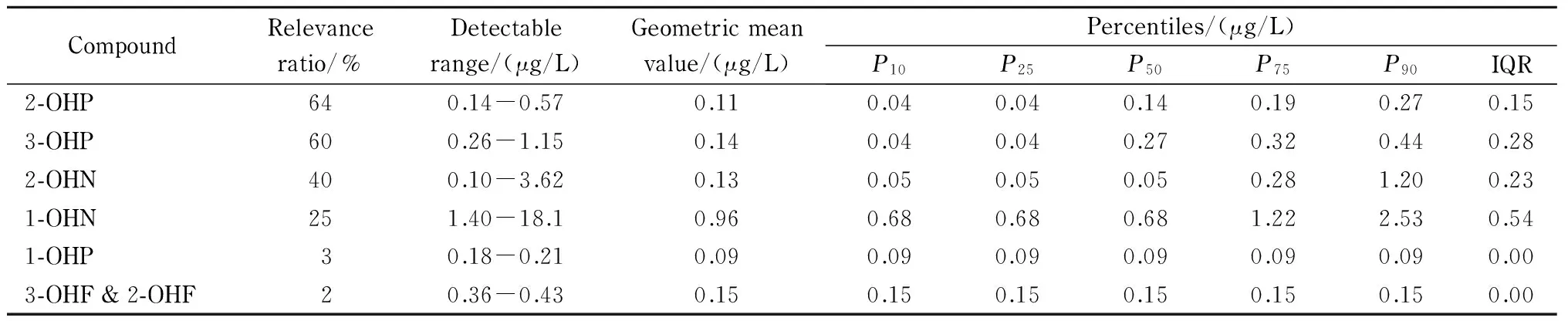
表 4 100份尿样中12种OH-PAHs的检测结果
*IQR: interquartile range.
3 结论

:
[1] Song X J, Li H Y, Yin M M, et al. Chinese Journal of Chromatography, 2018, 36(1): 51
宋晓娟, 李海燕, 尹明明, 等. 色谱, 2018, 36(1): 51
[2] Wang M F, Yang L L, Hu E Y. Chinese Journal of Chromatography, 2017, 35(6): 669
王美飞, 杨丽莉, 胡恩宇. 色谱, 2017, 35(6): 669
[3] Feng L, Zhang S J, Zhu G H, et al. Chinese Journal of Chromatography, 2017, 35(4): 466
冯利, 张胜军, 朱国华, 等. 色谱, 2017, 35(4): 466
[4] Zhao B, Li Y Q, Zhang S K, et al. Chinese Journal of Chromatography, 2014, 32(9): 960
赵波, 黎玉清, 张素坤, 等. 色谱, 2014, 32(9): 960
[5] Li Z, Romanoff L C, Trinidad D A, et al. Anal Chem, 2006, 78(16): 5744
[6] Pang Y H, Ma Y, Cui Y, et al. Journal of Environment and Health, 2012, 29(6): 567
庞月红, 马芸, 崔燕, 等. 环境与健康杂志, 2012, 29(6): 567
[7] Song X L, Hu X J, Lin S B. Journal of Environment and Health, 2017, 34(6): 555
宋喜丽, 胡小键, 林少彬. 环境与健康杂志, 2017, 34(6): 555
[8] Li Z, Romanoff L C, Trinidad D A, et al. Anal Bioanal Chem, 2014, 406(13): 3119
[9] Campo L, Mercadante R, Rossella F, et al. Anal Chim Acta, 2009, 631(2): 196
[10] Mattarozzi M, Musci M, Careri M, et al. J Chromatogr A, 2009, 1216(30): 5634
[11] Campo L, Rossella F, Fustinoni S. J Chromatogr B, 2008, 875(2): 531
[12] Romanoff L C, Li Z, Young K J, et al. J Chromatogr B, 2006, 835(1/2): 47
[13] Smith C J, Huang W, Walcott C J, et al. Anal Bioanal Chem, 2002, 372(1): 216
[14] Maisonnette C, Simon P, Hennion M C, et al. J Chromatogr A, 2006, 1120(1/2): 185
[15] Yang H M, Wang Y S, Li J H, et al. Applied Chemical Industry, 2014, 43(5): 957
杨红梅, 王永生, 黎俊宏, 等. 应用化工, 2014, 43(5): 957
[16] Wang Y, Dong Y L, Fan R F, et al. Journal of Environment and Health, 2006, 23(1): 76
王宇, 董玉莲, 范瑞芳, 等. 环境与健康杂志, 2006, 23(1): 76
[17] You F, Zhu L, He L, et al. Chinese Journal of Analytical Chemistry, 2014, 42(12): 1723
游钒, 朱岚, 何玲, 等. 分析化学, 2014, 42(12): 1723
[18] Chauhan A, Bhatia T, Singh A, et al. J Chromatogr B, 2015, 985: 110
[19] Ramsauer B, Sterz K, Hagedorn H W, et al. Anal Bioanal Chem, 2011, 399(2): 877
[20] Chen Y S, Wang S, Yu J J, et al. Tobacco Science & Technology, 2012(4): 37
陈玉松, 王昇, 余晶晶, 等. 烟草科技, 2012(4): 37
[21] Fan R F, Ramage R, Wang D L, et al. Talanta, 2012, 93(11): 383
[22] Zhao G, Chen Y, Wang S, et al. Talanta, 2013, 116(22): 822
[23] Li X X, Cui S W, He M F, et al. Chinese Preventive Medicine, 2012, 13(4): 246
李欣欣, 崔师伟, 何民富, 等. 中国预防医学杂志, 2012, 13(4): 246
[24] Ding C M, Jin Y L, Lin S B. Chinese Journal of Analytical Chemistry, 2012, 40(3): 397
丁昌明, 金银龙, 林少彬. 分析化学, 2012, 40(3): 397
[25] Huang C F, Yan H F, Pan Z F, et al. Journal of Hygiene Research, 2010, 39(3): 355
黄传峰, 闫慧芳, 潘祖飞, 等. 卫生研究, 2010, 39(3): 355
[26] Zheng L, Ding C M, Hu X J, et al. Journal of Environment and Health, 2011, 28(4): 348
郑磊, 丁昌明, 胡小键, 等. 环境与健康杂志, 2011, 28(4): 348

